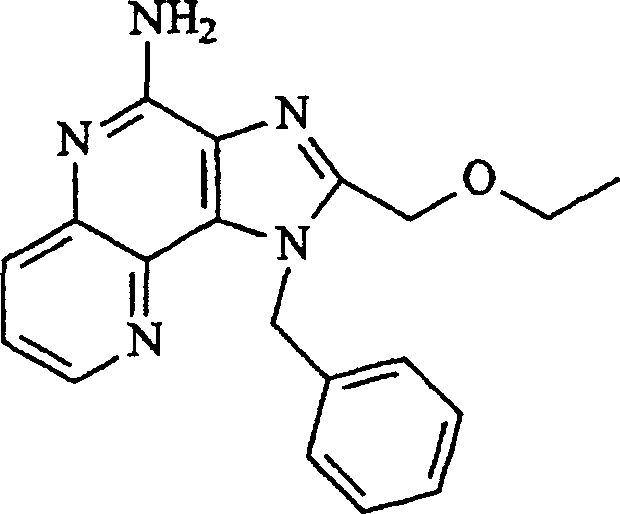
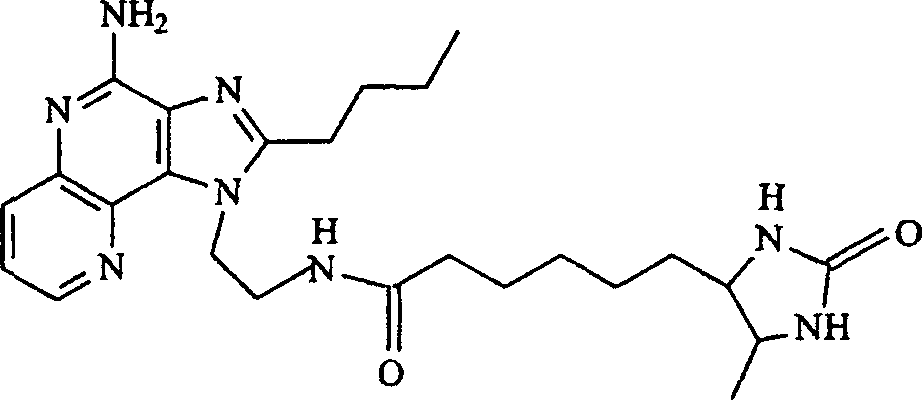
-
Die
vorliegende Erfindung betrifft Imidazonaphthyridin- und Tetrahydroimidazonaphthyridinverbindungen,
Verfahren zur Herstellung dieser Verbindungen und bei ihrer Herstellung
verwendete Zwischenprodukte. Die vorliegende Erfindung betrifft
außerdem
pharmazeutische Zusammensetzungen, die Imidazonaphthyridin- und
Tetrahydroimidazonaphthyridinverbindungen enthalten. Ein weiterer
Aspekt der vorliegenden Erfindung betrifft die Verwendung dieser
Verbindungen als Immunmodulatoren und zur Induktion der Cytokin-Biosynthese
in Tieren sowie die Verwendung der obigen Verbindungen zur Herstellung
eines Arzneimittels zur Behandlung einer Virusinfektion in einem
Tier.
-
Im
ersten zuverlässigen
Bericht über
das 1H-Imidazo[4,5-c]chinolin-Ringsystem
beschreiben Backman et al., J. Org. Chem. 15, 1278-1284 (1950),
die Synthese von 1-(6-Methoxy-8-chinolinyl)-2-methyl-1H-imidazo[4,5-c]chinolin
für eine
mögliche
Verwendung als Antimalariamittel. Danach wurde über Synthesen verschiedener
substituierter 1H-Imidazo[4,5-c]chinoline berichtet. Beispielsweise
synthetisierten Jain et al., J. Med. Chem. 11, S. 87-92 (1968),
die Verbindung 1-[2-(4-Piperidyl)ethyl]-1H-imidazo[4,5-c]chinolin
als mögliches
Antikonvulsivum und Herz-Kreislauf-Mittel. Außerdem berichteten Baranov
et al., Chem. Abs. 85, 94362 (1976), über einige 2-Oxoimidazo[4,5-c]chinoline
und Berenyi et al., J. Heterocyclic Chem. 18, 1537-1540 (1981), über bestimmte
2-Oxoimidazo[4,5-c]chinoline.
-
Später stellte
sich heraus, daß bestimmte
1H-Imidazo[4,5-c]chinolin-4-amine
und 1- und 2-substituierte Derivate davon zur Verwendung als Virustatika,
Bronchodilatoren und Immunmodulatoren geeignet sind. Diese werden
u.a. in den US-Patentschriften 4,689,338, 4,698,348, 4,929,624,
5,037,986, 5,268,376, 5,346,905 und 5,389,640, auf die hiermit ausdrücklich Bezug
genommen wird, beschrieben. Obwohl nach wie vor Interesse an Imidazochinolinringsystem
besteht, wie beispielsweise in der WO 98/30562 zu sehen ist, besteht
nach wie vor Bedarf an Verbindungen, die zur Modulierung der Immunantwort
durch Induktion der Cytokin-Biosynthese oder anderen Mechanismen
befähigt
sind.
-
Außerdem bezieht
sich die US-A-4689338 auf 1H-Imidazo[4,5-c]chinolin-4-amine
als Virustatika. Des weiteren werden pharmakologische Verfahren
zur Verwendung derartiger Verbindungen und pharmazeutische Zusammensetzungen,
die derartige Verbindungen enthalten, beschrieben.
-
In
der US-A-5482936 werden Verbindungen und pharmazeutisch unbedenkliche
Salze davon beschrieben, die sich formal durch Überbrückung der 1- und 2-Position
von 1H-Imidazo[4,5-c]chinolin-4-aminen ergeben.
-
Es
wurde nun eine neue Klasse von Verbindungen gefunden, die zur Verwendung
bei der Induktion der Cytokin-Biosynthese in Tieren geeignet sind.
Gegenstand der vorliegenden Erfindung sind demgemäß Imidazonaphthyridinverbindungen
der Formel I:
worin A, R
1 und
R
2 die nachstehend angegebene Bedeutung
besitzen.
-
Gegenstand
der Erfindung sind auch Tetrahydroimidazonaphthyridinverbindungen
der Formel II:
worin B, R
1 und
R
2 die nachstehend angegebene Bedeutung
besitzen.
-
Die
Verbindungen der Formel I und Formel II eignen sich zur Verwendung
als die Immunantwort modifizierende Mittel, da sie bei Verabreichung
an Tiere zur Induktion der Cytokin-Biosynthese und anderweitigen Modulierung
der Immunantwort befähigt
sind. Aufgrund dieser Fähigkeit
sind die Verbindungen zur Verwendung bei der Behandlung verschiedener
Leiden, z.B. Viruserkrankungen und Tumore, die auf derartige Änderungen
der Immunantwort ansprechen, geeignet.
-
Gegenstand
der Erfindung sind ferner pharmazeutische Zusammensetzungen, die
eine Verbindung der Formel I oder Formel II enthalten, und Verfahren
zur Induktion der Cytokin-Biosynthese in einem Tier und/oder zur
Behandlung einer Virusinfektion bei einem Tier durch Verabreichung
einer Verbindung der Formel I oder Formel II an das Tier.
-
Darüberhinaus
werden Verfahren zur Synthese von Verbindungen der Formel I und
Formel II und zur Verwendung bei der Synthese dieser Verbindungen
geeignete Zwischenprodukte bereitgestellt.
-
Gegenstand
der Erfindung ist ferner ein Verfahren zur Induktion der Interferon-Biosynthese
in einem Tier, bei dem man eine Verbindung der Formel I oder Formel
II in einer zur Induktion der Interferon-Biosynthese wirksamen Menge
an das Tier verabreicht, und ein Verfahren zur Behandlung einer
Virusinfektion bei einem Tier, bei dem man eine Verbindung der Formel
I oder Formel II in einer zur Inhibierung der Virusinfektion wirksamen
Menge an das Tier verabreicht.
-
Gegenstand
der Erfindung sind, wie weiter oben erwähnt, Verbindungen der Formel
I:
worin
A für =N-CR=CR-CR=,
=CR-N=CR-CR=, =CR-CR=N-CR= oder =CR-CR=CR-N= steht,
R
1 aus der Gruppe bestehend aus
– Wasserstoff,
– -C
1-20-Alkyl oder C
2-20-Alkenyl,
das gegebenenfalls durch einen oder mehrere Substituenten aus der
Gruppe bestehend aus
-Aryl,
-Heteroaryl,
-Heterocyclyl,
-O-C
1-20-Alkyl,
-O-(C
1-20-Alkyl)
0-1-aryl,
-O-(C
1-20-Alkyl)
0-1-heteroaryl,
-O-(C
1-20-Alkyl)
0-1-heterocyclyl,
-C
1-20-Alkoxycarbonyl,
-S(O)
0-2-C
1-20-Alkyl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-aryl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-heteroaryl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-heterocyclyl,
-N(R
3)
2,
-N
3,
Oxo,
-Halogen,
-NO
2,
-OH und
-SH
substituiert
ist, und
– -C
1-20-Alkyl-NR
3-Q-X-R
4 oder -C
2-20-Alkenyl-NR
3-Q-X-R
4, worin Q für -CO- oder -SO
2-
steht, X für
eine Bindung, -O- oder -NR
3- steht und R
4 für
Aryl, Heteroaryl, Heterocyclyl oder -C
1-20-Alkyl oder C
2-20-Alkenyl, das gegebenenfalls durch einen
oder mehrere Substituenten aus der Gruppe bestehend aus
-Aryl,
-Heteroaryl,
-Heterocyclyl,
-O-C
1-20-Alkyl,
-O-(C
1-20-Alkyl)
0-1-aryl,
-O-(C
1-20-Alkyl)
0-1-heteroaryl,
-O-(C
1-20-Alkyl)
0-1-heterocyclyl,
-C
1-20-Alkoxycarbonyl,
-S(O)
0-2-C
1-20-Alkyl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-aryl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-heteroaryl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-heterocyclyl,
-N(R
3)
2,
-NR
3-CO-O-C
1-20-Alkyl,
-N
3,
Oxo,
-Halogen,
-NO
2,
-OH und
-SH
substituiert
ist, oder für
worin Y -N- oder -CR- bedeutet,
steht,
ausgewählt
ist,
R
2 aus der Gruppe bestehend aus
-Wasserstoff,
-C
1-10-Alkyl,
-C
2-20-Alkenyl,
-Aryl,
-C
1-10-Alkyl-O-C
1-10-alkyl,
-C
1-10-Alkyl-O-C
2-10-alkenyl
und
-C
1-10-Alkyl oder C
2-10-Alkenyl,
das gegebenenfalls durch einen oder mehrere Substituenten aus der
Gruppe bestehend aus
-OH,
-Halogen,
-N(R
3)
2,
-CO-N(R
3)
2,
-CO-C
1-10-Alkyl,
-N
3,
-Aryl,
-Heteroaryl,
-Heterocyclyl,
-CO-Aryl
und
-CO-Heteroaryl
substituiert ist,
ausgewählt ist,
R
3 jeweils unabhängig voneinander aus der Gruppe
bestehend aus Wasserstoff und C
1-10-Alkyl
ausgewählt
ist und
R jeweils unabhängig
voneinander aus der Gruppe bestehend aus Wasserstoff, C
1-10-Alkyl,
C
1-10-Alkoxy, Halogen und Trifluormethyl
ausgewählt
ist,
oder ein pharmazeutisch unbedenkliches Salz davon.
-
Bevorzugte
Ausführungsformen
sind Verbindungen der Formel I, worin R
1 aus
der Gruppe bestehend aus C
1-6-Alkyl und C
1-6-Hydroalkyl ausgewählt ist; oder
worin R
1 aus der Gruppe bestehend aus n-Butyl, 2-Hydroxy-2-methylpropyl
und 2-Methylpropyl ausgewählt
ist; oder
worin R
2 aus der Gruppe bestehend
aus geradkettigem C
1-6-Alkyl und Alkoxyalkyl, worin der Alkoxyteil
und der Alkylteil jeweils unabhängig
voneinander 1 bis 4 Kohlenstoffatome enthalten, ausgewählt ist;
oder
worin R
2 aus der Gruppe bestehend
aus Methyl, n-Butyl, Benzyl, Ethoxymethyl und Methoxyethyl ausgewählt ist;
oder
worin R jeweils für
Wasserstoff steht; oder
worin R
1 für -C
1-20-Alkyl-NR
3-Q-X-R
4 steht; oder
worin R
1 für -C
1-20-Alkyl-NR
3-Q-X-R
4 steht und R
4 für
steht; oder
worin A
für =CH-CH=CH-N=
steht.
-
Gegenstand
der Erfindung sind auch Verbindungen der Formel II
worin
B für -NR-C(R)
2-C(R)
2-C(R)
2-, -C(R)
2-NR-C(R)
2-C(R)
2-, -C(R)
2-C(R)
2-NR-C(R)
2- oder -C(R)
2-C(R)
2-C(R)
2-NR- steht,
R
1 aus der Gruppe bestehend aus
– Wasserstoff,
– -C
1-20-Alkyl oder C
2-20-Alkenyl,
das gegebenenfalls durch einen oder mehrere Substituenten aus der
Gruppe bestehend aus
-Aryl,
-Heteroaryl,
-Heterocyclyl,
-O-C
1-20-Alkyl,
-O-(C
1-20-Alkyl)
0-1-aryl,
-O-(C
1-20-Alkyl)
0-1-heteroaryl,
-O-(C
1-20-Alkyl)
0-1-heterocyclyl,
-C
1-20-Alkoxycarbonyl,
-S(O)
0-2-C
1-20-Alkyl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-aryl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-heteroaryl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-heterocyclyl,
-N(R
3)
2,
-N
3,
Oxo,
-Halogen,
-NO
2,
-OH und
-SH
substituiert
ist, und
– -C
1-20-Alkyl-NR
3-Q-X-R
4 oder -C
2-20-Alkenyl-NR
3-Q-X-R
4, worin Q
für -CO-
oder -SO
2- steht, X für eine Bindung, -O- oder -NR
3-steht
und R
4 für
Aryl, Heteroaryl, Heterocyclyl oder -C
1-20-Alkyl
oder C
2-20-Alkenyl, das gegebenenfalls durch
einen oder mehrere Substituenten aus der Gruppe bestehend aus
-Aryl,
-Heteroaryl,
-Heterocyclyl,
-O-C
1-20-Alkyl,
-O-(C
1-20-Alkyl)
0-1-aryl,
-O-(C
1-20-Alkyl)
0-1-heteroaryl,
-O-(C
1-20-Alkyl)
0-1-heterocyclyl,
-C
1-20-Alkoxycarbonyl,
-S(O)
0-2-C
1-20-Alkyl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-aryl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-heteroaryl,
-S(O)
0-2-(C
1-20-Alkyl)
0-1-heterocyclyl,
-N(R
3)
2,
-NR
3-CO-O-C
1-20-Alkyl,
-N
3,
Oxo,
-Halogen,
-NO
2,
-OH und
-SH
substituiert
ist, oder für
worin Y -N- oder -CR- bedeutet,
steht, ausgewählt
ist,
R
2 aus der Gruppe bestehend aus
-Wasserstoff,
-C
1-10-Alkyl,
-C
2-20-Alkenyl,
-Aryl,
-C
1-10-Alkyl-O-C
1-10-alkyl,
-C
1-10-Alkyl-O-C
2-10-alkenyl
und
-C
1-10-Alkyl oder C
2-10-Alkenyl,
das gegebenenfalls durch einen oder mehrere Substituenten aus der
Gruppe bestehend aus
-OH,
-Halogen,
-N(R
3)
2,
-CO-N(R
3)
2,
-CO-C
1-10-Alkyl,
-N
3,
-Aryl,
-Heteroaryl,
-Heterocyclyl,
-CO-Aryl
und
-CO-Heteroaryl
substituiert ist,
ausgewählt ist,
R
3 jeweils unabhängig voneinander aus der Gruppe
bestehend aus Wasserstoff und C
1-10-Alkyl
ausgewählt
ist und
R jeweils unabhängig
voneinander aus der Gruppe bestehend aus Wasserstoff, C
1-10-Alkyl,
C
1-10-Alkoxy, Halogen und Trifluormethyl
ausgewählt
ist,
oder ein pharmazeutisch unbedenkliches Salz davon.
-
Bevorzugte
Ausführungsformen
sind Verbindungen der Formel II, worin R1 aus
der Gruppe bestehend C1-6-Alkyl und C1-6-Hydroxyalkyl ausgewählt ist,
oder R1 aus der Gruppe bestehend aus n-Butyl, 2-Hydroxy-2-methylpropyl und
2-Methylpropyl ausgewählt
ist, oder
worin R2 aus der Gruppe bestehend
aus Methyl, n-Butyl, Benzyl, Ethoxymethyl und Methoxyethyl ausgewählt ist,
oder
worin R jeweils für
Wasserstoff steht.
-
Gegenstand
der vorliegenden Erfindung sind auch
eine pharmazeutische Zusammensetzung,
die eine pharmazeutisch wirksame Menge einer Verbindung der Formel
I und einen pharmazeutisch unbedenklichen Träger enthält;
eine pharmazeutische
Zusammensetzung, die eine pharmzeutisch wirksame Menge einer Verbindung
der Formel II und einen pharmazeutisch unbedenklichen Träger enthält.
-
Im
Rahmen der vorliegenden Erfindung schließen die Begriffe "Alkyl" und "Alkenyl" und der Präfix "-alk" sowohl geradkettige
als auch verzweigtkettige Gruppen und cyclische Gruppen, d.h. Cycloalkyl
und Cycloalkenyl, ein. Diese cyclischen Gruppen können monocyclisch
oder polycyclisch sein und weisen vorzugsweise 3 bis 10 Ringkohlenstoffatome
auf. Beispiele für
cyclische Gruppen sind Cyclopropyl, Cyclopentyl, Cyclohexyl und
Adamantyl.
-
Im
Rahmen der vorliegenden Erfindung bezieht sich der Begriff "Aryl" auf carbocyclische
aromatische Ringe oder Ringsysteme, die unter Phenyl, Naphthyl,
Biphenyl, Fluorenyl und Indenyl ausgewählt sind. Der Begriff "Heteroaryl" bezieht sich auf
aromatische Ringe oder Ringsysteme, die mindestens ein Ringheteroatom (z.B.
O, S, N) enthalten und unter Furyl, Thienyl, Pyridyl, Chinolinyl,
Tetrazolyl und Imidazolyl ausgewählt
sind.
-
"Heterocyclyl" bezieht sich auf
nichtaromatische Ringe oder Ringsysteme, die mindestens ein Ringheteroatom
(z.B. O, S, N) enthalten und unter Pyrrolidinyl, Tetrahydrofuranyl,
Morpholinyl, Thiazolidinyl und Imidazolidinyl ausgewählt sind.
-
Die
Aryl-, Heteroaryl- und Heterocyclylgruppen können gegebenenfalls durch einen
oder mehrere Substituenten aus der Gruppe bestehend aus C1-20-Alkyl, Hydroxy, Halogen, N(R3)2, NO2,
C1-20-Alkoxy, C1-20-Alkylthio,
Trihalogenmethyl, C1-20-Acyl, Arylcarbonyl,
Heteroarylcarbonyl, (C1-10-Alkyl)0-1-aryl, (C1-20-Alkyl)0-1-heteroaryl, Nitril, C1-20-Alkoxycarbonyl,
Oxo, Arylalkyl, worin die Alkylgruppe 1 bis 10 Kohlenstoffatome
aufweist, und Heteroarylalkyl, worin die Alkylgruppe 1 bis 10 Kohlenstoffatome
aufweist, substituiert sein.
-
Die
Erfindung schließt
die hier beschriebenen Verbindungen in allen ihren pharmazeutisch
unbedenklichen Formen einschließlich
von Isomeren, wie Diastereomeren und Enantiomeren, Salzen, Solvaten,
Polymorphen und dergleichen ein.
-
Herstellung
der Verbindungen
-
Verbindungen
der Formel I und II, worin A für
=N-CR=CR-CR= steht
oder B für
-NR-C(R)2-C (R)2-C(R)2- steht und R, R1 und
R2 die oben angegebene Bedeutung besitzen,
können
gemäß Reaktionsschema
I hergestellt werden:
-
-
2-Aminonicotinsäuren der
Formel III sind in großer
Zahl bekannt (siehe beispielsweise
US
3,917,624 ). Die Verbindung, in der R für Wasserstoff steht, ist im
Handel erhältlich.
In Schritt (1) von Reaktionsschema I wird eine 2-Aminonicotinsäure der
Formel III durch Erhitzen mit Essigsäureanhydrid zu einem 2-Methyl-4H-pyrido[2,3-d][1,3]oxazin-4-on
der Formel IV umgesetzt. Die Verbindung der Formel IV, in der R
für Wasserstoff steht,
ist bekannt, und ihre Herstellung wurde in der US-PS 3,314,941 (Littell),
auf die hiermit ausdrücklich
Bezug genommen wird, beschrieben.
-
In
Schritt (2) von Reaktionsschema I wird eine Verbindung der Formel
IV in einem geeigneten Lösungsmittel,
wie Essigsäure,
mit Natriumazid zu einer Tetrazolylnicotinsäure der Formel V umgesetzt.
Die Reaktion kann zweckmäßigerweise
bei Umgebungsbedingungen durchgeführt werden.
-
In
Schritt (3) von Reaktionsschema I wird eine Säure der Formel V zu einer Verbindung
der Formel VI verestert. Die Veresterung kann nach herkömmlichen
Verfahren erfolgen. So kann man beispielsweise die Säure in Aceton
unter Verwendung von Kaliumcarbonat und Ethyliodid verestern.
-
In
Schritt (4) von Reaktionsschema I wird eine Verbindung der Formel
VI zu einem Tetrazolo[1,5-a][1,8] naphthyridin-5-ol der Formel VII
cyclisiert. Hierzu kann man die Verbindung der Formel VI bei Umgebungsbedingungen
mit einem Alkoxid in einem geeigneten Lösungsmittel, z.B. Kaliumethoxid
in N,N-Dimethylformamid,
umsetzen.
-
In
Schritt (5) von Reaktionsschema I wird eine Verbindung der Formel
VII unter Verwendung eines geeigneten Nitrierungsmittels, wie Salpetersäure, zu
einem 4-Nitrotetrazolo[1,5-a][1,8]naphthyridin-5-ol der Formel VIII
nitriert.
-
In
Schritt (6) von Reaktionsschema I wird eine Verbindung der Formel
VIII in ein Triflat der Formel IX umgewandelt. Hierbei geht man
vorzugsweise so vor, daß man
eine Verbindung der Formel VIII in einem geeigneten Lösungsmittel,
wie Dichlormethan, mit einer Base, vorzugsweise einem tertiären Amin
wie Triethylamin, vereinigt und dann Trifluormethansulfonsäureanhydrid
zugibt. Die Zugabe erfolgt vorzugsweise kontrolliert, z.B. durch
Zutropfen bei verminderter Temperatur, wie beispielsweise bei etwa
0°C. Das
Produkt kann nach herkömmlichen
Methoden isoliert oder ohne Isolierung wie nachstehend in Verbindung
mit Schritt (7) beschrieben weitergeführt werden.
-
In
Schritt (7) von Reaktionsschema I wird eine Verbindung der Formel
IX mit einem Amin der Formel R1NH2, worin R1 die oben
angegebene Bedeutung besitzt, zu einem 4-Nitrotetrazolo[1,5-a][1,8]naphthyridin-5-amin der Formel X
umgesetzt. Hierzu kann man das Amin zu der in Schritt (6) angefallenen
Reaktionsmischung geben. Man kann aber auch das Amin zu einer Lösung der
Formel IX und eines tertiären
Amins in einem geeigneten Lösungsmittel,
wie Dichlormethan, geben.
-
In
Schritt (8) von Reaktionsschema I wird eine Verbindung der Formel
X zu einem Tetrazolo[1,5-a][1,8]naphthyridin-4,5-diamin
der Formel XI reduziert. Hierzu verwendet man vorzugsweise einen
herkömmlichen
heterogenen Hydrierkatalysator, wie Platin auf Kohle oder Palladium
auf Kohle. Die Umsetzung kann zweckmäßigerweise in einer Parr-Apparatur
in einem geeigneten Lösungsmittel,
wie Ethanol, durchgeführt
werden.
-
In
Schritt (9) von Reaktionsschema I wird eine Verbindung der Formel
XI mit einer Carbonsäure
oder einem Äquivalent
davon zu einem 1H-Tetrazolo[1,5-a]imidazo[4,5-c][1,8]
naphthyridin der Formel XII umge setzt. Geeignete Äquivalente
von Carbonsäuren
sind u.a. Säurehalogenide,
Orthoester und Alkansäure-1,1-dialkoxyalkylester.
Die Carbonsäure
bzw. das Äquivalent
davon wird so gewählt,
daß sie
den gewünschten
Substituenten R2 in einer Verbindung der
Formel XII liefert. So liefert beispielsweise Essigsäurediethoxymethylester
eine Verbindung, in der R2 für Wasserstoff
steht, und Valerylchlorid eine Verbindung, in der R2 für Butyl
steht. Die Umsetzung kann ohne Lösungsmittel
in einer Carbonsäure,
wie Essigsäure,
oder in einem inerten Lösungsmittel
in Gegenwart einer Carbonsäure
durchgeführt
werden. Bei der Umsetzung wird so stark erhitzt, daß jeglicher
als Reaktionsnebenprodukt anfallende Alkohol oder jegliches als
Reaktionsnebenprodukt anfallendes Wasser ausgetrieben wird.
-
In
Schritt (10) von Reaktionsschema I wird eine Verbindung der Formel
XII mit Triphenylphosphin zu einem N-Triphenylphosphinyl-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin
der Formel XIII umgesetzt. Hierzu kann man eine Verbindung der Formel
XII in einem geeigneten Lösungsmittel,
wie 1,2-Dichlorbenzol, mit Triphenylphosphin vereinigen und erhitzen.
-
In
Schritt (11) von Reaktionsschema I wird eine Verbindung der Formel
XIII zu eine 1H-Imidazom[4,5-c][1,8]naphthyridin-4-amin
der Formel XIV, bei der es sich um eine Untergruppe von Formel I
handelt, hydrolysiert. Die Hydrolyse kann nach herkömmlichen
Verfahren durchgeführt
werden, wie durch Erhitzen in einem niederen Alkanol in Gegenwart
einer Säure.
Das Produkt oder ein pharmazeutisch unbedenkliches Salz davon kann
nach herkömmlichen
Verfahren isoliert werden.
-
In
Schritt (12) von Reaktionsschema I wird eine Verbindung der Formel
XIV zu einem 6,7,8,9-Tetrahydro-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin
der Formel XV, bei der es sich um eine Untergruppe der Formel II
handelt, reduziert. Hierzu suspendiert oder löst man eine Verbindung der
Formel XIV in Trifluoressigsäure, gibt
eine katalytisch wirksame Menge Platin(IV)-oxid zu und setzt die
Mischung dann unter Wasserstoffdruck. Die Reaktion kann zweckmäßigerweise
in einer Parr-Apparatur durchgeführt
werden. Das Produkt oder ein pharmazeutisch unbedenkliches Salz
davon kann nach herkömmlichen
Verfahren isoliert werden.
-
Alternativ
dazu kann man ein 6,7,8,9-Tetrahydro-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin
der Formel XV, durch Reduktion einer Verbindung der Formel XII herstellen,
wie es in Schritt (13) von Reaktionsschema I dargestellt ist. Hierzu
suspendiert oder löst
man eine Verbindung der Formel XII in Trifluoressigsäure, setzt
eine katalytisch wirksame Menge Platin(IV)-oxid zu und setzt die
Mischung dann unter Wasserstoffdruck. Die Umsetzung kann zweckmäßigerweise
in einer Parr-Apparatur
durchgeführt
werden. Wie oben kann das Produkt oder ein pharmazeutisch unbedenkliches
Salz davon nach herkömmlichen
Verfahren isoliert werden.
-
Verbindungen
der Formeln I und II, worin A für
=CR-N=CR-CR= steht
oder B für -C(R)2-NR-C(R)2-C(R)2- steht und R, R1 und
R2 die oben angegebene Bedeutung besitzen,
können
gemäß Reaktionsschema
II hergestellt werden.
-
-
-
In
Schritt (1) von Reaktionsschema II wird eine 3-Aminoisonicotinsäure der Formel XVI durch Erhitzen mit
Essigsäureanhydrid
zu einem 2-Methyl-4H-pyrido[3,4-d][1,3]oxazin-4-on
der Formel XVII umgesetzt. Die Verbindung der Formel XVII, worin
R für Wasserstoff
steht, ist bekannt, und ihre Herstellung wurde in der oben zitierten
Druckschrift von Littell beschrieben.
-
In
Schritt (2) von Reaktionsschema II wird eine Verbindung der Formel
XVII in einem geeigneten Lösungsmittel,
wie Essigsäure,
mit Natriumazid zu einer Tetrazolylisonicotinsäure der Formel XVIII umgesetzt. Die
Umsetzung kann zweckmäßigerweise
bei Umgebungsbedingungen durchgeführt werden.
-
In
Schritt (3) von Reaktionsschema II wird eine Säure der Formel XVIII zu einer
Verbindung der Formel XIX verestert. Die Veresterung kann nach herkömmlichen
Verfahren erfolgen. So kann man beispielsweise die Säure in Aceton
unter Verwendung von Kaliumcarbonat und Ethyliodid oder durch Umsetzung
mit Dimethylformamiddiethylacetal in einem geeigneten Lösungsmittel,
wie Dichlormethan, verestern.
-
In
Schritt (4) von Reaktionsschema II wird eine Verbindung der Formel
XIX zu einem Tetrazolo[1,5-a][1,7]naphthyridin-5-ol
der Formel XX cyclisiert. Hierzu kann man eine Verbindung der Formel
XIX bei Umgebungsbedingungen mit einem Alkoxid in einem geeigneten
Lösungsmittel,
z.B. Kaliumethoxid in N,N-Dimethylformamid,
umsetzen.
-
In
Schritt (5) von Reaktionsschema II wird eine Verbindung der Formel
XX mit einem geeigneten Chlorierungsmittel, wie Thionylchlorid,
Oxalylchlorid, Phosphorpentachlorid oder vorzugsweise Phosphoroxidchlorid,
zu einem 5-Chlortetrazolo[1,5-a][1,7]naphthyridin der Formel XXI
chloriert. Die Umsetzung kann in einem inerten Lösungsmittel oder gegebenenfalls
in unverdünntem
Chlorierungsmittel durchgeführt
werden. Vorzugsweise wird die Umsetzung in unverdünntem Phosphoroxidchlorid
unter Erhitzen auf etwa 90°C
durchgeführt.
-
In
Schritt (6) von Reaktionsschema II wird eine Verbindung der Formel
XXI mit einem Amin der Formel R1NH2, worin R1 die oben
angegebene Bedeutung besitzt, zu einem Tetrazolo[1,5-a][1,7]naphthyridin-5-amin der Formel
XXII umgesetzt. Die Umsetzung kann durch Erhitzen mit einem Überschuß des Amins
durchgeführt werden.
-
In
Schritt (7) von Reaktionsschema II wird eine Verbindung der Formel
XXII mit einem geeigneten Nitrierungsmittel, wie Salpetersäure, zu
einem 4-Nitrotetrazolo[1,5-a][1,7]naphthyridin-5-amin
der Formel XXIII nitriert. Die Umsetzung wird vorzugsweise in Essigsäure unter
gelindem Erhitzen mit einem Überschuß von Salpetersäure durchgeführt.
-
In
Schritt (8) von Reaktionsschema II wird eine Verbindung der Formel
XXIII zu einem Tetrazolo[1,5-a][1,7]naphthyridin-4,5-diamin
der Formel XXIV reduziert. Die Umsetzung wird vorzugsweise mit einem Überschuß von Natriumhydrogensulfid
in einem geeigneten Lösungsmittel,
wie Essigsäure,
durchgeführt.
-
In
Schritt (9) von Reaktionsschema II wird eine Verbindung der Formel
XXIV mit einer Carbonsäure oder
einem Äquivalent
davon zu einem 1H-Tetrazolo[1,5-a]imidazo[4,5-c][1,7]naphthyridin
der Formel XXV umgesetzt. Geeignete Äquivalente von Carbonsäuren sind
u.a. Säurehalogenide,
Orthoester und Alkansäure-1,1-dialkoxyalkylester.
Die Carbonsäure
oder das Äquivalent
davon wird so gewählt,
daß sie
den gewünschten
Substituenten R2 in einer Verbindung der
Formel XXV liefert. So liefert beispielsweise Essigsäurediethoxymethylester
eine Verbindung, in der R2 für Wasserstoff
steht, und Valerylchlorid eine Verbindung, in der R2 für Butyl
steht. Die Umsetzung kann ohne Lösungsmittel
in einer Carbonsäure,
wie Essigsäure,
oder in einem inerten Lösungsmittel
in Gegenwart einer Carbonsäure
durchgeführt
werden. Bei der Umsetzung wird so stark erhitzt, daß jeglicher
als Reaktionsnebenprodukt anfallende Alkohol oder jegliches als
Reaktionsnebenprodukt anfallendes Wasser ausgetrieben wird.
-
In
Schritt (10) von Reaktionsschema II wird eine Verbindung der Formel
XXV mit Triphenylphosphin zu einem N-Triphenylphosphinyl-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
der Formel XXVI umgesetzt. Hierzu kann man eine Verbindung der Formel
XXV in einem geeigneten Lösungsmittel,
wie 1,2-Dichlorbenzol, mit Triphenylphosphin vereinigen und erhitzen.
-
In
Schritt (11) von Reaktionsschema II wird eine Verbindung der Formel
XXVI zu einem 1H-Imidazo[4,5-c][1,7]naphthyridin-4-amin
der Formel XXVII, bei der es sich um eine Untergruppe der Formel
I handelt, hydrolisiert. Die Hydrolyse kann nach herkömmlichen
Verfahren durchgeführt
werden, wie durch Erhitzen in einem niederen Alkanol in Gegenwart
einer Säure.
Das Produkt oder ein pharmazeutisch unbedenkliches Salz davon kann
nach herkömmlichen
Verfahren isoliert werden.
-
In
Schritt (12) von Reaktionsschema II wird eine Verbindung der Formel
XXVII zu einem 6,7,8,9-Tetrahydro-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
der Formel XXVIII, bei der es sich um eine Untergruppe der Formel
II handelt, reduziert. Hierzu suspendiert oder löst man eine Verbindung der
Formel XXVII in Trifluoressigsäure,
gibt eine katalytisch wirksame Menge Platin(IV)-oxid zu und setzt
die Mischung dann unter Wasserstoffdruck. Die Umsetzung kann zweckmäßigerweise
in einer Parr-Apparatur durchgeführt
werden. Das Produkt oder ein pharmazeutisch unbedenkliches Salz
davon kann nach herkömmlichen
Verfahren isoliert werden.
-
Alternativ
dazu kann man ein 6,7,8,9-Tetrahydro-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
der Formel XXVIII durch Reduktion einer Verbindung der Formel XXV
herstellen, wie in Schritt (13) von Reaktionsschema II dargestellt.
Hierzu suspendiert oder löst
man eine Verbindung der Formel XXV in Trifluoressigsäure, gibt
eine katalytisch wirksame Menge Platin(IV)-oxid zu und setzt die
Mischung dann unter Wasserstoffdruck. Die Umsetzung kann zweckmäßigerweise
in einer Parr-Apparatur
durchgeführt
werden. Das Produkt oder ein pharmazeutisch unbedenkliches Salz
davon kann nach herkömmlichen
Verfahren isoliert werden.
-
Verbindungen
der Formeln I und II, worin A für
=CR-CR=CR-N= steht
oder B für -C(R)2-C(R)2-C(R)2-NR- steht und R, R1 und
R2 die oben angegebene Bedeutung besitzen,
können
gemäß Reaktionsschema
III hergestellt werden.
-
-
In
Schritt (1) von Reaktionsschema III wird ein 3- Nitro[1,5]naphthyridin-4-ol der Formel
XXIX mit einem geeigneten Chlorierungsmittel, wie Phosphoroxidchlorid,
zu einem 4-Chlor-3-nitro[1,5]naphthyridin der Formel XXX chloriert.
Hierzu kann man eine Verbindung der Formel XXIX in einem geeigneten
Lösungsmittel,
wie N,N-Dimethylformamid,
unter gelindem Erhitzen (~55°C)
mit Phosphoroxidchlorid umsetzen. Die Verbindung kann nach herkömmlichen
Verfahren isoliert oder ohne Isolierung wie unten in Verbindung
mit Schritt (2) beschrieben weitergeführt werden. Die Verbindung
der Formel XXIX, in der R für
Wasserstoff steht, ist bekannt, und ihre Herstellung wurde in Hart,
Journal of the Chemical Society, S. 212-214 (1956), beschrieben.
-
In
Schritt (2) von Reaktionsschema III wird ein 4-Chlor-3-nitro[1,5]naphthyridin der Formel
XXX mit einem Amin der Formel R1NH2, worin R1 die oben
angegebene Bedeutung besitzt, zu einem 3-Nitro[1,5]naphthyridin-4-amin der Formel XXXI
umgesetzt. Hierzu kann man die in Schritt (1) angefallene Reaktionsmischung mit
Wasser gefolgt von einem Überschuß an Amin
versetzen und dann auf einem Dampfbad erhitzen. Man kann aber auch
eine Lösung
einer Verbindung der Formel XXX in einem geeigneten Lösungsmittel,
wie Dichlormethan, mit einem Überschuß an Amin
versetzen und gegebenenfalls erhitzen. Die Verbindung der Formel
XXXI, in der R1 für Wasserstoff steht, ist bekannt,
und ihre Herstellung wurde in Wozniak et al., J.R. Neth. Chem. Soc.
102 (12), S. 511-513 (1983), beschrieben.
-
In
Schritt (3) von Reaktionsschema III wird ein 3-Nitro[1,5]naphthyridin-4-amin der Formel
XXXI zu einem [1,5]Naphthyridin-3,4-diamin der Formel XXXII reduziert.
Vorzugsweise wird die Reduktion mit einem herkömmlichen heterogenen Hydrierkatalysator,
wie Platin auf Kohle oder Palladium auf Kohle, durchgeführt. Die Umsetzung
kann zweckmäßigerweise
in einer Parr-Apparatur in einem geeigneten Lösungsmittel, wie Essigsäureethylester,
durchgeführt
werden.
-
In
Schritt (4) von Reaktionsschema III wird eine Verbindung der Formel
XXXII mit einer Carbonsäure oder
einem Äquivalent
davon zu einem 1H-Imidazo[4,5-c][1,5]naphthyridin
der Formel XXXIII umgesetzt. Geeignete Äquivalente von Carbonsäuren sind
u.a. Säurehalogenide,
Orthoester und Alkansäure-1,1-dialkoxyalkylester.
Die Carbonsäure
oder das Äquivalent
davon wird so gewählt.
Daß sie
den gewünschten
Substituenten R2 in einer Verbindung der
Formel XXXIII liefert. So liefert beispielsweise Essigsäurediethoxymethylester eine
Verbindung, in der R2 für Wasserstoff steht, und Orthovaleriansäuretrimethylester
eine Verbindung, in der R2 für Butyl
steht. Die Umsetzung kann ohne Lösungsmittel
in einer Carbonsäure,
wie Essigsäure,
oder in einem inerten Lösungsmittel
in Gegenwart einer Säure
durchgeführt
werden. Bei der Umsetzung wird so stark erhitzt, daß jeglicher
als Reaktionsnebenprodukt anfallender Alkohol oder jegliches als
Reaktionsnebenprodukt anfallende Wasser ausgetrieben wird.
-
Alternativ
dazu kann man Schritt (4) durchführen,
indem man (i) eine Verbindung der Formel XXXII mit einem Acylierungsmittel
umsetzt und dann (ii) das Produkt cyclisiert. In Teil (i) wird eine
Verbindung der Formel XXXII mit einem Säurehalogenid der Formel R2C(O)X, worin R2 die
oben angegebene Bedeutung besitzt und X für Chlor oder Brom steht, umgesetzt.
Die Umsetzung kann durch kontrollierte Zugabe (z.B. Zutropfen) des Acylhalogenids
zu einer Lösung
einer Verbindung der Formel XXXII in einem geeigneten Lösungsmittel,
wie Dichlormethan, bei verminderter Temperatur (z.B. 0°C) durchgeführt werden.
Das anfallende Amidzwischenprodukt kann durch Entfernung des Lösungsmittels
isoliert werden. In Teil (ii) wird das Produkt aus Teil (i) durch Umsetzung
mit methanolischem Ammoniak bei erhöhter Temperatur (z.B. 150°C) und erhöhtem Druck
cyclisiert.
-
In
Schritt (5) von Reaktionsschema III wird eine Verbindung der Formel
XXXIII mit einem herkömmlichen
Oxidationsmittel, das zur Bildung von N-Oxiden befähigt ist,
zu einem 1H-Imidazo[4,5-c][1,5]naphthyridin-5N-oxid der Formel XXXIV oxidiert. Vorzugsweise
setzt man eine Lösung
einer Verbindung der Formel XXXIII in Chloroform bei Umgebungsbedingungen
mit 3-Chlorperoxybenzoesäure um.
-
In
Schritt (6) von Reaktionsschema III wird eine Verbindung der Formel
XXXIV zu einem 1H-Imidazo[4,5-c][1,5]naphthyridin-4-amin
der Formel XXXV, bei der es sich um eine Untergruppe der Formel
I handelt, aminiert. Hierbei wird (i) eine Verbindung der Formel
XXXIV mit einem Acylierungsmittel umgesetzt und dann (ii) das Produkt
mit einem Aminierungsmittel umgesetzt. In Teil (i) von Schritt (6)
wird ein N-Oxid mit einem Acylierungsmittel umgesetzt. Geeignete
Acylierungsmittel sind u.a. Alkyl- oder Arylsulfonylchloride (z.B.
Benzolsulfonylchlorid, Methansulfonylchlorid, p-Toluolsulfonylchlorid).
Bevorzugt sind Arylsulfonylchloride. Ganz besonders bevorzugt ist
p-Toluolsulfonylchlorid. In Teil (ii) von Schritt (6) wird das Produkt
aus Teil (i) mit einem Überschuß eines
Aminierungsmittels umgesetzt. Geeignete Aminierungsmittel sind u.a.
Ammoniak (z.B. in Form von Ammoniumhydroxid) und Ammoniumsalze (z.B.
Ammoniumcarbonat, Ammoniumhydrogencarbonat, Ammoniumphosphat). Bevorzugt
ist Ammoniumhydroxid. Bei der Umsetzung geht man vorzugsweise so vor,
daß man
das N-Oxid der Formel XXXIV in einem inerten Lösungsmittel, wie Dichlormethan
löst, die
Lösung
mit dem Aminierungsmittel versetzt und dann das Acylierungsmittel
zugibt. Bevorzugt wird bei der Zugabe des Acylierungsmittels auf
etwa 0°C
bis etwa 5°C
abgekühlt.
Das Produkt oder ein pharmazeutisch unbedenkliches Salz davon kann
nach herkömmlichen
Verfahren isoliert werden.
-
Alternativ
dazu kann man Schritt (6) durchführen,
indem man (i) eine Verbindung der Formel XXXIV mit einem Isocyanat
umsetzt und dann (ii) das Produkt hydrolysiert. In Teil (i) wird
das N-Oxid mit einem Isocyanat, indem die Isocyanatogruppe an eine
Carbonylgruppe gebunden ist, umgesetzt. Bevorzugte Isocyanate sind
u.a. Trichloracetylisocyanat und Aroylisocyanate, wie BenzoylIsocyanat.
Die Umsetzung des Isocyanats mit dem N-Oxid wird unter weitgehend
wasserfreien Bedingungen durchgeführt, indem man eine Lösung des N-Oxids
in einem inerten Lösungsmittel,
wie Dichlormethan, mit dem Isocyanat versetzt. Das anfallende Produkt
kann durch Entfernung des Lösungsmittels
isoliert werden. In Teil (ii) wird das Produkt aus Teil (i) hydrolysiert.
Die Umsetzung kann nach herkömmlichen
Verfahren durchgeführt
werden, wie durch Erhitzen in Gegenwart von Wasser oder einem niederen
Alkanol, gegebenenfalls in Gegenwart eines Katalysators, wie eines Alkalihydroxids
oder niederen Alkoxids.
-
In
Schritt (7) von Reaktionsschema III wird eine Verbindung der Formel
XXXV zu einem 6,7,8,9-Tetrahydro-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
der Formel XXXVI, bei der es sich um eine Untergruppe der Formel
II handelt, reduziert. Hierzu suspendiert oder löst man eine Verbindung der
Formel XXXV in Trifluoressigsäure,
gibt eine katalytisch wirksame Menge Platin(IV)-oxid zu und setzt
die Mischung dann unter Wasserstoffdruck. Die Umsetzung kann zweckmäßigerweise
in einer Parr-Apparatur
durchgeführt
werden. Das Produkt oder ein pharmazeutisch unbedenkliches Salz
davon kann nach herkömmlichen
Verfahren isoliert werden.
-
Bestimmte
in Verbindung mit R1 und R2 aufgeführte funktionelle
Gruppen können
mit einigen der Reagenzien der Reaktionsschemata I, II und III inkompatibel
sein. Verbindungen mit derartigen funktionellen Gruppen können vom
Fachmann nach gut bekannten Verfahren zum Schutz und zur Manipulierung
funktioneller Gruppen hergestellt werden. So kann man beispielsweise
Amingruppen gegebenenfalls durch Derivatisierung mit Di-tert.-butyldicarbonat
schützen.
-
Einige
Verbindungen der Formel I oder Formel II mit bestimmten funktionellen
Gruppen können
leicht aus anderen Verbindungen der Formel I oder Formel II hergestellt
werden. So kann man beispielsweise Verbindungen, in denen der Substituent
R1 eine Amidgruppe enthält, zweckmäßigerweise durch Umsetzung
eines Säurechlorids
mit einer Verbindung der Formel I oder Formel II, worin der Substituent
R1 ein primäres Amin enthält, herstellen.
Ganz analog kann man Verbindungen, in denen der Substituent R1 eine Harnstoffgruppe enthält, durch
Umsetzung eines Isocyanats mit einer Verbindung der Formel I oder
Formel II, worin der Substituent R1 ein
primäres
Amin enthält,
herstellen. Ferner kann man Verbindungen, in denen der Substituent
R1 eine Carbamatgruppe enthält, durch
Umsetzung eines Chlorameisensäureesters
mit einer Verbindung der Formel I oder Formel II, worin der Substituent
R1 ein primäres Amin enthält, herstellen.
-
Bestimmte
zur Verwendung bei der Herstellung von Verbindungen der Formel I
und Formel II geeignete Zwischenverbindungen sind noch nicht vorbeschrieben
worden. Gegenstand der Erfindung sind daher auch zur Verwendung
bei der Herstellung von Verbindungen der Formel I und Formel II
geeignete Zwischenverbindungen. Die Strukturformeln dieser neuen
Zwischenprodukte sind nachstehend aufgeführt. Diese Verbindungen haben
die folgenden Strukturformeln: Zwischenverbindung
1
worin R
1, R
2 und
A die oben für
Verbindungen der Formel I und Formel II angegebene Bedeutung besitzen. Zwischenverbindung
2
worin R, R
1 und R
2 die oben für Verbindungen der Formel I
und Formel II angegebene Bedeutung besitzen. Zwischenverbindung
3
worin R, R
1 und R
2 die oben für Verbindungen der Formel I
und Formel II angegebene Bedeutung besitzen. Zwischenverbindung
4
worin R
7 für OH, Halogen
oder NHR
1 steht (und A und R
1 die
oben für
Verbindungen der Formel I angegebene Bedeutung besitzen) und R
8 für
H, NO
2 oder NH
2 steht. Zwischenverbindung
5
worin A die oben für Verbindungen der Formel I
angegebene Bedeutung besitzt und R
9 für H oder
C
1-10-Alkyl steht. Zwischenverbindung
6
worin R und R
1 die oben
für Verbindungen
der Formel I und Formel II angegebene Bedeutung besitzen, mit der Maßgabe, daß R
1 nicht für
Wasserstoff steht und R
10 für NO
2 oder NH
2 steht.
-
Pharmazeutische
Zusammensetzungen und biologische Wirkung
-
Erfindungsgemäße pharmazeutische
Zusammensetzungen enthalten eine therapeutisch wirksame Menge einer
Verbindung der Formel I oder Formel II gemäß obiger Definition in Kombination
mit einem pharmzeutisch unbedenklichen Träger. Im Rahmen der vorliegenden
Erfindung versteht man unter dem Begriff "eine therapeutisch wirksame Menge" eine Menge der Verbindung,
die zur Hervorrufung einer therapeutischen Wirkung, wie Cytokin-Induktion
oder Antiviruswirkung, ausreicht. Die genaue Menge der in einer
erfindungsgemäßen pharmazeutischen
Zusammensetzung verwendeten aktiven Verbindung variiert zwar mit
dem Fachmann bekannten Faktoren, wie der physikalischen und chemischen
Beschaffenheit der Verbindung sowie der Beschaffenheit des Trägers und
dem vorgesehenen Dosierungsschema, jedoch ist vorgesehen, daß die erfindugngsgemäßen Verbindungen
eine zur Bereitstellung einer Dosis von etwa 100 ng/kg bis etwa
50 mg/kg und vorzugsweise von etwa 10 μg/kg bis etwa 5 mg/kg der Verbindung
an den Patienten ausreichende Wirkstoffmenge enthalten. Es kommen
alle herkömmlichen
Dosierungsformen in Betracht, wie Tabletten, Pastillen, parenterale
Formulierungen, Sirupe, Cremes, Salben, Aerosolformulierungen, Transdermalpflaster,
Transmucosalpflaster und so weiter.
-
Es
hat sich gezeigt, daß die
erfindungsgemäßen Verbindungen
bei Versuchen, die gemäß der nachstehend
aufgeführten
Testmethode durchgeführt
wurden, die Produktion bestimmter Cytokine induziert. Diese Fähigkeit
deutet darauf hin, daß die
Verbindungen zur Verwendung als die Immunantwort modifizierende
Mittel, die die Immunantwort auf eine Reihe von verschiedenen Wegen
modulieren können,
und somit zur Behandlung verschiedener Erkrankungen geeignet sind.
-
Zu
den durch die Verabreichung von erfindungsgemäßen Verbindungen induzierten
Cytokinen gehören
im allgemeinen Interferon (IFN) und Tumornekrosefaktor (TNF) sowie
bestimmte Interleukine (IL). Insbesondere induzieren die Verbindungen
IFN-α, TNF-α, IL-1, 6,
10 und 12 und verschiedene andere Cytokine. Unter anderem inhibieren
Cytokine die Produktion von Viren und das Wachstum von Tumorzellen,
sodaß die
Verbindungen zur Verwendung bei der Behandlung von Tumoren und Virenerkrankungen
geeignet sind.
-
Neben
der Fähigkeit
zur Induktion der Produktion von Cytokinen beeinflussen die Verbindungen
auch andere Aspekte der angeborenen Immunantwort. So kann beispielsweise
die Aktivität
natürlicher
Killerzellen stimuliert werden, was möglicherweise auf die Cytokin-Induktion zurückzuführen ist.
Die Verbindungen können auch
Makrophagen aktivieren, was wiederum die Sekretion von Stickstoffmonoxid
und die Produktion zusätzlicher
Cytokine stimuliert. Des weiteren können die Verbindungen die Proliferation
und Differenzierung von B-Lymphozyten bewirken.
-
Erfindungsgemäße Verbindungen
haben auch eine Wirkung auf die erworbene Immunantwort. Beispielsweise
wird, obwohl nicht angenommen wird, daß eine direkte Wirkung auf
T-Zellen oder eine direkte Induktion von T-Zell-Cytokinen vorliegt, bei Verabreichung
der Verbindungen die Produktion des T-Helfer-Typ-1-Cytokins (Th1-Cytokins) IFN-γ indirekt
induziert und die Produktion des Th2-Cytokins IL-5 inhibiert. Aufgrund
dieser Wirkung eignen sich die Verbindungen zur Verwendung bei der
Behandlung von Erkrankungen, bei der die Heraufregulierung der Th1-Antwort
und/oder die Herabregulierung der Th2-Antwort erwünscht ist.
Angesichts der Fähigkeit
von Verbindungen der Formel I und Formel II, die T-Helfer-Typ-2-Immunantwort zu
inhibieren, wird erwartet, daß die
Verbindungen für
die Verwendung bei der Behandlung von Atopie, z.B. atopischer Dermatitis,
Asthma, Allergie, allergischer Rhinitis; als Impfhilfsstoff für zellvermittelte
Immunität
und möglicherweise
als Behandlung für
rezividierende Pilzerkrankungen und Chlamydia geeignet sind.
-
Aufgrund
ihrer die Immunantwort modifizierenden Wirkungen sind die Verbindungen
zur Verwendung bei der Behandlung verschiedenster Leiden geeignet.
Aufgrund ihrer Fähigkeit
zur Induktion von Cytokinen wie IFN-α und TNF-α eignen sich die Verbindungen
besonders gut zur Verwendung bei der Behandlung von Viruserkrankungen
und Tumoren. Diese immunmodulierende Wirkung legt nahe, daß erfindungsgemäße Verbindungen
zur Verwendung bei der Behandlung von Erkrankungen geeignet sind,
wie u.a. Viruserkrankungen, z.B. Feigwarzen, gemeinen Warzen, Sohlenwarzen,
Hepatitis B, Hepatitis C, Herpes Simplex Typ I und Typ II, Molluscum
Contagiosum, HIV, CMV, VZV, zervikaler intraepithelialer Neoplasie,
Humanpapillomavirus und damit einhergehende Neoplasien; Pilzerkrankungen,
z.B. Candida-, Aspergillus-, Cryptokokkenmeningitis; neoplastische
Erkrankungen, z.B. Basalzellkarzinom, Haarzellenleukämie, Kaposi-Sarkom, Nierenzellenkarzinom,
Plattenepitelkarzinom, myeloischer Leukämie, multiples Myelom, Melanom,
non-Hodgkin-Lymphom,
kutanem T-Zell-Lymphom und anderen Krebsarten; parasitischen Erkrankungen,
z.B. Pneumocystis carnii, Cryptosporidiose, Histoplasmose, Toxoplasmose,
Trypanosomeninfektion, Leishmaniase; bakterielle Infektionen, z.B.
Tuberkulose, Mycobakterium avium. Weitere Erkrankungen oder Leiden,
die mit den erfindungsgemäßen Verbindungen
behandelt werden können,
sind u.a. Ekzem, Eosinophilie, essentielle Thrombozythämie, Lepra, multiple
Sklerose, Ommen-Syndrom, rheumatoide Arthritis, systemischer Lupus
erythematodes, diskoider Lupus, Bowen-Krankheit und bowenoide Papulose.
-
Gegenstand
der Erfindung ist demgemäß ein Verfahren
zur Induktion der Cytokin-Biosynthese in einem Tier, bei dem man
dem Tier eine wirksame Menge einer Verbindung der Formel I oder
Formel II verabreicht. Eine zur Induktion der Cytokin-Biosynthese
wirksame Menge einer Verbindung ist eine Menge, die dazu ausreicht,
einen oder mehrere Zelltypen, wie z.B. Monozyten, Makrophagen, dendritische
Zellen und B-Zellen, zur Produktion einer Menge eines oder mehrerer
Cytokine, wie beispielsweise INF-α,
TNF-α, IL-1,
6, 10 und 12, die gegenüber
dem Hintergrundniveau derartiger Cytokine erhöht ist, zu veranlassen. Die
genaue Menge variiert mit an sich bekannten Faktoren, jedoch wird
erwartet, daß es
sich um eine Dosis von etwa 100 ng/kg bis etwa 50 mg/kg und vorzugsweise
etwa 10 μg/kg
bis etwa 5 mg/kg handelt. Gegenstand der Erfindung ist ferner ein
Verfahren zur Behandlung einer Virusinfektion in einem Tier, bei
dem man dem Tier eine wirksame Menge einer Verbindung der Formel
I oder Formel II verabreicht. Eine zur Behandlung oder Inhibierung
einer Virusinfektion wirksame Menge ist eine Menge, die einen Rückgang einer
oder mehrerer der Manifestationen der Virusinfektion, wie viralen
Läsionen,
Virusbelastung, Geschwindigkeit der Virusproduktion und Mortalität im Vergleich
zu unbehandelten Vergleichstieren bewirkt. Die genaue Menge variiert
mit an sich bekannten Faktoren, jedoch wird erwartet, daß es sich
um eine Dosis von 100 ng/kg bis etwa 50 mg/kg und vorzugsweise etwa
10 μg/kg
bis etwa 5 mg/kg handelt.
-
Die
Erfindung wird anhand der folgenden Beispiele näher erläutert.
-
Beispiel 1
-
Verbindung der Formel
V
-
2-(5-Methyl-1H-tetrazol-1-yl)nikotinsäure
-
Teil A:
-
2-Aminonicotinsäure (5 g,
36 mmol) wurde in Essigsäureanhydrid
(25 ml) suspendiert und dann zwei Stunden unter Rückfluß erhitzt.
Die Reaktionsmischung wurde unter Vakuum aufkonzentriert. Der erhaltene Rückstand
wurde mit Essigsäureethylester
und Hexan aufgeschlämmt
und dann filtriert, was 5 g 2-Methyl-4H-pyrido[2,3-d][1,3]oxazin-4-on ergab.
-
Teil B:
-
Die
Substanz aus Teil A wurde mit Essigsäure (75 ml) bedeckt und mit
Natriumazid (2 g) versetzt wonach die Reaktionsmischung über das
Wochenende bei Umgebungstemperatur gerührt wurde. Der erhaltene Niederschlag
wurde abfiltriert und dann getrocknet, was 5,6 g 2-(5-Methyl-1H-tetrazol-1-yl)nikotinsäure in Form
eines weißen
Feststoffs, Fp. 178-180°C
(Gasentwicklung), ergab.
Analyse: berechnet für C8H7N5O2: %C, 46,83; %H, 3,44; %N, 34,13; gefunden:
%C, 46,38; %H, 3,36; %N, 34,01.
-
Beispiel 2
-
Verbindung der Formel
VI
-
2-(5-Methyl-1H-tetrazol-1-yl)nikotinsäureethylester
-
2-(5-Methyl-1H-tetrazol-1-yl)nikotinsäure (5,6
g, 27 mmol) wurde in Aceton (250 ml) suspendiert und mit Kaliumcarbonat
(5 g) und Ethyliodid (5 ml) versetzt, wonach die Reaktionsmischung
2 Stunden unter Rückfluß erhitzt
wurde. Der nach Abziehen des Acetons unter Vakuum verbleibende Rückstand
wurde zwischen Wasser und Dichlormethan verteilt. Die Dichlormethanschicht
wurde abgetrennt, getrocknet und dann unter Vakuum auf konzentriert,
was 6,3 g 2-(5-Methyl-1H-tetrazol-1-yl)nikotinsäureethylester ergab.
-
Beispiel 3
-
Verbindung der Formel
VII
-
Tetrazolo[1,5-a][1,8]naphthyridin-5-ol
-
2-(5-Methyl-1H-tetrazol-1-yl)nikotinsäureethylester
(6,3 g, 27 mmol) wurde mit N,N-Dimethylformamid (50 ml) bedeckt
und mit Kaliumethoxid (4,5 g, 54 mmol) versetzt, wonach die Reaktionsmischung
2 Stunden bei Umgebungstemperatur gerührt wurde. Dann wurde die Reaktionsmischung
in Eiswasser mit etwa 17 ml Essigsäure gegossen. Der erhaltene
Niederschlag wurde abfiltriert, mit Wasser gewaschen und dann getrocknet,
was 4,5 g Tetrazolo[1,5-a][1,8]naphthyridin-5-ol in Form eines gebrochen
weißen
Feststoffs, Fp. 236° (Zersetzung),
ergab. Analyse: berechnet für
CaH5N5O: %C, 51,34;
%H, 2,69; %N, 37,42; gefunden: %C, 51,23; %H, 2,77; %N, 37,25.
-
Beispiel 4
-
5-Chlortetrazolo[1,5-a][1,8]naphthyridin
-
Tetrazolo[1,5-a][1,8]naphthyridin-5-ol
(0,5 g, 2,67 mmol) wurde in Phosphoroxidchlorid (10 ml) suspendiert
und 4 Stunden unter Rückfluß erhitzt.
Der nach Auf konzentrieren der Reaktionsmischung unter Vakuum verbleibende
Rückstand
wurde in Wasser gegossen. Nach Zugabe von Dichlormethan wurde die
wäßrige Schicht
mit Natriumcarbonat basisch gestellt. Die Dichlormethanschicht wurde
abgetrennt, über
Magnesiumsulfat getrocknet, filtriert und dann unter Vakuum auf
konzentriert. Der erhaltene Feststoff wurde aus Toluol umkristallisiert,
was 0,3 g 5-Chlortetrazolo[1,5-a][1,8]naphthyridin
in Form eines Feststoffs, Fp. 229-230°C (Zersetzung), ergab. Analyse:
berechnet für
C8H4ClN5:
%C, 46,73; %H, 1,96; %N, 34,06; gefunden: %C, 46,87; %H, 1,54; %N,
33,93.
-
Beispiel 5
-
Verbindung der Formel
VIII
-
4-Nitrotetrazolo[1,5-a][1,8]naphthyridin-5-ol
-
Eine
Suspension von Tetrazolo[1,5-a][1,8]naphthyridin-5-ol (4 g, 21 mmol) in Essigsäure (50
ml) wurde mit Salpetersäure
(1,33 ml, 16 M) versetzt. Die Reaktionsmischung wurde 5 Minuten
auf einem Dampfbad erhitzt und dann auf Umgebungstemperatur abgekühlt. Dann
wurde die Reaktionsmischung mit Natriumacetat (0,3 äq.) in etwas
Wasser versetzt. Der erhaltene Feststoff wurde abfiltriert und getrocknet,
was 5 g 4-Nitrotetrazolo[1,5-a][1,8]naphthyridin-5-ol
in Form eines Feststoffs, Fp. 278°C
(Zersetzung), ergab. Analyse: berechnet für C8H4N6O3 +
1,1 H2O: %C, 38,12; %H, 2,48; %N, 33,35;
gefunden: %C, 37,99; %H, 2,41; %N, 32,82.
-
Beispiel 6
-
Verbindung der Formel
X
-
N5-(2-Methylpropyl)-4-nitrotetrazolo[1,5-a][1,8]naphthyridin-5-amin
-
4-Nitrotetrazolo[1,5-a][1,8]naphthyridin-5-ol
(3 g, 13 mmol) wurde in Dichlormethan (3,8 ml) suspendiert und mit
Triethylamin (1,8 ml) versetzt, wonach die Reaktionsmischung in
einem Eisbad abgekühlt
wurde. Dann wurde Trifluormethansulfonsäureanhydrid (2,2 ml) zugetropft.
Nach Zugabe von Isobutylamin (3,8 ml) in einem Guß stieg
die Temperatur der Reaktionsmischung in Folge der exothermen Reaktion
an. Die Reaktionsmischung wurde zwischen Dichlormethan und wäßrigem Natriumhydrogencarbonat
verteilt. Die Dichlormethanschicht wurde abgetrennt, über Magnesiumsulfat
getrocknet und dann über
eine Kieselgelschicht filtriert. Das Kieselgel wurde zunächst mit
Dichlormethan und dann mit 5% Methanol in Dichlormethan eluiert.
Das Elutionsmittel wurde abgedampft, was N5-(2-Methylpropyl)-4-nitrotetrazolo[1,5-a][1,8]naphthyridin- 5-amin in Form eines
gelben Feststoffs, Fp. 171°C
(Zersetzung), ergab. Analyse: berechnet für C12H13N7O2:
%C, 50,17; %H, 4,56; %N, 34,13; gefunden: %C, 49,84; %H, 4,51; %N,
33,88.
-
Beispiel 7
-
Verbindung der Formel
XI
-
N5-(2-Methylpropyl)tetrazolo[1,5-a][1,8]naphthyridin-4,5-diamin
-
Eine
Suspension von N5-(2-Methylpropyl)-4-nitrotetrazolo[1,5-a][1,8]naphthyridin-5-amin
(2,45 g, 8,5 mmol) in Ethanol (120 ml) wurde mit einer katalytisch
wirksamen Menge von 5% Platin auf Kohle versetzt. Die Reaktionsmischung
wurde in einer Parr-Apparatur
2 Stunden bei 50 psi (3,5 kg/cm2) Wasserstoff
reduziert. Die Reaktionsmischung wurde zur Entfernung des Katalysators
filtriert. Das Filtrat wurde unter Vakuum auf konzentriert, was
N5-(2-Methylpropyl)tetrazolo[1,5-a][1,8]naphthyridin-4,5-diamin
in Form eines Öls
ergab.
-
Beispiel 8
-
Verbindung der Formel
XII
-
1-(2-Methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,8]naphthyridin
-
Das
N5-(2-Methylpropyl)tetrazolo[1,5-a][1,8]naphthyridin-4,5-diamin
aus Beispiel 7 wurde mit Essigsäurediethoxymethylester
(2 ml) vereinigt und 3 Stunden auf einem Dampfbad erhitzt. Die Reaktionsmischung wurde über Nacht
bei Umgebungstemperatur stehengelassen und dann mit Dichlormethan
und Methanol verdünnt.
Die erhaltene Lösung
wurde zur Entfernung des Dichlormethans und zur Verringerung des
Methanolvolumens auf 50 ml erhitzt und dann abgekühlt. Der
erhaltene Niederschlag wurde abfiltriert, was 1,2 g 1-(2-Methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,8)naphthyridin
in Form eines Feststoffs, Fp. 248- 250°C (Zersetzung),
ergab. Analyse: berechnet für
C13H13N7:
%C, 58,42; %H, 4,90; %N, 36,68; gefunden: %C, 58,04; %H, 4,79; %N,
36,23.
-
Beispiel
9 Verbindung
der Formel I 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin-hydrat
-
Teil A:
-
Eine
Lösung
von 1-(2-Methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,8]naphthyridin (0,5
g, 1,87 mmol) in 1,2-Dichlorbenzol (15 ml) wurde mit Triphenylphosphin
(1,0 g, 3,7 mmol) versetzt. Die Reaktionsmischung wurde 2 Stunden
unter Rückfluß erhitzt
und dann zur Entfernung des größten Teils
des 1,2-Dichlorbenzols unter Vakuum auf konzentriert. Der Rückstand
wurde 30 Minuten mit Hexangemisch aufgeschlämmt. Das erhaltene feste 1-(2-Methylpropyl)-N-triphenylphosphinyl-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin
wurde abfiltriert und getrocknet.
-
Teil B:
-
Das
1-(2-Methylpropyl)-N-triphenylphosphinyl-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin
aus Teil A wurde in Methanol (15 ml) gelöst. Nach Zusatz von Salzsäure (10
ml, 0,6 N) wurde die Reaktionsmischung 1 Stunde unter Rückfluß erhitzt.
Der nach Auf konzentrieren der Reaktionsmischung unter Vakuum verbleibende Rückstand
wurde mit Wasser verdünnt
und dann mit Natriumhydrogencarbonat basisch gestellt. Der erhaltene Feststoff
wurde abfiltriert, mit Ether aufgeschlämmt und dann abfiltriert. Der
Feststoff wurde in Toluol (25 ml) suspendiert. Die Suspension wurde
zum Rückfluß erhitzt
und dann zum Auflösen
des Feststoffs mit Methanol (10 ml) verdünnt. Die Lösung wurde zur Entfernung des
Methanols unter Rückfluß erhitzt
und dann auf Umgebungstemperatur abgekühlt. Der erhaltene Niederschlag
wurde abfiltriert und dann auf Kieselgel aufgetragen. Das Kieselgel
wurde mit 10-20% Methanol in Essigsäureethylester eluiert. Das
Elutionsmittel wurde bis zur Trockne auf konzentriert. Die erhaltene
Substanz wurde aus Methanol und Wasser umkristallisiert, was 0,35
g 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin-hydrat
in Form eines Feststoffs, Fp. 325-330°C (Zersetzung), ergab. Analyse:
berechnet für
C13H15N5 + ¼ H2O: %C, 63,52; %H, 6,35; %N, 28,49; gefunden: %C,
64,02; %H, 5,87; %N, 28,23.
-
Beispiel
10 Verbindung
der Formel II 6,7,8,9-Tetrahydro-1-(2-methylpropyl)-1H-imidazo[9,5-c][1,8]naphthyridin-4-amin
-
Eine
Lösung
von 1-(2-Methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,8]naphthyridin in
Trifluoressigsäure
(30 ml) wurde mit Platinoxid-Katalysator versetzt. Die Reaktionsmischung
wurde in einer Parr-Apparatur 5 Stunden bei 50 psi (3,5 kg/cm2) Wasserstoffdruck reduziert. Die Reaktionsmischung
wurde zur Entfernung des Katalysators filtriert. Das Filtrat wurde
unter Vakuum auf konzentriert. Der Rückstand wurde mit Wasser und
Natriumhydrogencarbonat vereinigt. Der erhaltene Niederschlag wurde
abfiltriert. Der Feststoff wurde in 1 N Salzsäure gelöst und über Aktivkohle filtriert. Das
Filtrat wurde mit 10% Natriumhydroxid behandelt. Der erhaltene Niederschlag
wurde abfiltriert und dann aus Essigsäurethylester/Methanol umkristallisiert.
Die umkristallisierte Substanz wurde in Dichlormethan/Methanol gelöst und auf
eine Kieselgelsäule
aufgetragen. Die Säule
wurde mit 10% Methanol in Essigsäureethylester
eluiert. Der nach Auf konzentrieren des Elutionsmittels unter Vakuum
verbleibende Rückstand
wurde aus Methanol/Wasser umkristallisiert, was 0,9 g 6,7,8,9-Tetrahydro-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin
in Form eines Feststoffs, Fp. 231-233°C, ergab. Analyse: berechnet
für C13H19N5:
%C, 63,65; %H, 7,81; %N, 28,55; gefunden: %C, 62,99; %H, 7,74; %N,
28,33.
-
Beispiel 11
-
Verbindung der Formel
XII
-
2-Butyl-1-(2-methylpropyl)-1H-tetrazolo
[1,5-a]imidazo[4,5-c][1,8]naphthyridin.
-
Eine
Suspension von N5-(2-Methylpropyl)-4-nitrotetrazolo[1,5-a][1,8]naphthyridin-5-amin
(5 g, 17,4 mmol) in Ethanol (300 ml) wurde mit einer katalytisch
wirksamen Menge von 5% Platin auf Kohle versetzt. Die Reaktionsmischung
wurde in einer Parr-Apparatur 2 Stunden bei 50 psi (3,5 kg/cm2) Wasserstoff reduziert. Die Reaktionsmischung
wurde zur Entfernung des Katalysators filtriert. Das Filtrat wurde
unter Vakuum auf konzentriert, was N5-(2-Methylpropyl)tetrazolo[1,5-a][1,8]naphthyridin-4,5-diamin
in Form eines Öls
ergab.
-
Das Öl wurde
mit Essigsäure
(300 ml) bedeckt und mit Valerylchlorid (2,1 ml, 17,4 mmol) versetzt,
wonach die erhaltene Mischung über
Nacht unter Rückfluß erhitzt
wurde. Der nach Auf konzentrieren der Reaktionsmischung unter Vakuum
erhaltene Rückstand
wurde in Dichlormethan aufgenommen, mit Natriumhydrogencarbonat
gewaschen, über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert.
Der Rückstand
wurde mittels Flash-Chromatographie
(Kieselgel; Elution mit 2-3% Methanol in Dichlormethan) gereinigt.
Das isolierte Produkt wurde mittels präparativer Hochleistungs-Flüssigkeitschromatographie
unter Elution mit 2% Methanol in Dichlormethan weiter gereinigt,
was 2-Butyl-1-(2-methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,8]-naphthyridin in Form
eines Feststoffs, Fp. 182-184°C,
ergab. Analyse: berechnet für
C17H21N7: %C,
63,14; %H, 6,55; %N, 30,32; gefunden: %C, 63,45; %H, 6,60; %N, 30,40.
-
Beispiel
12 Verbindung
der Formel I 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin
-
Eine
Lösung
von 2-Butyl-1-(2-methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,8]naphthyridin
(0,6 g, 1,8 mmol) in 1,2-Dichlorbenzol (15 ml) wurde mit Triphenylphosphin
(0,9 g, 3,7 mmol) versetzt. Die erhaltene Mischung wurde 2 Stunden
unter Rückfluß erhitzt
und dann zur Entfernung des größten Teils
des 1,2-Dichlorbenzols unter Vakuum auf konzentriert. Der Rückstand
wurde mit Hexangemisch aufgeschlämmt
und dann in Dichlormethan aufgenommen und über eine Kieselgelschicht filtriert.
Das Kieselgel wurde zunächst
zur Entfernung des 1,2-Dichlorbenzols mit Dichlormethan und dann
zur Gewinnung von 2-Butyl-1-(2-methylpropyl)-N-triphenylphosphinyl-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin
mit 10% Methanol in Dichlormethan eluiert.
-
Das
2-Butyl-1-(2-methylpropyl)-N-triphenylphosphinyl-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin
wurde in Methanol (15 ml) aufgenommen, mit Salzsäure (10 ml, 0,6 N) vereinigt
und dann 1 Stunde unter Rückfluß erhitzt.
Der nach Abziehen des Methanols unter Vakuum verbleibende Rückstand
wurde mit Wasser und 10%iger Salzsäure vereinigt und dann filtriert.
Das Filtrat wurde mit 10%iger Natronlauge neutralisiert. Der erhaltene
Niederschlag wurde abfiltriert und getrocknet. Der erhaltene Feststoff
wurde in Toluol unter Rückfluß erhitzt.
Nach Verringerung des Toluolvolumens wurde das Produkt unter Argonatmosphäre auskristallisieren gelassen,
was 0,25 g 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin-hemihydrat,
Fp. 237-240°C,
ergab. Analyse: berechnet für
C17H23N5 + ½ H2O: %C, 68,66; %H, 7,79; %N, 23,55; gefunden:
%C, 66,80; %H, 7,62; %N, 23,46.
-
Beispiel
13 Verbindung
der Formel II 2-Butyl-6,7,8,9-tetrahydro-1-(2-methylpropyl)-18-imidazo[4,5-c][1,8]naphthyridin-4-amin
-
Eine
Lösung
von 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin
(2,0 g, 6,2 mmol) in Trifluoressigsäure (30 ml) wurde mit einer katalytisch
wirksamen Menge Platinoxid versetzt. Die Reaktionsmischung wurde
in einer Parr-Apparatur unter 50 psi (3,5 kg/cm2)
Wasserstoffdruck reduziert. Die Reaktionsmischung wurde zur Entfernung
des Katalysators filtriert. Das Filtrat wurde unter Vakuum auf konzentriert.
Der Rückstand
wurde mit Wasser, Natriumhydrogencarbonat und 10%iger Natronlauge
vereinigt. Das gewonnene Öl
wurde mittels Umkehrphasen-Hochleistungsflüssigkeitschromatographie
unter Elution mit einem Gemisch aus Puffer (7,68 g Kaliumdihydrogenphosphat;
1,69 g Natriumhydroxid, 1 l Wasser) und Methanol im Verhältnis 30:70
gereinigt, was 2-Butyl-6,7,8,9-tetrahydro-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,8]naphthyridin-4-amin-hemihydrat
in Form eines Feststoffs, Fp. 81-84°C, ergab. Analyse: berechnet
für C17H27N5 + ½ H2O: %C, 65,77; %H, 9,09; %N, 22,56; gefunden:
%C, 65,57; %H, 9,15; %N, 22,53.
-
Beispiel 14
-
Verbindung der Formel
XVIII
-
3-(5-Methyl-1H-tetrazol-1-yl)pyridin-4-carbonsäure
-
3-Aminopyridin-4-carbonsäure (50,0
g, 0,36 mol) wurde in Essigsäureanhydrid
(250 ml) suspendiert und 2 Stunden unter Rückfluß erhitzt. Die Reaktionsmischung
wurde unter Vakuum auf konzentriert. Der feste Rückstand wurde mit Heptan aufgeschlämmt und
dann unter Vakuum auf konzentriert. Der erhaltene Feststoff wurde
mit Essigsäure
(300 ml) bedeckt und dann mit Natriumazid (23,5 g, 0,36 mol) versetzt.
Die Reaktion erreichte in Folge der exothermen Reaktion eine Temperatur
von 50°C.
Die Reaktionsmischung wurde über Nacht
bei Umgebungstemperatur rühren
gelassen. Der Niederschlag wurde abfiltriert und dann mit Methanol aufgeschlämmt und
filtriert. Der Feststoff wurde in 10% Natriumhydroxid gelöst. Die
Lösung
wurde 30 Minuten auf einem Dampfbad erhitzt, auf Umgebungstemperatur
abkühlen
gelassen und dann mit 6 N Salzsäure
neutralisiert. Der erhaltene Niederschlag wurde abfiltriert, mit
Wasser gewaschen und getrocknet, was 64,5 g 3-(5-Methyl-1H-tetrazol-1-yl)pyridin-4-carbonsäure in Form
eines gebrochen weißen
Feststoffs, Fp. 214-215°C
(Zersetzung), ergab.
-
Beispiel 15
-
Verbindung der Formel
XIX
-
3-(5-Methyl-1H-tetrazol-1-yl)pyridin-4-carbonsäureethylester
-
Eine
Suspension von 3-(5-Methyl-1H-tetrazol-1-yl)pyridin-4-carbonsäure (36 g) in Dichlormethan
(800 ml) wurde mit Dimethylformamiddiethylacetal (46 ml) versetzt.
Die Reaktionsmischung wurde über
Nacht bei Umgebungstemperatur gerührt und dann sechsmal mit Wasser
(500 ml) gewaschen, über
Magnesiumsulfat getrocket und unter Vakuum auf konzentriert. Der
Rückstand
wurde aus Essigsäureethylester/Hexangemisch umkristallisiert,
was 40 g 3-(5-Methyl-1H-tetrazol-1-yl)pyridin-4-carbonsäureethylester in Form eines
Feststoffs ergab.
-
Beispiel 16
-
Verbindung der Formel
XX
-
Tetrazolo[1,5-a][1,7]naphthyridin-5-ol-hydrat
-
Eine
Mischung aus 3-(5-Methyl-1H-tetrazol-1-yl)pyridin-4-carbonsäureethylester
(28 g) und Dimethylformamid (280 ml) wurde mit Kaliumethoxid (20,2
g) versetzt. Die Reaktionsmischung wurde über Nacht bei Umgebungstemperatur
rühren
gelassen und dann in kalte verdünnte
Essigsäure
gegossen. Der erhaltene Niederschlag wurde isoliert, mit Wasser
gewaschen und getrocknet, was 22,4 g Tetrazolo[1,5-a][1,7]naphthyridin-5-ol-hydrat
in Form eines Feststoffs, Fp. 247-248°C
(Zersetzung), ergab. Analyse: berechnet für C8H5N5O: %C, 46,83;
%H, 3,44; %N, 34,13; gefunden: %C, 46,48; %H, 3,42; %N, 34,03.
-
Beispiel 17
-
Verbindung der Formel
XXI
-
5-Chlortetrazolo[1,5-a][1,7]naphthyridin
-
Eine
Suspension von Tetrazolo[1,5-a][1,7]naphthyridin-5-ol (3,5 g) in Phosphoroxidchlorid
(15 ml) wurde 2 Stunden auf 90°C
erhitzt. Der nach Auf konzentrieren der Reaktionsmischung unter
Vakuum verbleibende Rückstand
wurde in Eiswasser gegossen und mit Dichlormethan versetzt, wonach
durch Zugabe von 10% Natriumhydroxid ein neutraler pH-Wert eingestellt
wurde. Das Produkt wurde in Dichlormethan verteilt. Die Dichlormethanschicht
wurde abgetrennt, über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert,
was 3,8 g 5-Chlortetrazolo[1,5-a][1,7]naphthyridin in Form eines
Feststoffs, Fp. 176-177°C,
ergab. Analyse: berechnet für
C8H4ClN5:
%C, 46,73; %H, 1,96; %N, 34,06; gefunden: %C, 46,80; %H, 2,16; %N,
34,45.
-
Beispiel 18
-
Verbindung der Formel
XXII
-
N5-(2-Methylpropyl)tetrazolo[1,5-a][1,7]naphthyridin-5- amin
-
Eine
Suspension von 5-Chlortetrazolo[1,5-a][1,7]naphthyridin (20 g) in
Isobutylamin (100 ml) wurde einige Stunden unter Rückfluß erhitzt.
Der nach Auf konzentrieren der Reaktionsmischung unter Vakuum verbleibende
Rückstand
wurde in Dichlormethan aufgenommen, mit Wasser gewaschen, über Magnesiumsulfat getrocknet
und dann unter Vakuum auf konzentriert. Der Rückstand wurde aus Toluol umkristallisiert,
was eine Substanz ergab, bei der es sich gemäß Dünnschichtchromatographie um
ein Gemisch handelte. Die Substanz wurde mittels Flash-Chromatographie
an Kieselgel unter Elution mit Dichlormethan, 5-20% Essigsäureethylester
in Dichlormethan und 10% Methanol in Dichlormethan gereinigt. Die
Fraktionen mit der langsamer laufenden Substanz wurden auf konzentriert, was
N5-(2-Methylpropyl)tetrazolo[1,5-a][1,7]naphthyridin-5-amin
in Form eines Feststoffs, Fp. 220-221°C, ergab. Analyse: berechnet
für C12H14N6:
%C, 59,49; %H, 5,82; %N, 34,69; gefunden: %C, 59,35; %H, 5,89; %N,
34,88.
-
Beispiel 19
-
Verbindung der Formel
XXIII
-
N5-(2-Methylpropyl)-4-nitrotetrazolo[1,5-a][1,7]naphthyridin-5-amin
-
Eine
Lösung
von N5-(2-Methylpropyl)tetrazolo[1,5-a][1,7]naphthyridin-5-amin
(2,0 g, 8,26 mmol) in Essigsäure
wurde mit Salpetersäure
(2 Äquivalente,
16 M) versetzt. Die Reaktionsmischung wurde etwa 1 Stunde auf einem
Dampfbad erhitzt und dann unter Vakuum auf konzentriert. Der Rückstand
wurde in Eiswasser gegossen, wonach die erhaltene Mischung mit Natriumhydrogencarbonat
neutralisiert wurde. Der erhaltene Niederschlag wurde mit Dichlormethan
extrahiert. Die Dichlormethanextrakte wurden vereinigt, mit Wasser
gewaschen und über
Magnesiumsulfat getrocknet. Da gemäß Dünnschichtchromatographie ein
Gemisch vorlag, wurde die Substanz über eine Kieselgelschicht filtriert,
wobei mit 5% Essigsäureethylester
in Dichlormethan eluiert wurde. Die Reaktion wurde mit 4 g Edukt,
aber nur einem Äquivalent
Salpetersäure
wiederholt. Dabei wurde ebenfalls ein Gemisch erhalten. Die Substanz
aus beiden Umsetzungen wurde vereinigt und dann mittels Flash-Chromatographie unter
Elution mit Gemischen aus Hexan und Essigsäureethylester gereinigt. Die die
langsamer laufende Substanz enthaltenden Fraktionen wurden vereinigt,
was etwa 0,3 g N5-(2-Methylpropyl)-4-nitrotetrazolo[1,5-a][1,7]naphthyridin-5-amin
in Form eines gelben Feststoffs, Fp. 173-174°C, ergab. Analyse: berechnet
für C12H13N7O2: %C, 50,17; %H, 4,56; %N, 34,13; gefunden:
%C, 49,85; %H, 4,53; %N, 34,26.
-
Beispiel 20
-
Verbindung der Formel
XXIV
-
N5-(2-Methylpropyl)tetrazolo[1,5-a][1,7]naphthyridin-4,5-diamin
-
N5-(2-Methylpropyl)-4-nitrotetrazolo[1,5-a][1,7]naphthyridin-5-amin
(1,5 g, 5,22 mmol) wurde in Essigsäure (75 ml) suspendiert. Ein Überschuß von Natriumhydrogensulfid
wurde in möglichst
wenig Wasser gelöst und
zu der Suspension gegeben. Die Reaktionsmischung wurde rot, und
die gesamte Substanz ging in Lösung.
Die Reaktionsmischung wurde zweimal mit Dichlormethan (150 ml) extrahiert.
Die Extrakte wurden vereinigt, mit Wasser gewaschen, über Magnesiumsulfat
getrocknet, filtriert und unter Vakuum auf konzentriert, was 1,22
g N5-(2-Methylpropyl)tetrazolo[1,5-a][1,7]naphthyridin-4,5-diamin in Form
eines hellgelben Feststoffs, Fp. 203-204, 5°C, ergab. Analyse: berechnet
für C12H15N7:
%C, 56,02; %H, 5,88; %N, 38,11; gefunden: %C, 55,68; %H, 5,81; %N,
37,74.
-
Beispiel 21
-
Verbindung der Formel
XXV
-
1-(2-Methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,7]naphthyridin
-
N5-(2-Methylpropyl)tetrazolo[1,5-a][1,7]naphthyridin-4,5-diamin (1,1 g,
4,3 mmol) wurde mit Essigsäurediethoxymethylester
(2 ml) vereinigt und über
Nacht auf einem Dampfbad erhitzt. Dann wurde die Reaktionsmischung
zwischen Dichlormethan und Ammoniumhydroxid verteilt. Die Dichlormethanschicht
wurde abgetrennt, mit Wasser gewaschen und über Magnesiumsulfat getrocknet
und unter Vakuum auf konzentriert. Der Rückstand wurde aus Essigsäureethylester/Hexan
umkristallisiert, was 0,85 g 1-(2-Methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,7]-naphthyridin in Form
eines Feststoffs, Fp. 181-182,5°C,
ergab. Analyse: berechnet für
C13H13N7:
%C, 58, 42; %H, 4,90; %N, 36,68; gefunden: %C, 58,87; %H, 5,04;
%N, 36,13.
-
Beispiel
22 Verbindung
der Formel I 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
-
Teil A:
-
Eine
Suspension von 1-(2-Methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,7]naphthyridin
(0,24 g, 0,9 mmol) in Dichlorbenzol (15 ml) wurde mit Triphenylphosphin
(0,49 g, 1,8 mmol) versetzt. Die Reaktionsmischung wurde über Nacht
unter Rückfluß erhitzt
und dann unter Vakuum auf konzentriert. Der Rückstand wurde mit Hexan aufgeschlämmt, wonach
das erhaltene feste 1-(2-Methylpropyl)-N-triphenylphosphinyl-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
abfiltriert wurde.
-
Teil B:
-
Das
1-(2-Methylpropyl)-N-triphenylphosphinyl-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
aus Teil A wurde in Methanol (30 ml) gelöst. Die Lösung wurde mit Salzsäure (3 ml,
3 N) versetzt, wonach die Reaktionsmischung über Nacht unter Rückfluß erhitzt
und dann zur Entfernung des Methanols unter Vakuum auf konzentriert
wurde. Der wäßrige Rückstand
wurde mit Natriumhydrogencarbonat neutralisiert und dann mit Dichlormethan
extrahiert. Das Extrakt wurde über Magnesiumsulfat
getrocknet und dann unter Vakuum auf konzentriert. Der Rückstand
wurde mittels Flash-Chromatographie
(Kieselgel unter Elution mit 5-10% Methanol in Dichlormethan) gereinigt,
was 0,15 g 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
in Form eines Feststoffs, Fp. 306-307°C, ergab. Analyse: berechnet
für C13H15N5:
%C, 64,71; %H, 6,27; %N, 29,02; gefunden: %C, 65,10; %H, 6,28; %N,
28,70.
-
Beispiel
23 Verbindung
der Formel II 6,7,8,9-Tetrahydro-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
-
Eine
Lösung
von 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin (0,4 g, 1,66
mmol) in Trifluoressigsäure
wurde mit einer katalytisch wirksamen Menge Platinoxid versetzt.
Die Reaktionsmischung wurde in einer Parr-Apparatur über Nacht
bei 50 psi (3,5 kg/cm2) Wasserstoffdruck
reduziert. Die Reaktionsmischung wurde zur Entfernung des Katalysators
filtriert und mit Methanol gewaschen. Das Filtrat wurde unter Vakuum
auf konzentriert. Der Rückstand
wurde mit Dichlormethan vereinigt und mit wäßriger Natriumhydrogencarbonatlösung versetzt,
bis die Mischung basisch war. Die Dichlormethanschicht wurde abgetrennt.
Die wäßrige Schicht
wurde fünfmal
mit Dichlormethan (100 ml) extrahiert. Die Dichlormethanextrakte
wurden vereinigt, über
Magnesiumsulfat getrocknet und unter Vakuum auf konzentriert. Der erhaltene
Rückstand
wurde aus Toluol umkristallisiert, was 0,34 g 6,7,8,9-Tetrahydro-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
in Form eines Feststoffs, Fp. 220-223°C, ergab. Analyse: berechnet
für C13H19N5 + ¼ H2O: %C, 62,50; %H, 7,87; %N, 28,03; gefunden:
%C, 62,50; %H, 7,72; %N, 27,46.
-
Beispiel 24
-
Verbindung der Formel
XXV
-
2-Methyl-1-(2-methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,7]naphthyridin
-
Eine
Lösung
von N-(2-Methylpropyl)tetrazolo[1,5-a][1,7]naphthyridin-4,5-diamin (0,8
g, 3,1 mmol) in Essigsäure
wurde mit Essigsäureanhydrid
(2-3 ml) versetzt. Die Reaktionsmischung wurde einige Stunden auf einem
Dampfbad erhitzt und dann unter Vakuum aufkonzentriert. Der Rückstand
wurde zwischen Dichlormethan und Wasser verteilt. Die wäßrige Schicht
wurde mit 10%iger Natronlauge basisch gestellt, wonach die Dichlormethanschicht
abgetrennt, über
Magnesiumsulfat getrocknet und unter Vakuum auf konzentriert wurde. Der
Rückstand
wurde mit Flash-Chromatographie (Kieselgel unter Elution mit 2-5%
Methanol in Dichlormethan) gereinigt, was 0,25 g 2-Methyl-1-(2-methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,7]naphthyridin
in Form eines Feststoffs, Fp. 157-158°C, ergab. Analyse: berechnet
für C14H15N7:
%C, 59,77; %H, 5,37; %N, 34,85; gefunden: %C, 59,64; %H, 5,48; %N,
34,98.
-
Beispiel
25 Verbindung
der Formel I 2-Methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
-
Teil A:
-
Eine
Suspension von 2-Methyl-1-(2-methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,7]naphthyridin (1
g, 4 mmol) in Dichlorbenzol wurde mit Triphenylphosphin (2,5 g,
9,6 mmol) versetzt. Die Reaktionsmischung wurde über Nacht unter Rückfluß erhitzt
und dann unter Vakuum auf konzentriert. Der Rückstand wurde mit Hexan aufgeschlämmt, wonach
das erhaltene feste 2-Methyl-1-(2-methylpropyl)-N-triphenylphosphinyl-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
abfiltriert wurde.
-
Teil B:
-
Das
2-Methyl-1-(2-methylpropyl)-N-triphenylphosphinyl-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin aus
Teil A wurde in Methanol (100 ml) gelöst. Die Lösung wurde mit Salzsäure (10
ml, 3 N) versetzt, wonach die Reaktionsmischung über Nacht unter Rückfluß erhitzt
und dann zur Entfernung des Methanols unter Vakuum auf konzentriert
wurde. Der Rückstand
wurde mit Flash-Chromatographie
(Kieselgel unter Elution mit Dichlormethan und allmählicher
Erhöhung
der Polarität
auf 5% Methanol in Dichlormethan) gereinigt, was 2-Methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
in Form eines Feststoffs, Fp. 322-324°C, ergab.
Analyse: berechnet für
C14H17N5:
%C, 65,86; %H, 6,71; %N, 27,43; gefunden: %C, 65,81; %H, 6,64; %N,
27,41.
-
Beispiel
26 Verbindung
der Formel II 6,7,8,9-Tetrahydro-2-methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
-
Eine
Lösung
von 2-Methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
(0,1 g, 0,4 mol) in Trifluoressigsäure wurde mit einer katalytisch
wirksamen Menge Platinoxid versetzt. Die Reaktionsmischung wurde
in einer Parr-Apparatur über
Nacht bei 50 psi (3,5 kg/cm2) Wasserstoffdruck
reduziert. Die Reaktionsmischung wurde zur Entfernung des Katalysators
filtriert und mit Methanol gewaschen, wonach das Filtrat unter Vakuum
aufkonzentriert wurde. Der Rückstand
wurde mit Dichlormethan vereinigt und mit wäßrigem Natriumhydrogencarbonat
versetzt, bis die Mischung basisch war. Die Dichlormethanschicht
wurde abgetrennt, wonach die wäßrige Schicht
dreimal mit Dichlormethan (100 ml) extrahiert wurde. Die vereinigten
Dichlormethanextrakte wurden über
Magnesiumsulfat getrocknet und unter Vakuum aufkonzentriert. Der
erhaltene Rückstand
wurde aus Toluol umkristallisiert, was 6,7,8,9-Tetrahydro-2-methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
in Form eines Feststoffs, Fp. 226-230°C,
ergab. Analyse: berechnet für C19H21N5 +
1, 75 H2O %C, 57,81; %H, 8,49; %N, 24,07;
gefunden: %C, 57,89; %H, 8,04; %N, 23,45.
-
Beispiel
27 Verbindung
der Formel I 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
-
Teil A:
-
Eine
Lösung
von N5-(2-Methylpropyl)tetrazolo[1,5-a][1,7]naphthyridin-4,5-diamin
(1,5 g, 5,8 mmol) in Acetonitril (15 ml) wurde mit Valerylchlorid
(0,76 ml, 6,4 mmol) versetzt. Die Reaktionsmischung wurde einige Stunden
bei Umgebungstemperatur rühren
gelassen. Der erhaltene Niederschlag wurde abfiltriert. Laut Dünnschichtchromatographie
enthielt die Substanz zwei Komponenten. Der Feststoff wurde in Essigsäure gelöst und über Nacht
unter Rückfluß erhitzt.
Der nach Auf konzentrieren der Reaktionsmischung unter Vakuum erhaltene
Rückstand
wurde mit Dichlormethan extrahiert. Das Dichlormethanextrakt wurde
mit Wasser gewaschen, über
Magnesiumsulfat getrocknet und unter Vakuum auf konzentriert, was
ein Gemisch aus 2-Butyl-1-(2-methylpropyl)-1H-tetrazolo[1,5-a]imidazo[4,5-c][1,7]naphthyridin
und dem acylierten, aber nicht cyclisierten Zwischenprodukt ergab.
-
Teil B:
-
Eine
Lösung
der Substanz aus Teil A in Dichlorbenzol wurde mit Triphenylphosphin
(2,4 g) versetzt. Die Reaktionsmischung wurde über Nacht unter Rückfluß erhitzt
und dann unter Vakuum auf konzentriert. Der Rückstand wurde mit Hexan aufgeschlämmt, wonach
das erhaltene feste 2-Butyl-1-(2-methylpropyl)-N-triphenylphosphinyl-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin abfiltriert
wurde.
-
Teil C:
-
Das
2-Butyl-1-(2-methylpropyl)-N-triphenylphosphinyl- 1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
aus Teil B wurde in Methanol gelöst.
Die Lösung
wurde mit Salzsäure
(3 N) versetzt, wonach die Reaktionsmischung über Nacht unter Rückfluß erhitzt
und dann zur Entfernung des Methanols unter Vakuum auf konzentriert
wurde. Der wäßrige Rückstand
wurde mit Dichlormethan vermischt und dann mit wäßrigem Natriumhydrogencarbonat
neutralisiert. Die Dichlormethanschicht wurde abgetrennt, über Magnesiumsulfat
getrocknet und unter Vakuum auf konzentriert. Der Rückstand
wurde mittels Flash-Chromatographie (Kieselgel unter Elution mit
Dichlormethan und allmählicher
Erhöhung
der Polarität
auf 5% Methanol in Dichlormethan) gereinigt, was 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
in Form eines Feststoffs, Fp. 213-214°C, ergab. Analyse: berechnet
für C17H23N5:
%C, 68,66; %H, 7,80; %N, 23,55; gefunden: %C, 68,26; %H, 7,69; %N,
23,41.
-
Beispiel
28 Verbindung
der Formel II 2-Butyl-6,7,8,9-Tetrahydro-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
-
Eine
Lösung
von 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
(0,5 g, 1,68 mmol) in Trifluoressigsäure (20 ml) wurde mit einer
katalytisch wirksamen Menge Platinoxid versetzt. Die Reaktionsmischung
wurde in einer Parr-Apparatur über
Nacht bei 50 psi (3,5 kg/cm2) reduziert.
Die Reaktionsmischung wurde zur Entfernung des Katalysators filtriert
und mit Methanol gewaschen. Das Filtrat wurde unter Vakuum auf konzentriert.
Der Rückstand
wurde mit Dichlormethan vereinigt und mit wäßrigem Natriumhydrogencarbonat
versetzt, bis die Mischung basisch war. Die Dichlormethanschicht
wurde abgetrennt. Die wäßrige Schicht
wurde dreimal mit Dichlormethan (100 ml) extrahiert. Die Dichlormethanextrakte
wurden vereinigt, über
Magnesiumsulfat getrocknet und unter Vakuum auf konzentriert. Der
erhaltene Rückstand
wurde aus Toluol umkristallisiert und dann mittels Flash-Chromatographie (Kieselgel
unter Elution mit 20% Methanol in Dichlormethan mit einer Spur Ammoniumhydroxid)
gereinigt, was 6,7,8,9-Tetrahydro-2-butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,7]naphthyridin-4-amin
in Form eines Feststoffs, Fp. 164-166°C, ergab. Analyse: berechnet
für C17H27N5 +
0,5 H2O: %C, 65,77; %H, 9,09; %N, 22,56;
gefunden: %C, 65,99; %H, 8,71; %N, 22,23.
-
Beispiel 29
-
Verbindung der Formel
XXXI
-
N4-(2-Methylpropyl)-3-nitro[1,5]naphthyridin-4-amin
-
Phosphoroxidchlorid
(0,6 ml, 6,44 mmol) wurde mit N,N-Dimethylformamid umgesetzt und dann
zu einer Lösung
von 3-Nitro[1,5]naphthyridin-4-ol (1,0 g, 5,23 mmol) in N,N-Dimethylformamid
(20 ml) gegeben. Die Reaktionsmischung wurde mit Hilfe eines Mantelkolbens
unter Verwendung von refluxierendem Aceton als Wärmequelle erwärmt. Nach
3 Stunden wurde die Reaktionsmischung in Eiswasser gegossen, wonach
Isobutylamin (2,0 ml, 20,1 mmol) zugegeben und die Mischung auf
einem Dampfbad erhitzt wurde. Nach einigen Stunden wurde die Reaktionsmischung
auf Umgebungstemperatur abgekühlt,
filtriert und mit Wasser gewaschen. Die wäßrige Schicht wurde mit Dichlormethan
extrahiert. Das Dichlormethanextrakt wurde mit wäßrigem Natriumhydrogencarbonat
gewaschen, mit Wasser gewaschen, über Magnesiumfiltrat getrocknet
und dann auf eine Kieselgelschicht aufgetragen. Das Kieselgel wurde
zunächst
zur Entfernung einer Verunreinigung mit Dichlormethan und dann zur
Gewinnung des Produkts mit 5% Methanol in Dichlormethan eluiert.
Das Elutionsmittel wurde bis zur Trockne auf konzentriert, was N4-(2-Methylpropyl)-3-nitro[1,5]naphthyridin-4-amin in
Form eines Feststoffs, Fp. 97-99°C,
ergab.
-
Beispiel 30
-
Verbindung der Formel
XXXIII
-
1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin
-
Teil A:
-
Eine
Lösung
von N4-(2-Methylpropyl)-3-nitro[1,5]naphthyridin-4-amin
(1,0 g, 4,1 mmol) in Essigsäureethylester
(50 ml) wurde mit einer katalytisch wirksamen Menge von 5% Platin
auf Kohle versetzt. Die Reaktionsmischung wurde in einer Parr-Apparatur vier Stunden
bei 50 psi (3,5 kg/cm2) Wasserstoff reduziert.
Die Reaktionsmischung wurde zur Entfernung des Katalysators filtriert,
wonach das Filtrat unter Vakuum auf konzentriert wurde, was N4-(2-Methylpropyl)[1,5]naphthyridin-3,4-diamin
in Form eines rohen Feststoffs ergab.
-
Teil B:
-
Der
rohe Feststoff aus Teil A wurde mit Essigsäurediethoxymethylester (2 ml)
versetzt und über
Nacht auf einem Dampfbad erhitzt. Dann wurde die Reaktionsmischung
in Dichlormethan aufgenommen, mit Wasser gewaschen, über Magnesiumsulfat
getrocknet und dann über
eine Kieselgelschicht filtriert. Das Kieselgel wurde zur Entfernung
von überschüssigem Essigsäurediethoxymethylester
mit Dichlormethan und dann zur Gewinnung des Produkts mit 5% Methanol
in Dichlormethan eluiert. Das Elutionsmittel wurde auf konzentriert, was
ein Öl
ergab, das mittels Flash-Chromatographie
(Kieselgel unter Elution mit 50% Essigsäureethylester/Hexan und dann
mit Essigsäureethylester)
gereinigt wurde, was 0,25 g 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin
in Form eines Feststoffs, Fp. 82-84°C, ergab. Analyse: berechnet
für C13H14N4:
%C, 69,00; %H, 6,24; %N, 24,76; gefunden: %C, 68,79; %H, 6,44; %N,
24,73.
-
Beispiel 31
-
Verbindung der Formel
XXXIV
-
1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
-
Eine
Lösung
von 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin (1,5 g) in Chloroform
wurde bei Umgebungstemperatur über
einen Zeitraum von 30 Minuten in kleinen Portionen mit 3-Chlorperoxybenzoesäure (3,7
g, 50%ig) versetzt. Nach 3 Stunden wurde die Reaktionsmischung mit
Chloroform verdünnt,
zweimal mit 2,0 M Natronlauge und einmal mit Wasser gewaschen, über Magnesiumsulfat
getrocknet und dann unter Vakuum auf konzentriert. Der Rückstand
wurde aus Essigsäureethylester/Hexan
umkristallisiert, was 1,2 g 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid in Form eines
Feststoffs, Fp. 183-185°C,
ergab. Analyse: berechnet für
C13H14N4O:
%C, 64, 45; %H, 5, 82; %N, 23,12; gefunden: %C, 64,15; %H, 5,92; %N,
23,02.
-
Beispiel
32 Verbindung
der Formel I 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
-
Eine
Lösung
von 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid (0,6 g)
in Dichlormethan (30 ml) wurde mit Ammoniumhydroxid (10 ml) versetzt.
Die Reaktionsmischung wurde in einem Eisbad abgekühlt und
dann mit Tosylchlorid (0,5 g) in Dichlormethan versetzt, wobei der
Ansatz schnell gerührt
wurde. Die Reaktionsmischung wurde über Nacht bei Raumtemperatur
gerührt.
Die abgeschiedene Dichlormethanschicht wurde mit wäßrigem Natriumhydrogencarbonat
gewaschen, über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert.
Der Rückstand
wurde aus Essigsäureethylester/Hexan
umkristallisiert, was 0,2 g 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin in Form eines
Feststoffs, Fp. 230-231,5°C,
ergab. Analyse: berechnet für
C13H15N5:
%C, 64,71; %H, 6,27; %N, 29,02; gefunden: %C, 64,70; %H, 6,01; %N,
29,08.
-
Beispiel
33 Verbindung
der Formel II 6,7,8,9-Tetrahydro-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
-
Eine
Lösung
von 1-(2-Methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin (0,46 g)
in Trifluoressigsäure
(10 ml) wurde mit einer katalytisch wirksamen Menge von Platinoxid
versetzt. Die Reaktionsmischung wurde in einer Parr-Apparatur unter
45 psi (3,15 kg/cm2) Wasserstoffdruck 4
Stunden reduziert. Die Reaktions mischung wurde zur Entfernung des
Katalysators abfiltriert, wonach das Filtrat unter Vakuum auf konzentriert wurde.
Der Rückstand
wurde mit wäßrigem Natriumhydrogencarbonat
vereinigt und dann mit etwas 10%iger Natronlauge versetzt. Der erhaltene
Niederschlag wurde mit Dichlormethan extrahiert. Das Dichlormethanextrakt
wurde über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert.
Der Rückstand
wurde mittels Flash-Chromatographie (Kieselgel unter Elution mit
5% Methanol in Dichlormethan mit 0,5% Ammoniumhydroxid) gereinigt.
Das Elutionsmittel wurde unter Vakuum auf konzentriert. Der Rückstand
wurde aus Essigsäureethylester
umkristallisiert, was 6,7,8,9-Tetrahydro-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]-naphthyridin-4-amin in Form eines
Feststoffs, Fp. 222-226°C,
ergab. Analyse: berechnet für
C13H19N5:
%C, 63,65; %H, 7,81; %N, 28,55; gefunden: %C, 63,07; %H, 7,51; %N,
28,00.
-
Beispiel 34
-
Verbindung der Formel
XXXIII
-
2-Methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin
-
Teil A:
-
Eine
Lösung
von N4-(2-Methylpropyl)-3-nitro[1,5]naphthyridin-4-amin
(4,0 g, 16,2 mmol) in Essigsäureethylester
(250 ml) wurde mit Magnesiumsulfat (3 g) und einer katalytisch wirksamen
Menge von 5% Platin auf Kohle versetzt. Die Reaktionsmischung wurde
in einer Parr-Apparatur 4 Stunden bei 50 psi (3,5 kg/cm2) Wasserstoff
reduziert. Die Reaktionsmischung wurde zur Entfernung des Katalysators
filtriert, wonach das Filtrat unter Vakuum auf konzentriert wurde,
was N4-(2-Methylpropyl)[1,5]naphthyridin-3,4-diamin
in Form eines rohen Feststoffs ergab.
-
Teil B:
-
Der
rohe Feststoff aus Teil A wurde in Essigsäure aufgenommen, mit Essigsäureanhydrid
vereinigt und dann über
Nacht unter Rückfluß erhitzt.
Die Reaktionsmischung wurde unter Vakuum auf konzentriert. Der erhaltene
Rückstand
wurde zur Zersetzung von überschüssigem Essigsäureanhydrid
mit Methanol vereinigt und unter Vakuum auf konzentriert. Der erhaltene
Rückstand
wurde zur Entfernung der Essigsäure
mit Cyclohexan vereinigt und dann unter Vakuum auf konzentriert.
Der erhaltene Rückstand
wurde aus Hexangemisch umkristallisiert, was 2,2 g 2-Methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin
in Form von gebrochen weißen
Nadeln, Fp. 118-119°C,
ergab. Analyse: berechnet für
C14H16N4:
%C, 69,97; %H, 6,71; %N, 23,31; gefunden: %C, 69,24; %H, 6,67; %N,
23,23.
-
Beispiel 35
-
Verbindung der Formel
XXXIV
-
2-Methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
-
Eine
Lösung
von 2-Methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin (2,1
g, 8,7 mmol) in Chloroform wurde bei Umgebungstemperatur über einen
Zeitraum von 30 Minuten in kleinen Portionen mit 3-Chlorperoxybenzoesäure (4,5
g, 50%ig, 13,1 mmol) versetzt. Nach 3 Stunden wurde die Reaktionsmischung mit
Chloroform verdünnt,
zweimal mit 2,0 M Natronlauge, einmal mit Wasser und einmal mit
Kochsalzlösung gewaschen, über Magnesiumsulfat
getrocknet und dann unter Vakuum auf konzentriert. Der Rückstand
wurde mittels Flash-Chromatographie (Kieselgel unter Elution mit
5% Methanol in Dichlormethan) gereinigt, was 2-Methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
in Form eines Feststoffs, Fp. 228-230 °C, ergab. Analyse: berechnet
für C14H16N4O:
%C, 65,61; %H, 6,29; %N, 21,86; gefunden: %C, 65,73; %H, 6,31; %N,
21,95.
-
Beispiel
36 Verbindung
der Formel I 2-Methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
-
Eine
Lösung
von 2-Methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
(1,1 g, 4,29 mmol) in Dichlormethan (50 ml) wurde mit Ammoniumhydroxid
(10 ml) versetzt. Die Reaktionsmischung wurde in einem Eisbad abgekühlt und
dann mit Tosylchlorid (0,82 g, 4,29 mmol) in Dichlormethan versetzt.
Der Ansatz wurde unter kräftigem
Rühren
auf etwa 30°C
erwärmt.
Dann wurde die Reaktionsmischung über Nacht bei Umgebungstemperatur
gerührt.
Die Dichlormethanschicht wurde abgetrennt, mit 10%iger Natronlauge,
Wasser und Kochsalzlösung
gewaschen, über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert. Der
Rückstand
wurde aus Essigsäureethylester
umkristallisiert, was 0,8 g 2-Methyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
in Form eines Feststoffs, Fp. 228-230°C,
ergab. Analyse: berechnet für C14H17N5:
%C, 65,86; %H, 6,71; %N, 27,43; gefunden: %C, 65,65; %H, 6,69; %N,
27,59.
-
Beispiel 37
-
Verbindung der Formel
XXXIII
-
2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin
-
Teil A:
-
Eine
Lösung
von N4-(2-Methylpropyl)-3-nitro[1,5]naphthyridin-4-amin
(3,0 g, 12,2 mmol) in Essigsäureethylester
(150 ml) wurde mit Magnesiumsulfat (3 g) und einer katalytisch wirksamen
Menge von 5% Platin auf Kohle versetzt. Die Reaktionsmischung wurde
in einer Parr-Apparatur vier Stunden bei 50 psi (3,5 kg/cm2) reduziert. Die Reaktionsmischung wurde
zur Entfernung des Katalysators filtriert, wonach das Filtrat unter
Vakuum auf konzentriert wurde, was N4-(2-Methylpropyl)[1,5]naphthyridin-3,4-diamin
in Form eines rohen Feststoffs ergab.
-
Teil B:
-
Der
rohe Feststoff aus Teil A wurde in Acetonitril aufgenommen und dann
mit Valerylchlorid (1,5 ml, 12,2 mmol) vereinigt. Die Mischung wurde
30 Minuten bei Umgebungstemperatur gerührt. Der erhaltene Niederschlag
wurde abfiltriert, mit etwas Acetonitril gewaschen und an der Luft
getrocknet, was 2,75 g N-(4-(2-Methylpropylamino)[1,5]naphthyridin-3-yl)valeramidhydrochlorid
in Form eines Feststoffs ergab.
-
Teil C:
-
Der
Feststoff aus Teil B wurde in Essigsäure suspendiert und über Nacht
unter Rückfluß erhitzt.
Der nach Auf konzentrieren der Reaktionsmischung unter Vakuum verbleibende
Rückstand
wurde zwischen Dichlormethan und wäßrigem Natriumhydrogencarbonat
verteilt. Die Dichlormethanschicht wurde abgetrennt, über Magnesiumsulfat
getrocknet und unter Vakuum auf konzentriert, was 2,3 g 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin
in Form eines Öls
ergab.
-
Beispiel 38
-
Verbindung der Formel
XXXIV
-
2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
-
Eine
Lösung
von 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin (2,3
g, 10,2 mmol) in Chloroform wurde bei Umgebungstemperatur über einen
Zeitraum von 30 Minuten in kleinen Portionen mit 3-Chlorperoxybenzoesäure (5,3
g, 50%ig, 15,2 mmol) versetzt. Nach 3 Stunden wurde die Reaktionsmischung mit
Chloroform verdünnt,
zweimal mit 2,0 M Natronlauge, einmal mit Wasser und einmal mit
Kochsalzlösung gewaschen, über Magnesiumsulfat
getrocknet und dann unter Vakuum auf konzentriert. Der Rückstand
wurde mit Flash-Chromatographie (Kieselgel unter Elution mit 5%
Methanol in Dichlormethan) gereinigt, was 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid ergab. Analyse:
berechnet für
C17H22N4O: %C,
68,43; %H, 7,43; %N, 18,78; gefunden: %C, 67,67; %H, 6,73; %N, 18,13.
-
Beispiel
39 Verbindung
der Formel I 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
-
Eine
Lösung
von 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
(2,0 g, 6,7 mmol) in Dichlormethan (100 ml) wurde mit Ammoninumhydroxid
(25 ml) versetzt. Die Reaktionsmischung wurde in einem Eisbad abgekühlt und
dann mit Tosylchlorid (1,3 g, 6,7 mmol) in Dichlormethan versetzt.
Der Ansatz wurde unter kräftigem
Rühren
auf etwa 30°C
erwärmt.
Dann wurde die Reaktionsmischung über Nacht bei Umgebungstemperatur
gerührt.
Die Dichlormethanschicht wurde abgetrennt, mit 10%iger Natronlauge, Wasser
und Kochsalzlösung
gewaschen, über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert.
Der Rückstand
wurde aus Hexan umkristallisiert, was 1,55 g 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
in Form eines Feststoffs, Fp. 115-116°C, ergab. Analyse: berechnet
für C17H23N5:
%C, 68,66; %H, 7,80; %N, 23,55; gefunden: %C, 69,52; %H, 7,72; %N,
21,72.
-
Beispiel
40 Verbindung
der Formel II 6,7,8,9-Tetrahydro-2-butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
-
Eine
Lösung
von 2-Butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
(0,5 g) in Trifluouressigsäure
(15 ml) wurde mit einer katalytisch wirksamen Menge von Platinoxid
versetzt. Die Reaktionsmischung wurde in einer Parr-Apparatur über Nacht
unter 50 psi (3,5 kg/cm2) Wasserstoffdruck
reduziert. Die Reaktionsmischung wurde zur Entfernung des Katalysators
filtriert, wonach das Filtrat unter Vakuum auf konzentriert wurde.
Der Rückstand
wurde mit wäßrigem Natriumhydrogencarbonat
vereinigt und dann mit etwas 10%iger Natronlauge versetzt. Der erhaltene
Niederschlag wurde mit Dichlormethan extrahiert. Das Dichlormethanextrakt
wurde über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert.
Der Rückstand
wurde mittels Flash-Chromatographie (Kieselgel unter Elution mit
1-5% Methanol in Dichlormethan mit 0,5% Ammoniumhydroxid) gereinigt.
Das Elutionsmittel wurde unter Vakuum auf konzentriert. Der Rückstand
wurde aus Hexan/Essigsäureethylester
umkristallisiert, was 6,7,8,9-Tetrahydro-2-butyl-1-(2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
in Form eines Feststoffs, Fp. 143-147°C, ergab. Analyse: berechnet
für C17H27N5:
%C, 67,74; %H, 9,03; %N, 23,23; gefunden: %C, 61,90; %H, 7,51; %N,
19,91.
-
Beispiel 41
-
Verbindung der Formel
XXXI
-
N-{4-[(3-Nitro[1,5]naphthyridin-4-yl)amino]butyl}carbamidsäure-1,1-dimethylethylester
-
Phosphoroxidchlorid
(4 ml, 0,31 mol) wurde unter Kühlen
in einem Eisbad mit N,N-Dimethylformamid (100 ml) vereinigt. Die
erhaltene Mischung wurde zu einer Lösung von 3-Nitro[1,5]naphthyridin-4-ol
(50 g, 0,26 mol) in N,N-Dimethylformamid (500 ml) gegeben. Die Reaktionsmischung
wurde 6 Stunden bei Umgebungstemperatur gerührt. Dann wurde die Reaktionsmischung
in Eiswasser gegossen und danach mit Dichlormethan (1800 ml) extrahiert.
Die organische Schicht wurde abgetrennt und dann mit Triethylamin
(45 ml) vereinigt. Nach Zusatz von N-(4-Aminobutyl)carbamidsäure-tert.-butylester wurde
die Reaktionsmischung über
Nacht gerührt.
Der nach Auf konzentrieren der Reaktionsmischung unter Vakuum verbleibende
Rückstand
wurde mit Wasser (1500 ml) behandelt. Der erhaltene Feststoff wurde
abfiltriert, mit Wasser gewaschen und getrocknet, was 76 g N-{4-[(3-Nitro[1,5]naphthyridin-4-yl)amino]butyl}carbamidsäure-1,1-dimethylethylester
in Form eines Feststoffs ergab. Eine kleine Probe wurde aus Isopropylalkohol
umkristallisiert, was eine reine Probe, Fp. 137-138°C, ergab.
Analyse: berechnet für
C17H23N5O4: %C, 56,50; %H, 6,41; %N, 19,38; gefunden:
%C, 56,26; %H, 6,30; %N, 19,53.
-
Beispiel 42
-
Verbindung der Formel
XXXII
-
N-{4-[(3-Amino[1,5]naphthyridin-4-yl)amino]butyl}carbamidsäure-1,1-dimethylethylester
-
N-{4-[(3-Nitro[1,5]naphthyridin-4-yl)amino]butyl}-carbamidsäure-1,1-dimethylethylester
(42,7 g, 0,12 mol), Platin auf Kohle (2 g) und Essigsäureethylester
(500 ml) wurden vereinigt und dann in einer Parr-Apparatur 1 Stunde bei 30 psi (2,1 kg/cm2) Wasserstoffdruck hydriert. Der Katalysator
wurde abfiltriert und mit Essigsäureethylester
gewaschen. Das Filtrat wurde unter Vakuum auf konzentriert, was
N-{4-[(3-Amino[1,5]naphthyridin-4-yl)amino]butyl}-carbamidsäure-1,1-dimethylethylester
in Form eines leuchtend gelborangen Feststoffs ergab.
-
Beispiel 43
-
Verbindung der Formel
XXXIII
-
N-[4-(2-Butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäure-1,1-dimethylethylester
-
Eine
Mischung aus N-{4-[(3-Amino[1,5]naphthyridin-4-yl)amino]butyl}carbamidsäure-1,1-dimethylethylester
(39 g, 0,12 mol) in warmem Xylol (500 ml) wurde mit frisch destilliertem
Orthovaleriansäuretrimethylester
(41 ml, 0,24 mol) versetzt. Die Reaktionsmischung wurde über Nacht
unter Rückfluß erhitzt.
Danach war gemäß Dünnschichtchromatographie
noch mindestens die Hälfte
des Edukts vorhanden. Dann wurde p-Toluolsulfonsäureanhydrid-monohydrat (6 g)
zugegeben.
-
Nach
kurzer Zeit war die Reaktion gemäß Dünnschichtchromatographie
vollständig.
Die Reaktionsmischung wurde auf Umgebungstemperatur abkühlen gelassen
und dann mit Essigsäureethylester
verdünnt
und mit wäßrigem Natriumhydrogencarbonat
gewaschen. Die organische Schicht wurde unter Vakuum auf konzentriert,
was einen öligen
Rückstand
ergab. Der Rückstand
wurde mit Hexan trituriert, was einen dunkelrosa Feststoff ergab.
Dieser Feststoff wurde aus Acetonitril umkristallisiert, was N-[4-(2-Butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäure-1,1-dimethylethylester
in Form eines blaßpfirsichfarbenen Feststoffs,
Fp. 96,0-98,0°C
ergab. Analyse: berechnet für
C22H31N5O2: %C, 66,47; %H, 7,86; %N, 17,62; gefunden:
%C, 66,29; %H, 7,78; %N, 17,76.
-
Beispiel 44
-
Verbindung der Formel
XXXIV
-
1-{4-[(1,1-Dimethylethylcarbonyl)amino]butyl}-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
-
Eine
Lösung
von N-[4-(2-Butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäure-1,1-dimethylethylester
in Chloroform (50 ml) wurde portionsweise mit 3-Chlorperbenzoesäure (1 Äq., 57%ig)
versetzt. Die Reaktionsmischung wurde 2 Stunden bei Umgebungstemperatur
rühren
gelassen, wonach gemäß Dünnschichtchromatographie
kein Edukt mehr vorhanden war. Die Reaktionsmischung wurde mit Dichlormethan verdünnt und
dann zweimal mit 1 M Natronlauge gewaschen. Die organische Schicht
wurde über
wasserfreiem Magnesiumsulfat getrocknet und dann unter Vakuum auf
konzentriert, was 1-{4-[(1,1-Dimethylethylcarbonyl)amino]butyl}-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
in Form eines orangen Öls,
das beim Stehen fest wurde, ergab.
-
Beispiel
45 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäure-1,1- dimethylethylester
-
Eine
Lösung
von 1-{4-[(1,1-Dimethylethylcarbonyl)amino]butyl}-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
(19,4 g) in Chloroform wurde mit Ammoniumhydroxid (20 ml) versetzt.
Danach wurde langsam Tosylchlorid (9 g) zugegeben. Gemäß Dünnschichtchromatographie
schritt die Reaktion nur langsam voran. Es wurde zweimal zusätzliches
Tosylchlorid zugegeben. Nachdem die Reaktion gemäß Dünnschichtchromatographie vollständig war,
wurden die Schichten getrennt. Die organische Schicht wurde mit
verdünntem
wäßrigem Natriumcarbonat
gewaschen, über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert.
Der Rückstand
wurde mit Essigsäuremethylester
(10 ml) bedeckt und mit Hexan (5 ml) versetzt, wonach die Mischung über Nacht
stehengelassen wurde. Der erhaltene kristalline Feststoff wurde
abfiltriert, mit Hexan gewaschen und dann getrocknet, was 15,1 g
N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäure-1,1-dimethylethylester,
Fp. 148,5-149,5°C,
ergab. Analyse: berechnet für C22H32N6O2: %C, 64,05; %H, 7,82; %N, 20,37; gefunden:
%C, 64,15; %H, 7,82; %N, 20,55.
-
Beispiel
46 Verbindung
der Formel I 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
-
Eine
Suspension von N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäure-1,1-dimethylethylester
(13,8 g) in 1 N Salzsäure
(140 ml) wurde auf einem Dampfbad 1,5 Stunden erhitzt. Die Reaktionsmischung
wurde auf Umgebungstemperatur abkühlen gelassen und dann mit
50%iger Natronlauge basisch gestellt (pH>11). Der erhaltene Niederschlag wurde
abfiltriert, mit Wasser gewaschen und dann getrocknet, was 9,5 g
4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
in Form eines weißen
Feststoffs, Fp. 212-213°C,
ergab. Analyse: berechnet für
C17H24N6:
%C, 65,36; %H, 7,74; %N, 26,90; gefunden: %C, 65,16; %H, 7,65; %N,
27,29.
-
Beispiel
47 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-N'-phenylharnstoff
-
Unter
Stickstoffatmosphäre
wurde eine Suspension von 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,15
g, 0,48 mmol) in wasserfreiem Tetrahydrofuran (60 ml) mit Phenylisocyanat
(52 μl,
0,48 mmol) versetzt. Die Reaktionsmischung wurde 20 Minuten gerührt, wonach
sie homogen geworden war und gemäß Dünnschichtchromatographie
kein Edukt mehr vorhanden war. Nach Zugabe von Aminomethylharz (280
mg, 1% vernetzt, 100-200 mesh, von BACHEM, Torrance, Kalifornien,
USA) wurde die Reaktionsmischung 0,5 h rühren gelassen. Dann wurde Kieselgel
(0,4 g) zugegeben, wonach die Mischung unter Vakuum auf konzentriert
wurde, was einen Feststoff ergab. Der Feststoff wurde mittels Flash-Chromatographie
unter Elution mit einem Gemisch aus Dichlormethan und Methanol im
Verhältnis
95/5 gereinigt, was einen weißen
Feststoff ergab, der bei 60°C
unter Vakuum getrocknet wurde, was 0,12 g N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-N'-phenylharnstoff
ergab. Analyse: berechnet für
C24H29N7O
+ 1/5 H2O: %C, 66,25; %H, 6,81; %N, 22,53;
gefunden: %C, 66,27; %H, 6,63; %N, 22,83.
-
Beispiel
48 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-N'-cyclohexylharnstoff
-
In
Analogie zu Beispiel 47 wurde Cyclohexylisocyanat (61 μl, 0,48 mmol)
mit 4-(4-Amino-2-butyl-1H- imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
(0,15 g, 0,48 mmol) umgesetzt, was 0,14 g N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-N'-cyclohexylharnstoff in Form eines weißen Feststoffs
ergab. Analyse: berechnet für
C24H35N7O:
%C, 65, 88; %H, 8,06; %N, 22,41. 1H-NMR
(300 MHz, CDCl3) δ 8,60 (dd, J = 4,4, 1,4 Hz,
1H), 8,08 (d, J = 8,5 Hz, 1H), 7,44 (dd, J = 8,5, 4,4 Hz, 1H), 5,55
(br s, 2H), 4,92 (t, J = 5,8 Hz, 1H), 4,82 (scheinbares t, J = 7,8
Hz, 2H), 4,13 (d, J = 8,6 Hz, 1H), 3,48 (m, 1H), 3,35 (scheinbares q,
J = 6,4 Hz, 2H), 2,93 (scheinbares t, J = 7,8 Hz, 2H), 1,80-2,05
(m, 4H), 1,45-1,75 (m, 6 H), 1,2-1,4 (m, 2H), 1,0-1,2 (m, 2H), 1,03
(t, 7,4 Hz, 3H); HRMS (EI) berechnet für C24H35N7O(M+)
437,2903, gefunden 437,2903.
-
Beispiel
49 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-N'-butylharnstoff
-
In
Analogie zu Beispiel 47 wurde Butylisocyanat (54 μl, 0,48 mmol)
mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,15
g, 0,48 mmol) umgesetzt, was 0,13 g N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-N'-butylharnstoff in Form eines weißen Feststoffs
ergab. Analyse: berechnet für
C22H33N7O:
%C, 64,21; %H, 8,08; %N, 23,82; gefunden: %C, 64,05; %H, 7,97; %N, 24,00.
-
Beispiel
50 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäurephenylester
-
In
Analogie zu Beispiel 47 wurde Chlorameisensäurephenylester (61 μl, 0,48 mmol)
mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
(0,15 g, 0,48 mmol) umgesetzt, was 0,12 g N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäurephenylester
in Form eines Feststoffs ergab. Analyse: berechnet für C24H28N6O2: %C, 66,65; %H, 6,53; %N, 19,43; gefunden:
%C, 66,49; %H, 6,59; %N, 19,32.
-
Beispiel
51 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-2-furamid
-
In
Analogie zu Beispiel 47 wurde Furoylchlorid (15,8 μl, 0,16 mmol)
mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,05
g, 0,16 mmol) umgesetzt, was 0,019 g N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-2-furamid
in Form eines weißen
Feststoffs ergab. 1H-NMR (300 MHz, CDCl3) δ 8,
58 (dd, J = 4,4, 1,5 Hz, 1H), 8,06 (dd, J = 8,6 Hz, 1,6 Hz, 1H),
7, 41 (dd, J = 8,5, 4,4 Hz, 1H), 7,33 (m, 1H), 7,08 (dd, J = 3,5,
0,6 Hz, 1H), 6,84 (m, 1H), 6,47 (dd, J = 3,5, 1,7 Hz, 1H), 4,86
(scheinbares t, J = 7,7 Hz, 2H), 3,59 (scheinbares q, J = 6,5 Hz,
2H), 2,92 (scheinbares t, J = 7,8 Hz, 2 H), 1,7-2,1 (m, 6H), 1,51
(m, 2H), 1,00 (t, J = 7,3 Hz, 3H); HRMS (EI) berechnet für C22H26N6O2(M+) 406, 2117,
gefunden 406,2121.
-
Beispiel
52 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]benzamid
-
In
Analogie zu Beispiel 47 wurde Benzoylchlorid (56 μl, 0,48 mmol)
mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,15
g, 0,48 mmol) umgesetzt, was 0,11 g N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]benzamid
in Form eines weißen
Feststoffs ergab. Analyse: berechnet für C24H28N6O + ¼ H2O: %C, 68,47; %H, 6,82; %N, 19,96; gefunden:
%C, 68,24; %H, 6,76; %N, 19,90.
-
Beispiel
53 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-N'-benzylharnstoff
-
Eine
Suspension von 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,15
g, 0,48 mmol) in Tetrahydrofuran (60 ml) wurde bei Umgebungstemperatur
mit Benzylisocyanat (59 μl,
0,48 mmol) versetzt. In weniger als 30 Minuten wurde eine Lösung erhalten,
und die Dünnschichtchromatographie (Dichlormethan/Methanol
9:1) zeigte einen großen
neuen Punkt mit höherem
Rf-Wert und nur eine Spur Edukt. Nach Zugabe
von Aminomethylharz (280 mg) wurde die Reaktionsmischung 15 Minuten
gerührt.
Der nach Abziehen des Lösungsmittels
unter Vakuum verbleibende Rückstand
wurde mittels Säulenchromatographie
gereinigt, was 0,16 g N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-N'-benzylharnstoff
in Form eines weißen
Feststoffs ergab. Analyse: berechnet für C25H31N7O: %C, 67,39;
%H, 7,01; %N, 22,00; gefunden: %C, 67,43; %H, 6,92; %N, 22,02.
-
Beispiel
54 Verbindung
der Formel I N
3-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]nicotinamid
-
4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,050
g, 0,16 mmol) wurde in Tetrahydrofuran (30 ml) suspendiert. Die
Suspension wurde mit N,N-Diisopropylethylamin (28 μl, 0,16 mmol) gefolgt
von Nicotinoylchlorid-hydrochlorid (0,028 g, 0,16 mmol) versetzt.
Die Reaktionsmischung wurde 1 Stunde bei Umgebungstemperatur gerührt, wonach
eine Lösung
erhalten wurde. Die Dünnschichtchromatographie
(Dichlormethan/Methanol 9:1) zeigte einen großen neuen Punkt mit höherem Rf-Wert und nur eine Spur Edukt. Nach Zugabe
von Aminomethylharz (100 mg) wurde die Reaktionsmischung 5 Minuten
gerührt. Der
nach Abziehen des Lösungsmittels
unter Vakuum verbleibende Rückstand
wurde in Dichlormethan gelöst und
auf eine Kieselgelschicht aufgegeben. Das Kieselgel wurde zunächst mit
Dichlormethan und dann mit Dichlormethan/Methanol 9:1 eluiert. Die
reinsten Fraktionen wurden vereinigt und dann unter Vakuum auf konzentriert,
was N3-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]nicotinamid
in Form eines weißen
Pulvers ergab. 1H-NMR (300 MHz, CDCl3) δ 8,91
(m, 1H), 8,68 (d, J = 4,5 Hz, 1H), 8,45 (d, J = 4,3, 1H), 8,03 (m,
2H), 7,30-7,40 (m, 2H), 6,98 (s, 2H), 5,51 (s, 1H), 4,86 (scheinbares
t, J = 7,9 Hz, 2H), 3,66 (q, J = 6,5 Hz, 2H), 2,92 (scheinbares
t, J = 7,7 Hz, 2H), 2,05 (m, 2H), 1,75-1,95 (m, 4H), 1,51 (m, 2H), 1,00 (t,
J = 7,3 Hz, 3 H); HRMS (EI) berechnet für C23H27N7O(M+)
417,2277, gefunden 417,2276.
-
Beispiel
55 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]phenylaceatamid
-
Eine
Suspension von 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,050
g, 0,16 mmol) in Tetrahydrofuran (30 ml) wurde mit Phenylacetylchlorid
(21 μl,
0,16 mmol) versetzt. Die Reaktionsmischung wurde 1 Stunde bei Umgebungstemperatur
gerührt,
wonach eine Lösung
erhalten wurde. Die Dünnschichtchromatographie
(Dichlormethan/Methanol 9:1) zeigte einen großen neuen Fleck mit höherem Rf-Wert und nur eine Spur Edukt. Nach Zugabe
von Aminomethylharz (100 mg) wurde die Reaktionsmischung 5 Minuten
gerührt.
Das Lösungsmittel
wurde unter Vakuum abgezogen, was ein weißes Pulver ergab. Diese Substanz
wurde auf eine kurze Kieselgelsäule
aufgegeben und gereinigt, wobei zunächst mit Dichlormethan und
dann mit Dichlormethan/Methanol 9:1 eluiert wurde. Die reinsten
Fraktionen wurden vereinigt und dann unter Vakuum aufkonzentriert,
was ein farbloses Öl
ergab. Das Öl
wurde in Dichlormethan gelöst
und gerade bis zum Trübwerden
der Lösung
mit Hexan versetzt, wonach das Lösungsmittel
abgezogen wurde, was N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]phenylacetamid
in Form eines weißen Pulvers
ergab. Analyse: berechnet für
C25H30N6O2: %C, 67,24; %H, 6,77; %N, 18,82; gefunden:
%C, 67,52; %H, 6,85; %N, 18,38. 1H-NMR (300 MHz, CDCl3) δ 8,51
(dd, J = 4,4, 1,5 Hz, 1H), 8,11 (dd, J = 8,4, 1,4 Hz, 1H), 7,43
(dd, J = 8,4, 4,4 Hz, 1H), 7,10-7,20 (m, 5H), 6,30 (br s, 2H), 5,83
(m, 1H), 4,72 (scheinbares t, J = 7,8 Hz, 2H), 3,54 (s, 2H), 3,35
(scheinbares q, J = 6,5 Hz, 2H), 2,88 (scheinbares t, J = 7,8 Hz,
2H), 1,80-1,90 (m, 4H), 1,45-1,65 (m, 4H), 1,00 (t, J = 7,3 Hz,
3H); HRMS (EI) berechnet für
C25H30N6O(M+) 430, 2481, gefunden 430,2490.
-
Beispiel
56 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäurebenzylester
-
In
Analogie zu Beispiel 55 wurde Chlorameisensäurebenzylester (83 μl, 0,58 mmol)
mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
(0,15 g, 0,48 mmol) versetzt, was 0,18 g N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäurebenzylester
in Form eines weißen
Pulvers ergab.
-
Beispiel
57 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäure-9H-9-fluorenylmethylester
-
In
Analogie zu Beispiel 55 wurde Chlorameisensäure-9-fluorenylmethylester (0,085 g, 0,33
mmol) mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,105
g, 0,33 mmol) umgesetzt, was 0,125 g N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäure-9H-9-fluorenylmethylester
in Form eines weißen
Pulvers ergab. Analyse: berechnet für C32H34N6O2 + ¼ H2O: %C, 71,29; %H, 6,45; %N, 15,59; gefunden:
%C, 70,99; %H, 6,35; %N, 15,55.
-
Beispiel
58 Verbindung
der Formel I N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäureethylester
-
In
Analogie zu Beispiel 55 wurde Chlorameisensäureethylester (46 μl, 0,48 mmol)
mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
(0,15 g, 0,48 mmol) umgesetzt, was 0,15 g N-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäureethylester
in Form eines weißen
Pulvers ergab. Analyse: berechnet für C20H28N6O2:
%C, 62,48; %H, 7,34; %N, 21,86; gefunden: %C, 61,73; %H, 7,28; %N,
21,62.
-
Beispiel 59
-
Verbindung der Formel
XXXI
-
1,1-Dimethyl-2-[(3-nitro[1,5]naphthyridin-4-yl)amino]ethanol
-
Phosphoroxidchlorid
(4 ml, 43 mmol) wurde unter Kühlung
in einem Eisbad mit N,N-Dimethylformamid (15 ml) umgesetzt. Diese
Mischung wurde zu einer Lösung
von 3-Nitro[1,5]naphthyridin-4-ol
(6,9 g, 36,1 mmol) in N,N-Dimethylformamid
(60 ml) gegeben. Die Reaktionsmischung wurde in einem Ölbad auf
60°C erwärmt. Nach
3 Stunden wurde die Reaktionsmischung in Eiswasser gegossen. Der
erhaltene Niederschlag wurde abfiltriert und dann mit Wasser gewaschen.
Das feuchte rohe 5-Chlor-3-nitro [1,5]naphthyridin wurde in Dichlormethan
(150 ml) suspendiert. Nach Zugabe von Diisopropylethylamin wurde
langsam mit Hydroxyisobutylamin (3,4 g, 40 mmol) versetzt. Die Reaktionsmischung
wurde 2 Stunden unter Rückfluß erhitzt
und dann mit Wasser (100 ml) vereinigt. Der erhaltene Niederschlag
wurde abfiltriert, was 7,2 g 1,1-Dimethyl-2-[(3-nitro[1,5]naphthyridin-4-yl)amino]ethanol
ergab. Eine kleine Probe wurde aus Isopropanol umkristallisiert,
was eine reine Probe, Fp. 184,5-186°C ergab. Analyse: berechnet
für C12H14N4O3: %C, 54,96; %H, 5,38; %N, 21,36; gefunden:
%C, 54,63; %H, 5,36; %N, 21,51.
-
Beispiel 60
-
Verbindung der Formel
XXXIII
-
1,1-Dimethyl-2-(2-butyl[1,5]naphthyridin-1-yl)ethanol
-
Teil A
-
Eine
Suspension von 1,1-Dimethyl-2-[(3-nitro[1,5]naphthyridin-4-yl)amino)ethanol
(7 g, 26 mmol) in Isopropanol (300 ml) wurde mit einer katalytisch
wirksamen Menge von 5% Platin auf Kohle versetzt. Die Mischung wurde
in einer Parr-Apparatur 3 Stunden bei 50 psi (3,5 kg/cm2)
Wasserstoffdruck hydriert. Die Reaktionsmischung wurde zur Entfernung
des Katalysators filtriert. Das Filtrat wurde unter Vakuum auf konzentriert. Der
Rückstand
wurde mit Toluol versetzt, wonach die Mischung zur Entfernung des
gesamten Alkohols unter Vakuum auf konzentriert wurde, was rohes
1,1-Dimethyl-2-[(3-amino[1,5]naphthyridin-4-yl)amino]ethanol ergab.
-
Teil B
-
Eine
Suspension von 1,1-Dimethyl-2-[(3-amino[1,5]naphthyridin-4-yl)amino]ethanol
(3,5 g, 13 mmol) in Xylol (100 ml) wurde mit Orthovaleriansäuretrimethylester
(3,6 ml, 20 mmol) versetzt. Die Reaktionsmischung wurde 2 Tage unter
Rückfluß erhitzt.
Dann wurde die Mischung mit methanolischem Ammonik verdünnt, in
einen Parr-Behälter
eingebracht und dann 4 Stunden auf 110°C erhitzt. Der nach Auf konzentrieren der
Reaktionsmischung unter Vakuum verbleibende Rückstand wurde zwischen Dichlormethan
und Wasser verteilt. Die Schichten wurden getrennt. Die organische
Schicht wurde mit Wasser gewaschen, über Magnesiumsulfat getrocknet
und dann unter Vakuum aufkonzentriert, was ein Öl ergab. Das Öl wurde
aus Essigsäuremethylester/Benzol
umkristallisiert, was 2,8 g 1,1-Dimethyl-2-(2-butyl[1,5]naphthyridin-1-yl)ethanol
in Form eines Feststoffs, Fp. 85-88,5°C, ergab. Analyse: berechnet
für C17H22N4O:
%C, 68,43; %H, 7,43; %N, 18,78; gefunden: %C, 68,04; %H, 7,18; %N,
19,09.
-
Beispiel 61
-
Verbindung der Formel
XXXIV
-
2-Butyl-1-(2-hydroxy-2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
-
Eine
Lösung
von 1,1-Dimethyl-2-(2-butyl[1,5]naphthyridin-1-yl)ethanol
(2,6 g, 8,7 mmol) in Chloroform (50 ml) wurde in einem mit Aluminiumfolie
bedeckten Kolben in 3 Portionen mit 3-Chlorperbenzoesäure (2,6 g, 9,5 mmol) versetzt.
Die Reaktionsmischung wurde 4 Stunden bei Umgebungstemperatur gewaschen
und dann zweimal mit verdünntem
wäßrigem Natriumhydrogencarbonat
und Kochsalzlösung
gewaschen, über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert.
Der Rückstand
wurde aus Essigsäuremethylester
umkristallisiert, was 2,25 g 2-Butyl-1-(2-hydroxy-2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid, Fp. 156-158°C ergab.
Analyse: berechnet für
C17H22N4O2 + ¼ H2O: %C, 64,03; %H, 7,11; %N, 17,57; gefunden:
%C, 63,96; %H, 6,84; %N, 17,71.
-
Beispiel
62 Verbindung
der Formel I 1,1-Dimethyl-2-(4-amino-2-butyl[1,5]naphthyridin-1-yl)ethanol
-
Eine
Lösung
von 2-Butyl-1-(2-hydroxy-2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid (1,9
g, 6,0 mmol) in Dichlormethan (40 ml) wurde mit Ammoniumhydroxid
(15 ml) versetzt. Dann wurde langsam Tosylchlorid (1,2 g, 6,4 mmol)
zugegeben. Die Reaktion schritt gemäß Dünnschichtchromatographie nur langsam
voran. Es wurde zweimal zusätzliches
Tosylchlorid zugegeben. Nachdem die Reaktion gemäß Dünnschichtchromatographie vollständig war,
wurden die Schichten getrennt. Die organische Schicht wurde mit
verdünntem
wäßrigem Natriumcarbonat
gewaschen, über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert.
Der Rückstand
wurde mit Essigsäuremethylester
(10 ml) bedeckt und mit Hexan (5 ml) versetzt, wonach die Mischung über Nacht
stehengelassen wurde. Der erhaltene kristalline Feststoff wurde
abfiltriert, was 0,9 g 1,1-Dimethyl-2-(4-amino-2-butyl[1,5]naphthyridin-1-yl)ethanol,
Fp. 177-179°C,
ergab. Analyse: berechnet für
C17H23N5O:
%C, 65,15; %H, 7,40; %N, 22,35; gefunden: %C, 64,97; %H, 7,33; %N,
22,71.
-
Beispiel 63
-
Verbindung der Formel
XXXIII
-
1,1-Dimethyl-2-(2-phenylmethyl[1,5]naphthyridin-1-yl)ethanol
-
Teil A
-
Eine
Suspension von 1,1-Dimethyl-2-[(3-amino[1,5]naphthyridin-4-yl)amino]ethanol
(3,5 g, 13 mmol) in Dichlormethan (100 ml) wurde mit Phenylacetylchlorid
(2,0 ml, 20 mmol) versetzt. Die Reaktionsmischung wurde unter Rückfluß erhitzt,
bis die Reaktion gemäß Dünnschichtchromatographie
vollständig
war. Die Reaktionsmischung wurde im nächsten Schritt eingesetzt.
-
Teil B
-
Das
Material aus Teil A wurde mit 7% Ammoniak in Methanol (100 ml) vereinigt,
in einen verschlossenen Behälter
eingebracht und dann 6 Stunden auf 150°C erhitzt. Der nach Auf konzentrieren
der Reaktionsmischung unter Vakuum verbleibende Rückstand
wurde mit Wasser (100 ml) vereinigt und dann mit Dichlormethan (2 × 75 ml)
extrahiert. Die Extrakte wurden vereinigt, mit Wasser (100 ml) gewaschen, über Magnesiumsulfat
getrocknet und dann unter Vakuum aufkonzentriert. Der Rückstand
wurde aus Essigsäuremethylester umkristallisiert,
was 2,1 g 1,1-Dimethyl-2-(2-phenylmethyl[1,5]naphthyridin-1-yl)ethanol
in Form eines Feststoffs, Fp. 150-152°C, ergab. Analyse: berechnet
für C20H20N4O:
%C, 72,27; %H, 6,06; %N, 16,85; gefunden: %C, 72,11; %H, 6,01; %N,
17,00.
-
Beispiel 64
-
Verbindung der Formel
XXXIV
-
2-Phenylmethyl-1-(2-hydroxy-2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
-
Eine
Lösung
von 1,1-Dimethyl-2-(2-phenylmethyl[1,5]naphthyridin-1-yl)ethanol
(2 g, 6 mmol) in Chloroform (50 ml) wurde in einem mit Aluminiumfolie
bedeckten Kolben in 3 Portionen mit 3-Chlorperbenzoesäure (1,8 g, 6,6 mmol) versetzt.
Die Reaktionsmischung wurde über
Nacht bei Umgebungstemperatur gerührt und dann zweimal mit verdünntem wäßrigem Natriumhydrogencarbonat
und Kochsalzlösung
gewaschen, über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert.
Der Rückstand
wurde aus Isopropanol umkristallisiert, was 2,25 g 2-Phenylmethyl-1-(2-hydroxy-2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid,
Fp. 204-206°C,
ergab. Analyse: berechnet für
C20H20N4O2 + ½ H2O: %C, 67,21; %H, 5,92; %N, 15,68; gefunden:
%C, 67,05; %H, 5,65; %N, 15,39.
-
Beispiel
65 Verbindung
der Formel I 1,1-Dimethyl-2-(4-amino-2-phenylmethyl[1,5]naphthyridin-1-yl)ethanol
-
Eine
Lösung
von 2-Phenylmethyl-1-(2-hydroxy-2-methylpropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid (1,5 g, 4,3
mmol) in Dichlormethan (40 ml) wurde mit Ammoniumhydroxid (10 ml)
versetzt. Dann wurde langsam Tosylchlorid (0,8 g, 4,3 mmol) zugegeben.
Die Reaktion schritt gemäß Dünnschichtchromatographie
nur langsam voran. Es wurde zweimal zusätzliches Tosylchlorid zugegeben.
Nachdem die Reaktion gemäß Dünnschichtchromatographie
vollständig
war, wurden die Schichten getrennt. Die organische Schicht wurde
mit verdünntem
wäßrigem Natriumcarbonat
gewaschen, über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert.
Der Rückstand
wurde mit Essigsäuremethylester
(10 ml) bedeckt und mit Hexan (5 ml) versetzt, wonach die Mischung über Nacht
stehengelassen wurde. Der erhaltene kristalline Feststoff wurde
abfiltriert, was 1,1-Dimethyl-2-(4-amino-2-phenylmethyl[1,5]naphthyridin-1-yl)ethanol,
Fp. 211-213°C, ergab.
Analyse: berechnet für
C20H21N5O:
%C, 69,14; 5H, 6,09; %N, 20,16; gefunden: %C, 69,10; %H, 6,12; %N,
20,48.
-
Beispiel 66
-
Verbindung der Formel
XXXI
-
N-Phenylmethyl-3-nitro[1,5]naphthyridin-4-amin
-
Phosphoroxidchlorid
(3,5 ml, 37,7 mmol) wurde unter Kühlung in einem Eisbad mit N,N-Dimethylformamid
(15 ml) umgesetzt. Diese Mischung wurde zu einer Lösung von
3-Nitro[1,5]naphthyridin-4-ol (6,0 g, 31,4 mmol) in N,N-Dimethylformamid
(60 ml) gegeben. Die Reaktionsmischung wurde in einem Ölbad auf 60°C erwärmt. Nach
3 Stunden wurde die Reaktionsmischung in Eiswasser gegossen. Der
erhaltene Niederschlag wurde abfiltriert und dann mit Wasser gewaschen.
Das feuchte rohe 5-Chlor-3-nitro[1,5]naphthyridin wurde in Dichlormethan
(150 ml) suspendiert. Nach Zugabe von Diisopropylethylamin (1,2 Äq.) wurde
langsam mit Benzylamin (4,7 ml, 40 mmol) versetzt. Die Reaktionsmischung
wurde 2 Stunden unter Rückfluß erhitzt und
dann mit Wasser (100 ml) vereinigt. Nach Trennung der Schichten
wurde die organische Schicht unter Vakuum auf konzentriert, was
5,5 g N-Phenylmethyl-3-nitro[1,5]naphthyridin-4-amin
ergab. Eine kleine Probe wurde aus Isopropanol umkristallisiert,
was eine reine Probe, Fp. 127-129°C,
ergab. Analyse: berechnet für C15H12N4O2: %C, 64,28; %H, 4,32; %N, 19,99; gefunden:
%C, 63,89; %H, 4,40; %N, 20,35.
-
Beispiel 67
-
N-(4-Phenylmethylamino[1,5]naphthyridin-3-yl)ethoxyacetamid-hydrochlorid
-
Eine
Suspension von N-Phenylmethyl-3-nitro[1,5]naphthyridin-4-amin
(5,1 g, 18,2 mmol) in Toluol (300 ml) wurde mit einer katalytisch
wirksamen Menge von Platin auf Kohle versetzt. Die Reaktionsmischung
wurde in einer Parr-Apparatur 1 Stunde unter einem Wasserstoffdruck
von 50 psi (3,5 kg/cm2) hydriert. Die Reaktionsmischung
wurde zur Entfernung des Katalysators abfiltriert. Das Filtrat wurde
unter Vakuum auf ein Volumen von etwa 200 ml auf konzentriert und
dann mit Ethoxyacetylchlorid (2,5 g, 20 mmol) umgesetzt. Der erhaltene
gelbe Niederschlag wurde abfiltriert, in Diethylether suspendiert
und dann abfiltriert, was 5,8 g N-(4-Phenylmethylamino[1,5]naphthyridin-3-yl)ethoxyacetamid-hydrochlorid,
Fp. 205-212°C,
ergab. Analyse: berechnet für
C19H20N4O2 HCl: %C, 61,21; %H, 5,68; %N, 15,03; gefunden:
%C, 60,90; %H, 5,38; %N, 15,38.
-
Beispiel 68
-
Verbindung der Formel
XXXIII
-
2-Ethoxymethyl-1-phenylmethyl-1H-imidazo[4,5-c][1,5]naphthyridin
-
N-(4-Phenylmethylamino[1,5]naphthyridin-3-yl)ethoxyacetamid-hydrochlorid
(5,8 g, 15,5 mmol) wurde mit einer 7%igen Lösung von Ammonik in Methanol
(100 ml) vereinigt, in einen verschlossenen Parr-Behälter eingebracht
und dann 6 Stunden auf 150°C
erhitzt. Der nach Auf konzentrieren der Reaktionsmischung unter Vakuum
verbleibende Rückstand
wurde zwischen Wasser und Dichlormethan verteilt. Die Dichlormethanschicht
wurde abgetrennt, mit Wasser gewaschen, über Magnesiumsulfat getrocknet
und dann unter Vakuum auf konzentriert. Der Rückstand wurde aus Essigsäuremethylester
umkristallisiert, was 4,3 g 2-Ethoxymethyl-1-phenylmethyl-1H-imidazo[4,5-c][1,5]naphthyridin,
Fp. 118-119°C,
ergab. Analyse: berechnet für C19H18N4O:
%C, 71,68; %H, 5,70; %N, 17,60; gefunden: %C, 71,44; %H, 5,60; %N,
17,66.
-
Beispiel 69
-
Verbindung der Formel
XXXIV
-
2-Ethoxymethyl-1-phenylmethyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
-
Eine
Lösung
von 2-Ethoxymethyl-1-phenylmethyl-1H-imidazo[4,5-c][1,5]naphthyridin (3,9
g, 12,2 mmol) in Chloroform (100 ml) wurde in einem mit Aluminiumfolie
bedeckten Kolben in 3 Portionen mit 3-Chlorperbenzoesäure (3,7 g, 13,4 mmol) versetzt.
Die Reaktionsmischung wurde über
Nacht bei Umgebungstemperatur gerührt und dann zweimal mit verdünntem wäßrigem Natriumhydrogencarbonat
und einmal mit Kochsalzlösung
gewaschen. Die Chloroformschicht wurde in zwei Portionen aufgeteilt.
Eine Portion wurde im nachstehenden Beispiel verwendet. Die zweite
Portion wurde unter Vakuum auf konzentriert. Der Rückstand
wurde aus Isopropylalkohol umkristallisiert, was 2-Ethoxymethyl-1-phenylmethyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
in Form eines Feststoffs, Fp. 187,5-189°C,
ergab. Analyse: berechnet für
C19H18N4O2 + ¼ H2O: %C, 67,52; %H, 5,49; %N, 16,58; gefunden:
%C, 67,56; %H, 5,36; %N, 16,77.
-
Beispiel
70 Verbindung
der Formel I 2-Ethoxymethyl-1-phenylmethyl-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
-
Die
Chloroformlösung
von 2-Ethoxymethyl-1-phenylmethyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
aus dem obigen Beispiel wurde mit Ammoniumhydroxid (20 ml) versetzt.
Dann wurde langsam Tosylchlorid zugegeben. Die Reaktion schritt
gemäß Dünnschichtchromatographie
nur langsam voran. Es wurde zweimal zusätzliches Tosylchlorid zugegeben.
Nachdem die Reaktion gemäß Dünnschichtchromatographie vollständig war,
wurden die Schichten getrennt. Die organische Schicht wurde mit
verdünntem
wäßrigem Natriumcarbonat
gewaschen, über
Magnesiumsulfat getrocknet und dann unter Vakuum auf konzentriert.
Der Rückstand
wurde mit Essigsäuremethylester
(10 ml) bedeckt und mit Hexan (5 ml) versetzt, wonach die Mischung über Nacht
stehengelassen wurde. Der erhaltene kristalline Feststoff wurde
abfiltriert, was 2-Ethoxymethyl-1-phenylmethyl-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin,
Fp. 173-174°C,
ergab. Analyse: berechnet für
C19H19N5O:
%C, 68,45; %H, 5,74; %N, 21,01; gefunden: %C, 68,35; %H, 5,83; %N,
21,27.
-
Beispiel 71
-
Verbindung der Formel
XXXI
-
N4-(3-Isopropoxypropyl)-3-nitro[1,5]naphthyridin-4-amin
-
Teil A
-
Phosphoroxidchlorid
(3,4 ml, 30 mmol) wurde zu auf einem Eisbad gekühltem N,N-Dimethylformamid (15
ml) gegeben. Die erhaltene Lösung
wurde zu einer Lösung
von 3-Nitro[1,5]naphthyridin-4-ol (5,73 g, 30 mmol) in N,N-Dimethylformamid
(35 ml) getropft. Die Reaktionsmischung wurde 5 Stunden bei Umgebungstemperatur
gehalten und dann auf Eis gegossen. Der erhaltene gelbe Niederschlag
wurde abfiltriert und dann zwischen Dichlormethan (200 ml) und Wasser
(150 ml) verteilt. Die organische Schicht wurde abgetrennt, über Magnesiumsulfat
getrocknet, filtriert und dann unter Vakuum auf konzentriert, was
4,2 g rohes 4-Chlor-3-nitro[1,5]naphthyridin
ergab.
-
Teil B
-
4-Chlor-3-nitro[1,5]naphthyridin
(4,1 g), Dichlormethan (150 ml), Triethylamin (4,1 ml, 29,5 mmol)
und 3- Isopropoxypropylamin
(3,3 ml, 23,8 mmol) wurden vereinigt. Die Reaktionsmischung wurde über Nacht
bei Umgebungstemperatur gehalten und dann mit Wasser (100 ml) gequencht.
Nach Trennung der Phasen wurde die wäßrige Phase mit Dichlormethan
(100 ml) extrahiert. Die organischen Phasen wurden vereinigt, über Magnesiumsulfat
getrocknet, filtriert und dann unter Vakuum auf konzentriert, was
ein gelbes Öl
ergab. Das Öl wurde
mittels Flash-Chromatographie (Kieselgel unter Elution mit Essigsäureethylester/Hexangemisch
1:1) gereinigt, was 4,8 g N4-(3-Isopropoxypropyl)-3-nitro[1,5]naphthyridin-4-amin
in Form eines gelben Pulvers, Fp. 62,5-63,5°C, ergab. Analyse: berechnet
für C19H18N4O3: %C, 57,92; %H, 6,25; %N, 19,30; gefunden:
%C, 57,96; %H, 6,19; %N, 19,51. 1H-NMR (300
MHz, CDCl3) δ 10,08 (breites s, 1H), 9,38
(breites s, 1H), 8,78 (m, 1H), 8,21 (dd, J = 8,4, 1,6 Hz, 1H), 7,64
(dd, J = 8,4, 4,1 Hz, 1H), 4,57 (breites s, 2H), 3,65-3,57 (m, 3H),
2,05 (t, J = 5,6 Hz, 2H), 1,19 (d, J = 6,0 Hz, 6 H); MS (EI): m/e
290,1366 (290,1378 berechnet für
C14H18N4O3)
-
Beispiel 72
-
Verbindung der Formel
XXXII
-
N4-(3-Isopropoxypropyl)[1,5]naphthyridin-3,4-diamin
-
N4-(3-Isopropoxypropyl)-3-nitro[1,5]naphthyridin-4-amin
(4,2 g, 14,5 mmol), Platin auf Kohle (1,1 g, 5%) und Essigsäureethylester
(100 ml) wurden in einen Hydrierkolben gegeben. Die Mischung wurde
unter einem Wasserstoffdruck von 50 psi (3,5 kg/cm2)
2,5 Stunden geschüttelt.
Die Reaktionsmischung wurde filtriert, wonach der Katalysator mit
Essigsäureethylester
gewaschen wurde. Das Filtrat wurde über Magnesiumsulfat getrocket,
filtriert und dann unter Vakuum aufkonzentriert, was 3,6 g N4-(3-Isopropoxypropyl)[1,5]naphthyridin-3,4-diamin
in Form eines leuchtendgelben Öls
ergab. 1H-NMR (300 MHz, CDCl3) δ 8,70 (dd,
J = 4,1, 1,6 Hz, 1H), 8,39 (s, 1H), 8,17 (dd, J = 8,4, 1,6 Hz, 1H),
7,37 (dd, J = 8,4, 4,1 Hz, 1H), 5,99 (breites s, 1H), 3,98 (breites
s, 2H), 3,63-3,55 (m, 5H), 1,87 (Pentett, J = 6,2 Hz, 2H), 1,17
(d, J = 6,1 Hz, 6H); MS (EI): m/e 260,1630 (260,1637 berechnet für C14H20N4O).
-
Beispiel 73
-
Verbindung der Formel
XXXIII
-
2-Butyl-1-(3-Isopropoxypropyl)-1H-imidazo[4,5-c][1,5]naphthyridin
-
Teil A
-
Eine
auf einem Eisbad gekühlte
Lösung
von N4-(3-Isopropoxypropyl)[1,5]naphthyridin-3,4-diamin
(3,2 g, 12,3 mmol) in Dichlormethan (40 ml) wurde über einen
Zeitraum von 15 Minuten tropfenweise mit Valerylchlorid (1,53 ml,
12,9 mmol) versetzt. Nach Wegnahme des Kühlbads wurde die Reaktionsmischung
1 Stunde bei Umgebungstemperatur gehalten. Dann wurde das Lösungsmittel
unter Vakuum abgezogen, was einen dunkelbraunen Feststoff ergab.
-
Teil B
-
Das
Material aus Teil A und eine 7,5%ige Lösung von Ammoniak in Methanol
(100 ml) wurden in ein Druckgefäß eingebracht.
Das Gefäß wurde
verschlossen und dann 6 Stunden auf 150°C erhitzt. Nach Abkühlen auf
Umgebungstemperatur wurde die Mischung unter Vakuum auf konzentriert.
Der Rückstand
wurde zwischen Dichlormethan (150 ml) und Wasser (150 ml) verteilt.
Nach Trennung der Fraktionen wurde die wäßrige Fraktion mit Dichlormethan
(100 ml) extrahiert. Die organischen Fraktionen wurden vereinigt, über Magnesiumsulfat
getrocknet, filtriert und dann unter Vakuum auf konzentriert, was
ein braunes Öl
ergab. Das Öl
wurde mittels Flash-Chromatographie (Kieselgel unter Elution mit
Essigsäureethylester)
gereinigt, was 3,1 g 2-Butyl- 1-(3-Isopropoxypropyl)-1H-imidazo[4,5-c][1,5]naphthyridin
in Form eines farblosen Öls
ergab. 1H-NMR (300 MHz, CDCl3) δ 9,32 (s,
1H), 8,90 (dd, J = 4,3, 1,7 Hz, 1H), 8,49 (dd, J = 8,5, 1,7 Hz,
1H), 7,57 (dd, J = 8,5, 4,3 Hz, 1H), 4,94 (t, J = 7,0 Hz, 2H), 3,56
(Pentett, J = 6,1 Hz, 1H), 3,44 (t, J = 5,7 Hz, 2H), 3,05 (t, J
= 7,9 Hz, 2H), 2,29-2,20 (m, 2H), 2,01-1,90 (m, 2H), 1,60-1,48 (m,
2H), 1,15 (d, J = 6,1 Hz, 6H), 1,03 (t, J = 7,3 Hz, 3H); MS (EI):
m/e 326,2104 (326,2106 berechnet für C19H26N4O).
-
Beispiel 74
-
Verbindung der Formel
XXXIV
-
2-Butyl-1-(3-Isopropoxypropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
-
2-Butyl-1-(3-Isopropoxypropyl)-1H-imidazo[4,5-c][1,5]naphthyridin
(1,4 g, 4,3 mmol) in Chloroform (20 ml) wurde über einen Zeitraum von 20 Minuten
in vier Portionen mit 3-Chlorperbenzoesäure (1,2 g, 57-86%ig) versetzt.
Die Reaktionsmischung wurde 2 Stunden bei Umgebungstemperatur gehalten
und mit gesättigtem Natriumhydrogencarbonat
(2 × 15
ml) und Wasser (20 ml) gewaschen. Die organische Fraktion wurde über Magnesiumsulfat
getrocknet, filtriert und dann unter Vakuum auf konzentriert, was
ein gelbes Öl
ergab. Das Öl wurde
mittels Säulenchromatographie
(Kieselgel unter Elution mit Essigsäureethylester/Methanol 95:5)
gereinigt, was 0,95 g 2-Butyl-1-(3-Isopropoxypropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
in Form eines gelben Feststoffs, Fp. 92,0-93,0°C, ergab. Analyse: berechnet
für C19H26N4O2: %C, 66, 64; %H, 7, 65; %N, 16,36; gefunden:
%C, 66,18; %H, 7,39; %N, 16,26. 1H-NMR (300 MHz, CDCl3) δ 9,24
(dd, J = 8,8, 1,6 Hz, 1H), 9,05 (s, 1H), 8,98 (dd, J = 4,3, 1,6
Hz, 1H), 7,6 (dd, J = 8,8, 4,3 Hz, 1H), 4,89 (t, J = 7,0 Hz, 2H),
3,56 (Pentett, J = 6,1 Hz, 1H), 3,44 (t, J = 5,7 Hz, 2 H), 3,02
(t, J = 7,9 Hz, 2H), 2,27-2,18 (m, 2H), 1,97-1,87 (m, 2H), 1,59-1,47 (m,
2H), 1,15 (d, J = 6,1 Hz, 6H), 1,02 (t, J = 7,3 Hz, 3H).
-
Beispiel
75 Verbindung
der Formel I 2-Butyl-1-(3-isopropoxypropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
-
Unter
Stickstoffatmosphäre
wurde Trichloracetylisocyanat (0,42 ml, 3,5 mmol) zu einer Lösung von 2-Butyl-1-(3-isopropoxypropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
(0,8 g, 2,3 mmol) in Dichlormethan (25 ml) getropft. Die Reaktionsmischung
wurde 2 Stunden bei Umgebungstemperatur gehalten und dann unter Vakuum
auf konzentriert, was ein gelbes Öl ergab. Das Öl wurde
in Methanol (15 ml) gelöst
und dann langsam mit Natriummethoxid (0,8 ml, 25%ig in Methanol,
3,5 mmol) versetzt. Der Ansatz wurde über Nacht bei Umgebungstemperatur
gehalten. Der erhaltene Niederschlag wurde abfiltriert und dann
aus Essigsäuremethylester umkristallisiert,
was 0,47 g 2-Butyl-1-(3-isopropoxypropyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
in Form eines weißen
kristallinen Feststoffs, Fp. 174-175°C, ergab. Analyse: berechnet
für C19H27N5O:
%C, 66,83; %H, 7,97; %N, 20,51; gefunden: %C, 66,70; %H, 7,81; %N,
20,75. 1H-NMR (300 MHz, CDCl3): δ 8,50 (dd,
J = 4,3, 1,5 Hz, 1H), 7,90 (dd, J = 8,4, 1,5 Hz, 1H), 7,42 (dd,
J = 8,4, 4,3 Hz, 1H), 6,75 (s, 2H), 4,77 (t, J = 6,8 Hz, 2H), 3,50
(Pentett, J = 6,1 Hz, 1H), 3,35 (m, 2H), 2,95 (t, J = 7,8 Hz, 2H),
2,13-2,04 (m, 2H), 1,86-1,76 (m, 2H), 1,52-1,40 (m, 2H), 1,05 (d,
J = 6,1 Hz, 6H), 0,97 (t, J = 7,3 Hz, 3 H).
-
Beispiel 76
-
Verbindung der Formel
XXXI
-
N4-(3-Butoxypropyl)-3-nitro[1,5]naphthyridin-4-amin
-
Unter
Stickstoffatmosphäre
wurde 3-Butoxypropylamin (4,0 ml, 26 mmol) über einen Zeitraum von 10 Minuten
zu einer Lösung
von 4-Chlor-3-nitro[1,5]naphthyridin (4,6 g, 22 mmol) und Triethylamin
(4,6 ml, 33 mmol) in Dichlormethan (150 ml) getropft. Die Reaktionsmischung
wurde über
Nacht bei Umgebungstemperatur gehalten. Nach Zugabe von Wasser (100
ml) wurden die Phasen getrennt. Die wäßrige Phase wurde mit Dichlormethan
(100 ml) extrahiert. Die organischen Fraktionen wurden vereinigt, über Magnesiumsulfat
getrocknet, filtriert und dann unter Vakuum auf konzentriert, was
ein gelbes Öl
ergab. Das Öl
wurde mittels Flash-Chromatographie (Kieselgel unter Elution mit
Essigsäureethylester/Hexangemisch
1:1) gereinigt, was 5,3 g N4-(3-Butoxypropyl)-3-nitro[1,5]naphthyridin-4-amin
in Form eines farblosen Öls
ergab. 1H-NMR (300 MHz, CDCl3): δ 10,08 (breites
s, 1H), 9,38 (breites s, 1H), 8,78 (m, 1H), 8,22 (dd, J = 8,4, 1,6
Hz, 1H), 7,64 (dd, J = 8,4, 4,1 Hz, 1H), 4,57 (breites s, 2H), 3,63
(t, J = 5,8 Hz, 2H), 3,46 (t, J = 6,7 Hz, 2H), 2,10-2,03 (m, 2H), 1,65-1,55
(m, 2H), 1,44-1,32 (m, 2H), 0,92 (t, J = 7,3 Hz, 3H); MS (EI): m/e
304,1535 (304,1535 berechnet für C15H20N4O3).
-
Beispiel 77
-
Verbindung der Formel
XXXII
-
N4-(3-Butoxypropyl)[1,5]naphthyridin-3,4-diamin
-
In
Analogie zu Beispiel 72 wurde N4-(3-Butoxypropyl)-3-nitro[1,5]naphthyridin-4-amin
(4,9 g, 16 mmol) reduziert, was 4,3 g N4-(3-Butoxypropyl)[1,5]naphthyridin-3,4-diamin
in Form eines leuchtendgelben Öls ergab.
Analyse: berechnet für
C15H22N4O:
%C, 65,67; %H, 8,08; %N, 20,42; gefunden: %C, 65,48; %H, 8,07; %N, 20,41. 1H-NMR (300 MHz, CDCl3): δ 8,70 (dd,
J = 4,1, 1,6 Hz, 1H), 8,39 (s, 1H), 8,18 (dd, J = 8,4, 1,6 Hz, 1
H), 7,37 (dd, J = 8,4, 4,1 Hz, 1H), 5,97 (breites s, 1H), 3,96 (breites
s, 2H), 3,63-3,56 (m, 4H), 3,44 (t, J = 6,7 Hz, 2H), 1,89 (Pentett,
J = 6,2 Hz, 2H), 1,63-1,53 (m, 2H), 1,44-1,32 (m, 2H), 0,93 (t,
J = 7,3 Hz, 3H); MS (EI): m/e 274,1799 (274,1793 berechnet für C15H22N4O)
-
Beispiel 78
-
Verbindung der Formel
XXXIII
-
1-(3-Butoxypropyl)-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin
-
In
Analogie zu Beispiel 73 Teil A und Teil B wurde N4-(3-Butoxypropyl)[1,5]naphthyridin-3,4-diamin
(3,7 g, 13,5 mmol) mit Valerylchlorid (1,7 ml, 14,3 mmol) umgesetzt
und das erhaltene Amidzwischenprodukt cyclisiert, was 2,9 g 1-(3-Butoxypropyl)-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin
in Form eines farblosen Öls
ergab. Eine kleine Portion wurde mittels Flash-Chromatographie (Kieselgel unter Elution
mit Essigsäureethylester)
gereinigt, was eine reine Probe in Form eines weißen Pulvers,
Fp. 56,5-57,5°C,
ergab. Analyse: berechnet für
C20H28N4O:
%C, 70,56; %H, 8,29; %N, 16,46; gefunden: %C, 70,48; %H, 8,25; %N,
16,61. 1H-NMR (300 MHz, CDCl3): δ 9,32 (s,
1H), 8,90 (dd, J = 4,3, 1,6 Hz, 1H), 8,49 (dd, J = 8,5, 1,6 Hz,
1H), 7,57 (dd, J = 8,5, 4,3 Hz, 1H), 4,94 (t, J = 7,0 Hz, 2 H),
3,45-3,39 (m, 4H), 3,04 (t, J = 7,9 Hz, 2H), 2,26 (Pentett, J =
6,1 Hz, 2H), 2,01-1,91 (m, 2H), 1,62-1,48 (m, 4H), 1,45-1,33 (m, 2H), 1,03
(t, J = 7,3 Hz, 3 H), 0,94 (t, J = 7,3 Hz, 3H).
-
Beispiel 79
-
Verbindung der Formel
XXXIV
-
1-(3-Butoxypropyl)-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
-
In
Analogie zu Beispiel 74 wurde 1-(3-Butoxypropyl)-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin
(2,2 g, 6,47 mmol) oxidiert, was 1,6 g 1-(3-Butoxypropyl)-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
in Form eines gelben Pulvers, Fp. 126,5-127,5°C, ergab. Analyse: berechnet
für C20H28N4O2: %C, 67,39; %H, 7,92; %N, 15,72; gefunden:
%C, 67,13; %H, 7,69; %N, 15,82. 1H-NMR (300 MHz, CDCl3): δ 9,22
(dd, J = 8,8, 1,5 Hz, 1H), 9,04 (s, 1H), 8,99 (dd, J = 4,3, 1,5
Hz, 1H), 7,65 (dd, J = 8,8, 4,3 Hz, 1H), 4,89 (t, J = 7,0 Hz, 2H), 3,46-3,39
(m, 4H), 3,01 (t, J = 7,9 Hz, 2H), 2,28-2,20 (m, 2H), 1,97-1,87 (m, 2H), 1,62-1,46
(m, 4H), 1,45-1,33 (m, 2H), 1,03 (t, J = 7,3 Hz, 3H), 0,94 (t, J
= 7,3 Hz, 3H).
-
Beispiel
80 Verbindung
der Formel I 1-(3-Butoxypropyl)-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
-
In
Analogie zu Beispiel 75 wurde 1-(3-Butoxypropyl)-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
(1,2 g, 3,4 mmol) mit Trichloracetylisocyanat (0,6 ml, 5,0 mmol)
umgesetzt und das erhaltene Zwischenprodukt hydrolysiert, was 0,86
g 1-(3-Butoxypropyl)-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
in Form eines weißen
Pulvers, Fp. 101,0-101,5°C,
ergab. Analyse: berechnet für
C20H29N5O:
%C, 67,58; %H, 8,22; %N, 19,70; gefunden: %C, 67,55; %H, 7,96; %N,
20,10. 1H-NMR (300 MHz, DMSO): δ 8,50 (dd,
J = 4,4, 1,5 Hz, 1H), 7,91 (dd, J = 8,4, 1,6 Hz, 1H), 7,42 (dd,
J = 8,4, 4,4 Hz, 1H), 6,77 (s, 2H), 4,78 (t, J = 6,9 Hz, 2H), 3,38-3,30 (m, 4H), 2,93
(t, J = 7,8 Hz, 2H), 2,11 (Pentett, J = 6,1 Hz, 2H), 1,82 (Pentett,
J = 7,6 Hz, 2H), 1,51-1,39 (m, 4H), 1,37-1,25 (m, 2H), 0,96 (t,
J = 7,3 Hz, 3H), 0,88 (t, J = 7,2 Hz, 3H).
-
Beispiel 81
-
Verbindung der Formel
XXXI
-
N4-(2-Phenoxyethyl)-3-nitro[1,5]naphthyridin-4-amin
-
In
Analogie zu Beispiel 76 wurde 4-Chlor-3-nitro[1,5]naphthyridin (5,0 g, 24 mmol)
mit 2-Phenoxyethylamin
(3,5 ml, 27 mmol) umgesetzt, was 6,6 g N4-(2-Phenoxyethyl)-3-nitro[1,5]naphthyridin-4-amin
in Form eines gelben Feststoffs, Fp. 107-108°C, ergab. Analyse: berechnet
für C16H14N4O3: %C, 61,93; %H, 4,55; %N, 18,05; gefunden:
%C, 61,99; %H, 4,58; %N, 18,42. 1H-NMR (300 MHz, DMSO): δ 10,25 (breites
s, 1H), 9,39 (breites s, 1H), 8,81 (dd, J = 4,1, 1,7 Hz, 1H), 8,25
(dd, J = 8,5, 1,7 Hz, 1H), 7,67 (dd, J = 8,5, 4,1 Hz, 1H), 7,34-7,26
(m, 2H), 7,01-6,96 (m, 3H), 4,89 (breites s, 2H), 4,35 (t, J = 5,1
Hz, 2H). MS (EI) m/e 310, 1065 (310, 1065 berechnet für C16H14N4O3).
-
Beispiel 82
-
Verbindung der Formel
XXXII
-
N4-(2-Phenoxyethyl)[1,5]naphthyridin-3,4-diamin
-
In
Analogie zu Beispiel 77 wurde N4-(2-Phenoxyethyl)-3-nitro[1,5]naphthyridin-4-amin
(5,4 g, 17,4 mmol) reduziert, was 4,6 g N4-(2-Phenoxyethyl)[1,5]naphthyridin-3,4-diamin
in Form eines leuchtendgelben Öls
ergab. 1H-NMR (300 MHz, DMSO): δ 8,68 (dd,
J = 4,1, 1,7 Hz, 1H), 8,40 (s, 1H), 8,10 (dd, J = 8,4, 1,7 Hz, 1
H), 7,39 (dd, J = 8,4, 4,1 Hz, 1H), 7,28-7,22 (m, 2 H), 6,94-6,90
(m, 3H), 6,12 (t, J = 7,0 Hz, 1H), 5,15 (s, 2H), 4,13 (t, J = 5,5
Hz, 2H), 3,93-3,87 (m, 2H); MS (CI): m/e 281 (M+H).
-
Beispiel 83
-
Verbindung der Formel
XXXIII
-
2-(2-Butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethylphenylether
-
In
Analogie zu Beispiel 73 Teil A und Teil B wurde N4-(2-Phenoxyethyl)[1,5]naphthyridin-3,4-diamin (4,4
g, 15,7 mmol) mit Valerylchlorid (1,95 ml, 16,4 mmol) umgesetzt
und das erhaltene Amidzwischenprodukt cyclisiert, was 4,0 g 2-(2-Butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethylphenylether
in Form eines weißen Feststoffs,
Fp. 150-150,5°C,
ergab. Analyse: berechnet für
C21H22N4O:
%C, 72,81; %H, 6,40; %N, 16,17; gefunden: %C, 72,78; %H, 6,40; %N,
16,31. 1H-NMR (300 MHz, DMSO): δ 9,25 (s,
1H), 9,00 (dd, J = 4,3, 1,7 Hz 1H), 8,52 (dd, J = 8,4, 1,7 Hz, 1H),
7,74 (dd, J = 8,4, 4,3 Hz, 1H), 7,25-7,20 (m, 2H), 6,91-6,84 (m,
3 H), 5,22 (t, J = 5,2 Hz, 2H), 4,53 (t, J = 5,2 Hz, 2 H), 3,09
(t, J = 7,7 Hz, 2H), 1,91 (Pentett, J = 7,6 Hz, 2H), 1,55-1,43 (m,
2H), 0,97 (t, J = 7,3 Hz, 3 H); MS (EI): m/e 346,1794 (346,1793
berechnet für
C21H22N4O
)
-
Beispiel 84
-
Verbindung der Formel
XXXIV
-
2-Butyl-1-(2-phenoxyethyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
-
In
Analogie zu Beispiel 74 wurde 2-(2-Butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethylphenylether (0,6
g, 1,7 mmol) oxidiert, was 0,44 g 2-Butyl-1-(2-phenoxyethyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid in Form eines
gelben Pulvers ergab. 1H-NMR (300 MHz, CDCl3): δ 9,10-9,03
(m, 3H), 7,81 (dd, J = 8,7, 4,3 Hz, 1H), 7,25-7,20 (m, 2H), 6,92-6,83
(m, 3H), 5,16 (t, J = 4,9 Hz, 2H), 4,51 (t, J = 4,9 Hz, 2H), 3,06
(t, J = 7,7 Hz, 2H), 1,93-1,83 (m, 2H), 1,54-1,41 (m, 2H), 0,96 (t, J = 7,3 Hz, 3H);
MS (CI): m/e 363 (M+H).
-
Beispiel
85 Verbindung
der Formel I 2-Butyl-1-(2-phenoxyethyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
-
In
Analogie zu Beispiel 75 wurde 2-Butyl-1-(2-phenoxyethyl)-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid (0,38 g, 1,05
mmol) mit Trichloracetylisocyanat (0,19 ml, 1,6 mmol) umgesetzt
und das erhaltene Zwischenprodukt hydrolysiert, was 0,23 g 2-Butyl-1-(2-phenoxyethyl)-1H-imidazo[4,5-c][1,5]naphthyridin-4-amin
in Form eines weißen
Pulvers, Fp. 159,0-159,2°C,
ergab. 1H-NMR (300 MHz, DMSO): δ 8,52 (dd, J
= 4,4, 1,5 Hz, 1 H), 7,92 (dd, J = 8,4, 1,5 Hz, 1H), 7,45 (dd, J
= 8,4, 4,4 Hz, 1H), 7,26-7,21 (m, 2H), 6,92-6,86 (m, 3 H), 6,79
(s, 2H), 5,13 (t, J = 5,2 Hz, 2H), 4,48 (t, J = 5,2 Hz, 2H), 3,00
(t, J = 7,8 Hz, 2H), 1,91-1,81 (Pentett, J = 7,4 Hz, 2H), 1,52-1,40
(m, 2H), 0,95 (t, J = 7,3 Hz, 3H); MS (EI): m/e 361,1899 (361,1902
berechnet für
C21H23N5O).
-
Beispiel 86
-
Verbindung der Formel
XXXI
-
N-{2-[(3-Nitro[1,5]naphthyridin-4-yl)amino]ethyl}carbamidsäure-1,1-dimethylethylester
-
Eine
Lösung
von Diisopropylethylamin (13,47 g, 0,10 mol) in Dichlormethan (25
ml) wurde zu einer Lösung
von 5-Chlor-3-nitro[1,5]naphthyridin (18,2 g, 0,086 mol) in Dichlormethan
(250 ml) gegeben. Dann wurde die Reaktionsmischung langsam mit einer
Lösung
von N-(2-Aminoethyl)carbamidsäure-tert.-butylester
(16,7 g, 0,10 mol) in Dichlormethan (75 ml) versetzt. Die Reaktionsmischung
wurde über
Nacht unter Rückfluß erhitzt.
Nach Zugabe von zusätzlichem
N-(2-Aminoethyl)carbamidsäure-tert.-butylester
(1 g) wurde die Reaktionsmischung noch 3 Stunden unter Rückfluß erhitzt.
Dann wurde die Reaktionsmischung auf Umgebungstemperatur abkühlen gelassen
und mit zusätzlichem
Dichlormethan verdünnt,
mit Wasser und mit Kochsalzlösung gewaschen,
getrocknet und dann unter Vakuum auf konzentriert, was einen dunklen
Feststoff ergab. Dieser Feststoff wurde mittels Flash-Chromatographie (Kieselgel
unter Elution mit Dichlormethan) gereinigt, was 24,8 g N-{2-[(3-Nitro[1,5]naphthyridin-4-yl)amino]ethyl}carbamidsäure-1,1-dimethylethylester
in Form eines kanariengelben Feststoffs ergab. Eine Portion (0,3
g) wurde aus Toluol (10 ml) und Heptan (10 ml) umkristallisiert, was
0,2 g kanariengelbe Nadeln, Fp. 149-151°C, ergab. Analyse: berechnet
für C15H19N5O4: %C, 54,05; %H, 5,75; %N, 21,01; gefunden:
%C, 54,17; %H, 5,73; %N, 20,90.
-
Beispiel 87
-
Verbindung der Formel
XXXII
-
N-{2-[(3-Amino[1,5]naphthyridin-4-yl)amino]ethyl}carbamidsäure-1,1-dimethylethylester
-
N-{2-[(3-Nitro[1,5]naphthyridin-4-yl)amino]ethyl}carbamidsäure-1,1-dimethylethylester
(10 g, 0,03 mol), Essigsäureethylester
(800 ml) und Platin auf Kohle als Katalysator wurden in einer Parr-Flasche
vereinigt, wonach die Mischung über
Nacht hydriert wurde. Dann wurde die Reaktionsmischung zur Entfernung
des Katalysators filtriert. Das Filtrat wurde unter Vakuum aufkonzentriert,
was 9,1 g N-{2-[(3-Amino[1,5]naphthyridin-4-yl)amino]ethyl}carbamidsäure-1,1-dimethylethylester
in Form eines gelben Sirups ergab. Analyse: berechnet für C15H21N5O2 + 0,1 CH3CO2C2H5:
%C, 59,25; %H, 7,04; %N, 22,43; gefunden: %C, 58,96; %H, 6,87; %N,
22,46.
-
Beispiel 88
-
Verbindung der Formel
XXXIII
-
N-[2-(H-Butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]carbamidsäure-1,1-dimethylethylester
-
N-{2-[(3-Amino[1,5]naphthyridin-4-yl)amino]ethyl}carbamidsäure-1,1-dimethylethylester
(0,6 g, 2 mmol), Orthovaleriansäuretrimethylester
(0,35 g, 2,1 mmol) und Toluol (25 ml) wurden vereinigt und 2 Stunden unter
Rückfluß erhitzt.
Nach Zugabe von zusätzlichem
Orthovaleriansäuretrimethylester
(1 Äq.)
wurde die Reaktionsmischung über
Nacht unter Rückfluß erhitzt.
Dann wurde Xylol zugegeben und das Toluol abdestilliert. Die Reaktionsmischung
wurde weitere 8 Stunden unter Rückfluß erhitzt.
Nach Abdestillieren des größten Teils des
Xylols verblieb ein Volumen von etwa 5 ml. Die Reaktionsmischung
wurde abkühlen
gelassen. Der erhaltene Niederschlag wurde abfiltriert, mit Heptan
gewaschen und getrocknet, was 0,35 g N-[2-(2-Butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]carbamidsäure-1,1-dimethylethylester
in Form eines elfenbeinfarbenen Pulvers, Fp. 198-199°C, ergab.
Analyse: berechnet für
C20H27N5O2: %C, 65,01; %H, 7,36; %N, 18,95; gefunden:
%C, 64,75; %H, 7,57; %N, 19,09.
-
Beispiel 89
-
Verbindung der Formel
XXXIII
-
1-{2-[(1,1-Dimethylethoxycarbonyl)amino]ethyl}-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
-
3-Chlorperbenzoesäure (0,7
g, 57-86%ig) wurde in Chloroform (10 ml) gelöst. Eine Hälfte dieser Lösung wurde
zu einer Lösung
von N-[2-(2-Butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]carbamidsäure-1,1-dimethylethylester
(1,0 g, 2,7 mmol) in Chloroform (10 ml) gegeben. Die Reaktionsmischung
wurde 30 Minuten bei Umgebungstemperatur gerührt und dann tropfenweise mit
der anderen Hälfte
der Chlorperbenzoesäurelösung versetzt.
Die Reaktionsmischung wurde insgesamt 2,5 Stunden bei Umgebungstemperatur
gerührt
und dann mit Chloroform (50 ml) verdünnt, mit Natriumcarbonat, 10%iger
Natronlauge, Wasser und Kochsalzlösung gewaschen, getrocknet
und unter Vakuum auf konzentriert, was 1,1 g eines gelben Feststoffs
ergab. Diese Substanz wurde zweimal aus Acetonitril umkristallisiert,
was 1,0 g 1-{2-[(1,1-Dimethylethoxycarbonyl)amino]ethyl}-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
ergab. Analyse: berechnet für C20H27N5O3: %C, 62,32; %H, 7,06; %N, 18,17; gefunden:
%C, 62,03; %H, 6,73; %N, 18,10.
-
Beispiel
90 Verbindung
der Formel I N-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]carbamidsäure-1,1-dimethylethylester
-
Trichloracetylisocyanat
(4,8 ml, 40 mmol) wurde mit einer Spritze zu einer Lösung von
1-{2-[(1,1-Dimethylethoxycarbonyl)amino]ethyl}-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
(10,4 g, 27 mmol) in Dichlormethan (75 ml) gegeben. Die Reaktionsmischung
wurde 1 Stunde bei Umgebungstemperatur gerührt. Nach Zugabe von Natriummethoxid
(9 ml, 25% Natriummethoxid in Methanol) wurde die Reaktionsmischung über Nacht
bei Umgebungstemperatur gerührt.
Da die Umsetzung gemäß Dünnschichtchromatographie
nicht vollständig
war, wurden zweimal zusätzliches
Natriummethoxid zugegeben, wobei nach jeder Zugabe 2 Stunden bei
Umgebungstemperatur gerührt
wurde. Dann wurde die Reaktionsmischung mit Dichlormethan verdünnt, mit
Natriumcarbonat, Wasser und dann mit Kochsalzlösung gewaschen, getrocknet
und dann unter Vakuum auf konzentriert, was 10,4 g eines gelben
Feststoffs ergab. Diese Substanz wurde mittels Säulenchromatographie (Kieselgel
unter Elution mit Dichlormethan) gereinigt, was 8,5 g eines Feststoffs
ergab. Dieser Feststoff wurde aus Toluol (20 ml) umkristallisiert,
was 6,0 g N-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]carbamidsäure-1,1-dimethylethylester
in Form von elfenbeinfarbenen Kristallen, Fp. 118-120°C, ergab.
Analyse: berechnet für
C20H28N6O2: %C, 62,48; %H, 7,34; %N, 21,85; gefunden:
%C, 62,31; %H, 7,23; %N, 22,13. HRMS (EI): berechnet für C20H28N6O2(M+)384,2273, gefunden 384,2273.
-
Beispiel
91 Verbindung
der Formel I 2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
-
Eine
Lösung
von N-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]carbamidsäure-1,1-dimethylethylester
(5,7 g, 15 mmol) in Dichlormethan (10 ml) wurde mit Trifluoressigsäure (5 ml)
versetzt. Die Reaktionsmischung wurde 1 Stunde bei Umgebungstemperatur
gerührt.
Dann wurde die Reaktionsmischung mit Dichlormethan verdünnt und
mit 10%iger Salzsäure
extrahiert. Das Salzsäureextrakt
wurde zweimal mit Dichlormethan gewaschen und dann mit Ammoniumhydroxid
basisch gestellt. Der erhaltene Niederschlag wurde abfiltriert und
getrocknet, was 3,7 g 2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
in Form eines weißen
Pulvers, Fp. 175-176°C,
ergab. Analyse: berechnet für
C15H20N6:
%C, 63,36; %H, 7,09; %N, 29,55; gefunden: %C, 62,98; %H, 6,92; %N,
29,89. HRMS (EI): berechnet für C15H20N6(M+)284,1749,
gefunden 284,1748.
-
Beispiel
92 Verbindung
der Formel I N
1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]acetamid
-
Unter
Stickstoffatmosphäre
wurde Acetylchlorid (50 μl,
0,7 mmol) in Dichlormethan (25 ml) zu einer auf einem Eisbad gekühlten Lösung von
2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin (0,2
g, 0,7 mmol) in Dichlormethan (50 ml) getropft. Nach vollständiger Zugabe
wurde die Reaktionsmischung auf Umgebungstemperatur kommen gelassen.
Nach 30 Minuten war die Reaktion gemäß Dünnschichtchromatographie vollständig. Dann
wurde die Reaktionsmischung mit 10%iger Natronlauge, Wasser und
Kochsalzlösung
gewaschen, getrocknet und unter Vakuum auf konzentriert, was 0,25
g Rohprodukt ergab. Diese Substanz wurde mittels Säulenchromatographie
(Kieselgel unter Elution mit Dichlormethan) gereinigt, was 0,2 g eines
Feststoffs ergab. Dieser Feststoff wurde aus Acetonitril (30 ml)
umkristallisiert, was 0,18 g N1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]acetamid
in Form eines weißen
Pulvers, Fp. 228-230°C,
ergab. Analyse: berechnet für
C17H22N6O:
%C, 62,56; %H, 6,79; %N, 25,75; gefunden: %C, 62,50; %H, 6,59; %N,
26,04. HRMS (EI): berechnet für
C22H26N6O2 (M+)326,1855, gefunden 326,1846.
-
Beispiel
93 Verbindung
der Formel I N
1-[2-(9-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-(E)-2-butenamid
-
In
Analogie zu Beispiel 92 wurde Crotonylchlorid (68 μl, 0,7 mmol)
mit 2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin (0,2
g, 0,7 mmol) umgesetzt, was 0,2 g N1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-(E)-2-butenamid in Form
eines weißen
Pulvers, Fp. 198-200°C,
ergab. Analyse: berechnet für
C19H24N6O:
%C, 64,75; %H, 6,86; %N, 23,85; gefunden: %C, 64,25; %H, 6,68; %N,
23,99. HRMS (EI): berechnet für
C19H24N6O
(M+)352,2011, gefunden 352,1996.
-
Beispiel
94 Verbindung
der Formel I N
1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-1-cyclohexancarboxamid
-
In
Analogie zu Beispiel 92 wurde Cyclohexancarbonylchlorid (94 μl, 0,7 mmol)
mit 2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(0,2 g, 0,7 mmol) umgesetzt, was 0,2 g N1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-1-cyclohexancarboxamid
in Form eines weißen
Pulvers, Fp. 188-190°C,
ergab. Analyse: berechnet für
C22H30N6O:
%C, 66,98 %H, 7,66; %N, 21,30; gefunden: %C, 66,72 %H, 7,57; %N,
21,48. HRMS (EI): berechnet für
C22H30N6O
(M+)394,2481, gefunden 394,2475.
-
Beispiel
95 Verbindung
der Formel I N
1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-3,5-di-(1,1-dimethylethyl)-4-hydroxybenzamid
-
In
Analogie zu Beispiel 92 wurde 3,5-Di-(1,1-dimethylethyl)-4-hydroxybenzoylchlorid
(0,47 g, 1,7 mmol) mit 2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(0,5 g, 1,7 mmol) umgesetzt, was 0,5 g N1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-3,5-di-(1,1-dimethylethyl)-4-hydroxybenzamid
in Form eines weißen
Pulvers, Fp. 248-250°C,
ergab. Analyse: berechnet für C30H40N6O2: %C, 69,74; %H, 7,80; %N, 16,27; gefunden:
%C, 69,65; %H, 7,69; %N, 16,42. HRMS (EI): berechnet für C30H40N6O2 (M+)516,3212, gefunden 516,3226.
-
Beispiel
96 Verbindung
der Formel I N
1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-3-phenylpropanamid
hydrochlorid
-
In
Analogie zu Beispiel 92 wurde Hydrocinnamoylchlorid (0,1 g, 0,7
mmol) mit 2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(0,2 g, 0,7 mmol) umgesetzt. Nach einer Stunde wurde die Reaktionsmischung
direkt auf eine Kieselgelsäule
gegossen und zunächst
mit Dichlormethan und dann mit 15% Methanol/Dichlormethan eluiert,
was 0,2 g eines Feststoffs ergab. Dieser Feststoff wurde aus Toluol
umkristallisiert, was 0,2 g N1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-3-phenylpropanamid-hydrochlorid
in Form eines weißen
Pulvers, Fp. 183-185°C,
ergab. Analyse: berechnet für
C29H28N6O
HCl: %C, 63,64; %H, 6,45; %N, 18,55; gefunden; %C, 63,68; %H, 6,43;
%N, 18,55.
-
Beispiel
97 Verbindung
der Formel I N-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-5-oxotetrahydro-2-furancarboxamid
-
Eine
Lösung
von (S)-(+)-5-Oxo-2-tetrahydrofurancarbonsäure (0,23 g, 1,7 mmol) in wasserfreiem
Dichlormethan (30 ml) wurde langsam zu einer Lösung von 2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin (0,5
g, 1,7 mmol) in wasserfreiem Dichlormethan (100 ml) gegeben. Die
Reaktionsmischung wurde 30 Minuten bei Umgebungstemperatur gerührt und
dann tropfenweise mit einer Lösung
von 1-[3-(Dimethoxyamino)propyl]-3-ethylcarbodiimid-hydrochlorid
(0,37 g, 1,9 mmol) in wasserfreiem Dichlormethan (50 ml) versetzt.
Die Reaktionsmischung wurde über
Nacht bei Umgebungstemperatur gerührt und dann zur Abtrennung
von Feststoffen filtriert. Das Filtrat wurde zweimal mit 10%iger
Natronlauge und dann mit Kochsalzlösung gewaschen, getrocknet
und dann unter Vakuum aufkonzentriert, was 0,3 g Rohprodukt ergab.
Diese Substanz wurde mittels Säulenchromatographie
(Kieselgel unter Elution mit Dichlormethan) gereinigt und dann aus
Acetonitril umkristallisiert, was 0,1 g N-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-5-oxotetrahydro-2-furancarboxamid
in Form eines weißen
Pulvers, Fp. 153-154°C
ergab. Analyse: berechnet für
C20H24N6O3: %C, 60,59; %H, 6,10; %N, 21,19; gefunden:
%C, 60,34; %H, 6,14; %N, 21,13. HRMS (EI): berechnet für C20H24N6O3 (M+)396,1909, gefunden 396,1905.
-
Beispiel
98 Verbindung
der Formel I N
1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-2-(3-hydroxyphenyl)acetamid
-
In
Analogie zu Beispiel 97 wurde 3-Hydroxyphenylessigsäure (0,26
g, 1,7 mmol) mit 2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(0,5 g, 1,7 mmol) umgesetzt, was 0,13 g N1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-2-(3-hydroxyphenyl)acetamid
in Form eines weißen Pulvers,
Fp. 208-210°C,
ergab. Analyse: berechnet für
C23H26N6O2: %C, 66,01; %H, 6,26; %N, 20,08; gefunden:
%C, 65,63; %H, 6,11; %N, 20,30. HRMS (EI): berechnet für C23H26N6O2 (M+)418,2117, gefunden 418,2109.
-
Beispiel
99 Verbindung
der Formel I N-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-6-hydroxy-2-pyridincarboxamid
-
In
Analogie zu Beispiel 97 wurde 6-Hydroxypicolinsäure (0,24 g, 1,7 mmol) mit
2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(0,5 g, 1,7 mmol) umgesetzt, was 0,15 g N-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-6-hydroxy-2-pyridincarboxamid
in Form eines weißen
Pulvers, Fp. 258-260°C,
ergab. Analyse: berechnet für
C21H23N7O2 + ½ CH3CN: %C, 62,03; %H, 5,80; %N, 24,66; gefunden:
%C, 61,87; %H, 5,70; %N, 24,60.
-
Beispiel
100 Verbindung
der Formel I N
1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-3,7-dimethyl-6-octenamid
-
In
Analogie zu Beispiel 97 wurde Citronellasäure (0,3 g, 1,7 mmol) mit 2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(0,5 g, 1,7 mmol) umgesetzt, was 0,5 g N1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-3,7-dimethyl-6-octenamid
in Form eines weißen
fedrigen Feststoffs, Fp. 163-164°C,
ergab. Analyse: berechnet für
C25H36N6O:
%C, 68,77; %H, 8,31; %N, 19,25; gefunden: %C, 68,84; %H, 8,14; %N,
19,58. HRMS (EI): berechnet für
C25H36N6O
(M+)436,2950, gefunden 436,2952.
-
Beispiel
101 Verbindung
der Formel I N-[1-({[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]amino}carbonyl)-3-methylbutyl]carbamidsäure-1,1-dimethylethylester
-
In
Analogie zu Beispiel 97 wurde N-t-BOC-L-leucin (0,41 g, 1,7 mmol)
mit 2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin (0,5
g, 1,7 mmol) umgesetzt, was 0,5 g N-[1-({[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]amino}carbonyl)-3-methylbutyl]carbamidsäure-1,1-dimethylethylester
in Form eines weißen
Feststoffs, Fp. 184-185°C, ergab.
HRMS (EI): berechnet für
C26H39N7O3 (M+)497,3114, gefunden 497,3093.
-
Beispiel
102 Verbindung
der Formel I N
1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-2-amino-4-methylpentanamid
-
N-[1-({[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]amino}carbonyl)-3-methylbutyl]carbamidsäure-1,1-dimethylethylester
(0,35 g, 0,7 mmol) wurde mit 1 N Salzsäure (40 ml) vereinigt und 30
Minuten auf einem Dampfbad erhitzt. Die Reaktionsmischung wurde
abkühlen
gelassen und dann mit 10%iger Natronlauge basisch gestellt. Der
erhaltene Niederschlag wurde abfiltriert und getrocknet, was 0,15
g N1-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-2-amino-4-methylpentanamid
in Form eines weißen Feststoffs,
Fp. 60-65°C,
ergab. Analyse: berechnet für
C21H31N7O:
%C, 63,27; %H, 7,86; %N, 24,66; gefunden: %C, 62,27; %H, 7,67; %N,
24,77. HRMS (EI): berechnet für
C21H31N7O
(M+)397,2590, gefunden 397,2582.
-
Beispiel
103 Verbindung
der Formel I N-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-3,5-dimethyl-4-isoxazolcarboxamid
-
In
Analogie zu Beispiel 97 wurde 3,5-Dimethylisoxazol-4-carbonsäure (0,25
g, 1,7 mmol) mit 2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(0,5 g, 1,7 mmol) umgesetzt, was 0,23 g N-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl)-3,5-dimethyl-4-isoxazolcarboxamid
in Form eines weißen
Pulvers, Fp. 188-189°C,
ergab. Analyse: berechnet für
C21H25N7O2: %C, 61,90; %H, 6,18; %N, 24,06; gefunden:
%C, 61,92; %H, 6,15; %N, 24,28. HRMS (EI): berechnet für C21H25N7O2 (M+)407,2069, gefunden 407,2068.
-
Beispiel
104 Verbindung
der Formel II N
1-[2-(4-Amino-2-butyl-6,7,8,9-tetrahydro-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-3,5-di-(1,1-dimethylethyl)-4-hydroxybenzamid
-
Eine
Lösung
von N1-[2-(9-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-3,5-di-(1,1-dimethylethyl)-4-hydroxybenzamid
(0,1 g, 0,19 mmol) in Trifluoressigsäure (15 ml) und Platinoxid
(0,1 g) wurden vereinigt und in einer Parr-Apparatur über Nacht
hydriert. Dann wurde die Reaktionsmischung zur Entfernung des Katalysators
filtriert. Das Filtrat wurde unter Vakuum auf konzentriert. Der
Rückstand
wurde in Dichlormethan gelöst.
Die Dichlormethanlösung
wurde zweimal mit 10%iger Natronlauge und Kochsalzlösung gewaschen,
getrocknet und dann unter Vakuum auf konzentriert, was Rohprodukt
ergab. Diese Substanz wurde mittels Chromatographie unter Elution
mit 10% Methanol in Dichlormethan gereinigt. Das erhaltene Öl wurde
mit Acetonitril trituriert, was 0,05 g N1-[2-(4-Amino-2-butyl-6,7,8,9-tetrahydro-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-3,5-di-(1,1-dimethylethyl)-4-hydroxybenzamid
in Form eines weißen
Pulvers, Fp. 208-210°C,
ergab. Analyse: berechnet für C30H44N6O2 + 0,1 CF3CO2H: %C, 68,17; %H, 8,35; %N, 15,79; gefunden:
%C, 68,48; %H, 8,29; %N, 16,08.
-
Beispiel
105 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-5-(1,3-dimethyl-2,6-oxo-2,3,6,7-tetrahydro-1H-purinyl)pentamid
-
4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,2
g), 5-(1,3-Dimethyl-2,6-oxo-2,3,6,7-tetrahydro-1H-purinyl)pentansäure (0,18
g) und Dichlormethan (100 ml) wurden vereinigt und 30 Minuten bei
Umgebungstemperatur gerührt.
Nach Zugabe von 1-[3-(Dimethylamino)propyl]-3-ethylcarbodiimid
(0,12 g) wurde die Reaktionsmischung 2 Stunden bei Umgebungstemperatur
gerührt.
Dann wurde der Ansatz über
eine Kieselgelsäule
filtriert und mit 10% Methanol in Dichlormethan eluiert, was 0,2
g N1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-5-(1,3-dimethyl-2,6-oxo-2,3,6,7-tetrahydro-1H- purinyl)pentamid,
Fp. 153,5-155°C,
ergab. Analyse: berechnet für
C29H38N10O3: %C, 60,61; %H, 6,66; %N, 24,37; gefunden:
%C, 60,65; %H, 6,66; %N, 24,32.
-
Beispiel
106 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-6-morpholinonicotinamid
-
In
Analogie zu Beispiel 105 wurde 6-Morpholinonicotinsäure (0,12
g, 64 mmol) mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,2
g, 0,64 mmol) umgesetzt, was N1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-6-morpholinonicotinamid
in Form eines weißen
Feststoffs, Fp. 95-100°C,
ergab. Analyse: berechnet für
C27H34N8O2 + ½ H2O: %C, 63,39; %H, 6,90; %N, 21,90; gefunden: %C,
63,69 %H, 6,95; %N, 21,52.
-
Beispiel
107 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-6-chinolincarboxamid
-
In
Analogie zu Beispiel 105 wurde 6-Chinolincarbonsäure (0,11 g, 64 mmol) mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
(0,2 g, 0,64 mmol) umgesetzt, was N1-[4-(4-Amino-2-butyl-1H-midazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-6-chinolincarboxamid
in Form eines weißen
Feststoffs, Fp. 190-191°C,
ergab. Analyse: berechnet für
C27H29N7O
+ ¼ H2O: %C, 68,70; %H, 6,30; %N, 20,77; gefunden: %C,
68,54; %H, 6,21; %N, 20,93.
-
Beispiel
108 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-2-(4-hydroxy-5-methyl-2-oxo-1,2-dihydro-1-pyrimidinyl)acetamid
-
In
Analogie zu Beispiel 105 wurde 2-(4-Hydroxy-5-methyl-2-oxo-1,2-dihydro-1-pyrimidinyl)essigsäure (0,12
g, 64 mmol) mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
(0,2 g, 0,64 mmol) umgesetzt, was 0,06 g N1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-2-(4-hydroxy-5-methyl-2-oxo-1,2-dihydro-1-pyrimidinyl)acetamid
in Form eines Feststoffs, Fp. 242-244°C, ergab.
-
Beispiel
109 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-2-(2-pyrimidinylsulfanyl)acetamid
-
In
Analogie zu Beispiel 105 wurde (2-Pyrimidinylthio)essigsäure (0,11
g, 64 mmol) mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,2
g, 0,64 mmol) umgesetzt, was N1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-2-(2-pyrimidinylsulfanyl)acetamid
in Form eines weißen
Feststoffs, Fp. 156-160°C
(Zers.), ergab.
-
Beispiel
110 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-2-(4-pyridylsulfanyl)acetamid
-
In
Analogie zu Beispiel 105 wurde (4-Pyridylthio)essigsäure (0,11 g, 64 mmol) mit 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,2
g, 0,64 mmol) umgesetzt, was 0,1 g N1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-2-(4-pyridylsulfanyl)acetamid
in Form eines Feststoffs, Fp. 127,5-129°C, ergab.
-
Beispiel
111 Verbindung
der Formel I 4-(4-Amino-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
-
Teil A
-
Eine
Lösung
von N-{4-[(3-amino[1,5]naphthyridin-4-yl)amino]butyl}carbamidsäure-1,1-dimethylethylester
(5,0 g, 15,1 mmol) in Toluol (150 ml) wurde mit Orthoameisensäuretriethylester
(2,8 ml, 16,6 mmol) versetzt. Die Reaktion wurde über Nacht
unter Rückfluß erhitzt,
wobei Ethanol in einer Dean-Stark-Falle aufgefangen wurde. Die Reaktionsmischung
wurde weitere 6 Stunden unter Rückfluß erhitzt,
dann mit p-Toluolsulfonsäure (1,4
g, 7,5 mmol) versetzt und über
Nacht unter Rückfluß erhitzt.
Es hatte sich ein dunkeloranges/braunes Öl gebildet. Der Toluolüberstand
wurde abdekantiert und unter Vakuum auf konzentriert, was 1,1 g
N-[4-(1H-Imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäure-1,1-dimethylethylester
ergab. Das Öl wurde
als 4-(1H-Imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin identifiziert. Diese
Substanz wurde mit 1,1-Dimethylethyldicarbonat umgesetzt, was noch
1 g N-[4-(1H-Imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäure-1,1-dimethylethylester
ergab. Die beiden Chargen wurden vereinigt und im nächsten Schritt
verwendet.
-
Teil B
-
Eine
Lösung
der Substanz aus Teil A in Chloroform (25 ml) wurde in kleinen Portionen
mit 3- Chlorperbenzoesäure (1,86
g, 60%ig) versetzt. Der Ansatz wurde über Nacht bei Raumtemperatur
gehalten und dann mit 5%iger Natriumcarbonatlösung verdünnt. Nach Trennung der Schichten
wurde die organische Schicht unter Vakuum auf konzentriert. Der
Rückstand
wurde mit heißem
Essigsäuremethylester
aufgeschlämmt,
abgekühlt
und dann filtriert, was 2,0 g 1-{4-[(1,1-Dimethylethylcarbonyl)amino]butyl}-1H-imidazo[4,5-c][1,5]naphthyridin-5N-oxid
ergab.
-
Teil C
-
Eine
Lösung
der Substanz aus Teil B (1,2 g, 3,37 mmol) in Dichlormethan (20
ml) wurde in kleinen Portionen langsam mit Tosylchlorid (0,64 g,
3,37 mmol) versetzt. Nach 4 Stunden wurden weitere 100 mg Tosylchlorid
zugegeben, um die Reaktion zum vollständigen Umsatz zu treiben. Dann
wurde der Ansatz mit konzentriertem Ammoniumhydroxid (5 ml) und
Wasser (10 ml) gequencht und über
das Wochenende bei Umgebungstemperatur gerührt. Nach Trennung der Schichten
wurde die organische Schicht unter Vakuum auf konzentriert, was
einen hellbraunen Feststoff ergab. Dieser Feststoff wurde in heißem Essigsäuremethylester
aufgeschlämmt,
abgekühlt
und filtriert, was 0,9 g N-[4-(4-Amino-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]carbamidsäure-1,1-dimethylethylester
ergab.
-
Teil D
-
Eine
Mischung aus der Substanz aus Teil C und 1 N Salzsäure (25
ml) wurde unter Rückfluß erhitzt, bis
die Reaktion gemäß Dünnschichtchromatographie
vollständig
war. Die Mischung wurde mit 6 N Natronlange auf pH 14 eingestellt.
Der erhaltene Niederschlag wurde abfiltriert, was 0,2 g 4-(4-Amino-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
in Form eines blaßgelben
Feststoffs, Fp. 161-163°C,
ergab. Massenspektrum (M+1)=257,09.
-
Beispiel
112 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-4-{[2-(dimethylamino)ethoxy](phenyl)methyl}benzamid
-
Teil A
-
Unter
Stickstoffatmosphäre
wurde Phenylmagnesiumbromid (39 ml, 3 M in Ether) über eine
Spritze über
einen Zeitraum von 30 Minuten zu einer Lösung von 4-Formylbenzoesäuremethylester (19,2 g, 117
mmol) gegeben. Die Mischung wurde noch 10 Minuten rühren gelassen
und dann durch Zugabe von 1 M Salzsäure (125 ml) gequencht. Dann
wurde die Reaktionsmischung mit Diethylether (2 × 200 ml) extrahiert. Die vereinigten
Extrakte wurden mit Kochsalzlösung
gewaschen, über
Magnesiumsulfat getrocknet, filtriert und dann unter Vakuum auf
konzentriert, was ein gelbes Öl
ergab. Diese Substanz wurde mittels Flash-Chromatographie (Kieselgel
unter Elution mit Hexangemisch/Essigsäureethylester 6:1) gereinigt,
was 6,9 g 4-(α-Hydroxybenzyl)benzoesäuremethylester
in Form eines klaren Öls
ergab.
-
Unter
Stickstoffatmosphäre
wurde eine Suspension von p-Toluolsulfonsäure-monohydrat
(10,7 g, 56 mmol) in Toluol (70 ml) unter Rückfluß erhitzt. In einer Dean-Stark-Falle wurde
Wasser (~1 ml) aufgefangen. Dann wurde der Heizmantel weggenommen.
Die warme Mischung wurde mit einer Lösung von 4-(α-Hydroxybenzyl)benzoesäuremethylester
(3,47 g, 14 mmol) und N,N- Dimethylethanolamin
(2,9 ml, 28 mmol) in möglichst
wenig Toluol gegeben. Die Mischung wurde 20 Minuten unter Rückfluß erhitzt
und dann auf Umgebungstemperatur abkühlen gelassen. Dann wurde die
Reaktionsmischung zwischen Diethylether und gesättigtem wäßrigem Natriumhydrogencarbonat
(die wäßrige Schicht
war basisch) verteilt. Die wäßrige Schicht
wurde mit weiteren 100 ml Diethylether extrahiert. Die vereinigten
organischen Schichten wurden getrocknet und dann unter Vakuum auf
konzentriert. Der Rückstand
wurde mittels Flash-Chromatographie
(Kieselgel unter Elution mit 5% und dann 10% Methanol in Dichlormethan)
gereinigt, was 2,49 g 4-[α-(2-N,N-Dimethylaminoethoxy)benzyl]benzoesäuremethylester
in Form eines farblosen Öls
ergab.
-
Eine
Lösung
von 4-[α-(2-N,N-Dimethylaminoethoxy)benzyl]benzoesäuremethylester
(0,53 g, 1,7 mmol) in Methanol (10 ml) wurde mit 1 N Natronlauge
(2,54 ml) versetzt. Die Lösung
wurde 1 Stunde unter Rückfluß erhitzt,
auf Umgebungstemperatur abkühlen
gelassen und dann mit 1 N Salzsäure
(2,54 ml) neutralisiert (pH 5-6).
Die Mischung wurde unter Vakuum auf konzentriert (Badtemperatur
45°C). Der
erhaltene Rückstand
wurde mit einem Gemisch aus Dichlormethan (15 ml) und Methanol (3
ml) extrahiert. Das Extrakt wurde filtriert, wonach das Filtrat
unter Vakuum auf konzentriert wurde, was einen viskosen Rückstand
ergab. Durch Triturieren mit mehreren Portionen Diethylether wurden
0,39 g 4-[α-(2-N,N-Dimethylaminoethoxy)benzyl]benzoesäure in Form
eines weißen
Pulvers erhalten.
-
Teil B
-
4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin (0,130
g, 0,4175 mmol) und 4-[α-(2-N,N-Dimethylaminoethoxy)benzyl]benzoesäure (0,125
g, 0,4175 mmol) wurden in Dichlormethan (150 ml) vereinigt und bei
Umgebungstemperatur gerührt,
bis eine klare Lösung
erhalten wurde. Nach Zusatz von 1-[3- (Dimethylamino)propyl]-3-ethylcarbodiimid-hydrochlorid
(0,088 g, 0,46 mmol) wurde der Ansatz 2 Tage bei Umgebungstemperatur
gehalten. Das nach Verringerung des Dichlormethanvolumens erhaltene
Konzentrat wurde mit Flash-Chromatographie (Kieselgel unter Elution
mit 10% Methanol in Dichlormethan) gereinigt, was 0,085 g N1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-4-{[2-(dimethylamino)ethoxy](phenyl)methyl}benzamid
in Form eines Feststoffs, Fp. 105-108°C ergab. Massenspektrum (M+1)=594,30.
-
Beispiel
113 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-4-benzoylbenzamid
-
In
Analogie zu Beispiel 112 Teil B wurde 4-Benzoylbenzoesäure (72 mg, 0,32 mmol) mit
4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
(100 mg, 0,32 mmol) umgesetzt, was 30 mg N1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butyl]-4-benzoylbenzamid
in Form eines weißen
Feststoffs ergab. Massenspektrum (M+1 = 521,31).
-
Beispiel
114 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-2-(5-methyl-2,4-dioxo-1,2,3,4-tetrahydro-1-pyrimidinyl)acetamid
-
In
Analogie zu Beispiel 112 Teil B wurde Thymin-1-essigsäure (130 mg, 0,70 mmol) mit
4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(200 mg, 0,70 mmol) umgesetzt, was 68 mg N1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-2-(5-methyl-2,4-dioxo-1,2,3,4-tetrahydro-1-pyrimidinyl)acetamid
in Form eines weißen
Feststoffs, Fp. 241-242°C,
ergab. Massenspektrum (M+1 = 451,24).
-
Beispiel
115 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-6-(5-methyl-2-oxo-4-imidazolidinyl)hexamid
-
In
Analogie zu Beispiel 112 Teil B wurde D-Desthiobiotin (151 mg, 0,70 mmol) mit
4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(200 mg, 0,70 mmol) umgesetzt, was 231 mg N1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-6-(5-methyl-2-oxo-4-imidazolidinyl)hexamid
in Form eines weißen
Feststoffs, Fp. 184-186°C,
ergab. Massenspektrum (M+1 = 481,35).
-
Beispiel
116 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]methansulfonamid
-
In
Analogie zu den nachstehenden Beispielen wurde 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin (14
mg, 50 μmol)
mit Methansulfonylchlorid (4 μl,
50 μmol)
umgesetzt, was 5, 3 mg N1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]methansulfonamid
ergab. 1H-NMR (500 MHz, d6-DMSO) δ = 8,49 (dd,
J = 4,3, 1,5 Hz, 1H), 7,92 (dd, J = 8,0, 1,5 Hz, 1H), 7,44 (dd,
J = 8,0, 4,3 Hz, 1H), 7,30 (t, J = 6 Hz, 1H), 6,76 (s, 2H), 4,77
(t, J = 6 Hz, 2H), 3,50 (q, J = 6 Hz, 2H), 2,98 (t, J = 7 Hz, 2
H), 2,85 (s, 3H), 1,82 (Quintett, J = 7 Hz, 2H), 1,46 (m, 2H), 0,96
(t, J = 7 Hz, 3H); Massenspektroskopie mittels APCI(+/–)-Pfropfeninjektion
ergab das gewünschte
MG.
-
Beispiel
117 Verbindung
der Formel I N
1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]benzolsulfonamid
-
In
Analogie zu den nachstehenden Beispielen 118-152 wurde 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(14 mg, 50 μmol)
mit Benzolsulfonylchlorid (6 μl,
50 μmol)
umgesetzt, was 10, 9 mg N1-[4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]benzolsulfonamid
ergab. 1H-NMR (500 MHz, d6-DMSO) δ =
8,43 (dd, J = 4,4, 1,5 Hz, 1H), 7,94 (t, J = 6 Hz, 1H), 7,89 (dd,
J = 8,4, 1,5 Hz, 1H), 7,68 (d, J = 8 Hz, 2H), 7,58 (t, J = 8 Hz,
1H), 7,50 (t, J = 8 Hz, 2H), 7,41 (dd, J = 8,4, 4,4 Hz, 1H), 4,72
(t, J = 6 Hz, 2H), 3,34 (m, 2H), 2,97 (t, J = 7 Hz, 2H), 1,81 (Quintett,
J = 7 Hz, 2 H), 1,45 (Sextett, J = 7 Hz, 2H), 0,97 (t, J = 7 Hz,
3 H); Massenspektroskopie mittels APCI(+/–)-Pfropfeninjektion ergab das gewünschte MG.
-
Beispiele 118-152
-
Verbindungen der Formel
I
-
Die
in der nachstehenden Tabelle dargestellten Verbindungen gemäß den Beispielen
118-152 wurden folgendermaßen
hergestellt. In einem Reagenzglas mit Schraubdeckel wurde 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(50 μmol)
in Dichlormethan (5 ml) gelöst,
wonach die Lösung
in einem Eis-Wasser-Bad abgekühlt
wurde. Dann wurde ein Säurechlorid
(50 μmol)
der Formel RACOCl in Form einer Lösung in
100 μl Dichlormethan
zugegeben (feste Säurechloride
wurden in 400 μl
Dichlormethan gelöst oder
suspendiert und dann zugegeben). Die Mischung wurde 15 Sekunden
bis 1 Minute verwirbelt, wobei sie trüb wurde, dann mit ~80 mg eines
Aminomethylpolystyrolharzes (0,62 mÄq/g, 100-200 mesh, 1% Vernetzung, Bachem
Nr. D-2100, Los-Nr. FM507) versetzt und noch 30 Sekunden verwirbelt.
Dann wurde die Mischung auf eine kurze Säule (3 × 1 cm) von mit Dichlormethan
konditioniertem Kieselgel aufgetragen. Das Produkt wurde mit einem
Gemisch aus Dichlormethan und Methanol im Verhältnis 10:1 eluiert, wobei ~2
ml-Fraktionen aufgefangen
wurden. Nach dünnschichtchromatographischer
Analyse der Fraktionen wurden Fraktionen mit dem Produktfleck vereinigt
und in einem Savant SpeedVac bis zur Trockne eingedampft. Die Reinheit
wurde mittels Umkehrphasen-HPLC überprüft (HPLC-Bedingungen
beziehen sich auf die Verwendung eines Systems HP 1090 von Hewlett
Packard mit einer Säule
der Bauart C18 Rainin Microsorb MV, 4,6 × 50 mm, Teilchengröße = 3 Mikron,
Porengröße = 100
Angstrom. Gradientenelution: linearer Gradient von 100% Wasser +
0,1% Trifluoressigsäure
auf 100% Acetonitril + 0,1% Trifluoressigsäure über einen Zeitraum von 5 Min.
bei 1 ml pro Minute. Die Detektion erfolgt bei 220 nm und 254 nm).
Die RPCI-Massenspektrendaten bestätigten die Gegenwart des erwarteten
Molekülions,
und die Protonen-NMR-Daten
stimmten mit der erwarteten Struktur überein.
-
-
-
-
-
-
-
-
Beispiele 153-190
-
Verbindungen
der Formel I
-
Die
in der nachstehenden Tabelle dargestellten Verbindungen gemäß den Beispielen
153-190 wurden folgendermaßen
hergestellt. In einem Reagenzglas mit Schraubdeckel wurde 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)butanamin
(25 μmol)
in Dichlormethan (10 ml) gelöst,
wonach die Lösung
in einem Eis-Wasser-Bad abgekühlt
wurde. Dann wurde ein Säurechlorid
(25 μmol)
der Formel RACOCl in Form einer Lösung in
100 μl Dichlormethan
zugegeben (feste Säurechloride
werden direkt zugegeben). Die Mischung wurde 15 Sekunden bis 1 Minute
verwirbelt, wobei sie trüb
wurde, dann mit ~80 mg eines Aminomethylpolystyrolharzes (0,62 mÄq/g, 100-200
mesh, 1% Vernetzung, Bachem Nr. D-2100, Los-Nr. FM507) versetzt
und noch 30 Sekunden verwirbelt. Dann wurde die Mischung auf eine
kurze Säule
(3 × 1
cm) von mit Dichlormethan konditioniertem Kieselgel aufgetragen.
Das Produkt wurde mit einem Gemisch aus Dichlormethan und Methanol
im Verhältnis
10:1 eluiert, wobei ~2 ml-Fraktionen
aufgefangen wurden. Nach dünnschichtchromatographischer
Analyse der Fraktionen wurden Fraktionen mit dem Produktfleck vereinigt
und in einem Savant SpeedVac bis zur Trockne eingedampft. Die Reinheit
wurde mittels Umkehrphasen-HPLC überprüft (HPLC-Bedingungen
beziehen sich auf die Verwendung eines Systems HP 1090 von Hewlett
Packard mit einer Säule
der Bauart C18 Rainin Microsorb MV, 4,6 × 50 mm, Teilchengröße = 3 Mikron,
Porengröße = 100 Angstrom.
Gradientenelution: linearer Gradient von 100 Wasser + 0,1% Trifluoressigsäure auf
100% Acetonitril + 0,1% Trifluoressigsäure über einen Zeitraum von 5 Min.
bei 1 ml pro Minute. Die Detektion erfolgt bei 220 nm und 254 nm.)
Die APCI-Massenspektrendaten bestätigten die Gegenwart des erwarteten
Molekülions,
und die Protonen-NMR-Daten
stimmten mit der erwarteten Struktur überein.
-
-
-
-
-
-
-
-
-
Beispiele 191-212
-
Verbindungen
der Formel I
-
Die
in der nachstehenden Tabelle dargestellten Verbindungen gemäß den Beispielen
191-212 wurden folgendermaßen
hergestellt. In einem Reagenzglas mit Schraubdeckel wurde 4-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(50 μmol)
in Dichlormethan (5 ml) gelöst,
und bei Umgebungstemperatur mit einer Carbonsäure (50 μmol) der Formel RACOOH
versetzt. In der Regel bildete sich innerhalb von 3 Minuten eine
helle Suspension. Nach Zugabe des Kupplungsmittels 1-(3-Dimethylaminopropyl)-3-ethylcarbodiimid-hydrochlorid
(10,5 mg, 55 μmol)
wurde die Mischung 1-2 h bei Umgebungstemperatur bei 400 U/Min. verwirbelt,
was in den meisten Fällen
eine klare Lösung
ergab. Dann wurde die Mischung auf eine kurze Säule (3 × 1 cm) von mit Dichlormethan
konditioniertem Kieselgel aufgetragen. Das Produkt wurde mit einem
Gemisch aus Dichlormethan und Methanol im Verhältnis 10:1 eluiert, wobei ~2
ml-Fraktionen aufgefangen wurden. Nach dünnschichtchromatographischer
Analyse der Fraktionen wurden Fraktionen mit dem Produktfleck vereinigt
und in einem Savant SpeedVac bis zur Trockne eingedampft. Die Reinheit
wurde mittels Umkehrphasen-HPLC überprüft (HPLC-Bedingungen
beziehen sich auf die Verwendung eines Systems HP 1090 von Hewlett
Packard mit einer Säule
der Bauart C18 Rainin Microsorb MV, 4,6 × 50 mm, Teilchengröße = 3 Mikron, Porengröße = 100
Angstrom. Gradientenelution: linearer Gradient von 100% Wasser +
0,1% Trifluoressigsäure
auf 100 Acetonitril + 0,1% Trifluoressigsäure über einen Zeitraum von 5 Min.
bei 1 ml pro Minute. Die Detektion erfolgt bei 220 nm und 254 nm).
Die APCI-Massenspektrendaten
bestätigten
die Gegenwart des erwarteten Molekülions, und die Protonen-NMR-Daten
stimmten mit der erwarteten Struktur überein.
-
-
-
-
-
-
Beispiel
213 Verbindung
der Formel II N-[2-(4-Amino-2-butyl-1H-imidazo
[4,5-c][1,5]naphthyridin-1-yl)ethyl]5-oxo-2-pyrrolincarboxamid
-
In
Analogie zu Beispiel 97 wurde L-Pyroglutaminsäure (0,23 g, 1,7 mmol) mit
2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethanamin
(0,5 g, 1,7 mmol) umgesetzt, was 0,10 g N-[2-(4-Amino-2-butyl-1H-imidazo[4,5-c][1,5]naphthyridin-1-yl)ethyl]-5-oxo-2-pyrrolincarboxamid
in Form eines weißen Pulvers,
Fp. 135-138°C,
ergab. Analyse: berechnet für
C20H25N7O2 ½ CH3CN: %C, 60,63; %H, 6,42; %N, 25,25; gefunden:
%C, 60,14; %H, 6,41; %N, 25,20. HRMS (EI) berechnet für C20H25N7O2 (M+) 396,2103 gefunden 396,2112.
-
TESTMETHODEN
-
CYTOKININDUKTION IN HUMANEN
ZELLEN
-
Zur
Beurteilung der Cytokininduktion durch erfindungsgemäße Verbindungen
diente ein in-vitro-Humanblutzellensystem.
Die Aktivität
gründet
sich auf die Messung von in Kulturmedien abgegebenem Interferon und
Tumornekrosefaktor (α)
(IFN bzw. TNF), wie von Testerman et al. in "Cytokine Induction by the Immunomodulators
Imiquimod and S-27609",
Journal of Leukocyte Biology, 58, 365-372 (September, 1995), beschrieben.
-
Blutzellenpräparation
zur Kultur
-
Vollblut
von gesunden menschlichen Spendern wird durch Venenpunktion in EDTA-Vacutainer-Röhrchen gesammelt.
Aus Vollblut wurden durch Dichtegradientenzentrifugation mit Histopaque®-1077
(Sigma Chemicals, St. Louis, NO, USA) periphere mononukleare Blutzellen
(PBMCs) abgetrennt. Die PBMCs werden in einer Konzentration von
1,5-2 × 106 Zellen/ml in RPMI-1640-Medium mit 10% fötalem Rinderserum, 2 mM L-Glutamin
und 1% Penicillin/Streptomycin-Lösung
(RPMI komplett) suspendiert. 1-ml-Portionen der PBMC-Suspension
werden in sterile Flachboden-Gewebekulturplatten mit 24 Vertiefungen
gefüllt.
-
Vorbereitung
der Verbindung
-
Die
Verbindungen werden in Dimethylsulfoxid (DMSO) solubilisiert. Die
DMSO-Konzentration sollte eine Endkonzentration von 1% für die Zugabe
zu den Kulturvertiefungen nicht überschreiten.
Die Verbindungen werden im allgemeinen in einem Konzentrationsbereich
von 0,1 bis 100 μM
geprüft.
-
Inkubation
-
Die
Lösung
der Testverbindung wird zu den 1 ml PBMCs in Medium enthaltenden
Vertiefungen gegeben. Die Platten werden mit Kunststoffdeckeln abgedeckt,
vorsichtig vermischt und dann mit einer 5% Kohlendioxid enthaltenden
Atmosphäre
18 bis 24 Stunden bei 37°C
inkubiert.
-
Trennung
-
Nach
der Inkubation werden die Platten 5-10 Minuten bei 1000 U/Min. (~200 × g) bei
4°C zentrifugiert. Der Zellkulturüberstand
wird mit einer sterilen Polypropylenpipette entnommen und in ein
steriles 2-ml-Cryoröhrchen überführt. Die
Proben werden bis zur Analyse bei –70°C gehalten.
-
Interferon-Analyse/Berechnung
-
Die
Bestimmung von Interferon erfolgt mittels Bioassay unter Verwendung
von mit Encephalomyocarditis provozierten Humanlungenkarzinomzellen
A549. Die Einzelheiten dieser Bioassay-Methode sind von G.L. Brennan
und L.H. Kronenberg in "Automated
Bioassay of Interferons in Micro-test Plates", Biotechniques, Juni/Juli, 78, 1983,
beschrieben worden, worauf hiermit ausdrücklich Bezug genommen wird.
Kurz gesagt geht man hierbei folgendermaßen vor: A549-Zellen werden
mit Proben und Standard-Interferonverdünnungen 24 Stunden bei 37°C inkubiert.
Die inkubierten Zellen werden dann mit einem Inoculum des Encephalomyocarditis-Virus
infiziert. Die infizierten Zellen werden weitere 24 Stunden bei
37°C inkubiert,
wonach die cytopathische Wirkung des Virus quantitativ bestimmt
wird. Die quantitative Bestimmung der cytopathischen Wirkung des
Virus erfolgt durch Anfärben
und anschließende
visuelle Benotung der Platten. Die Ergebnisse werden als Alpha-Referenzeinheiten/ml
auf der Basis des für
NIH-Humanleukozyten-IFN-Standard
erhaltenen Werts ausgedrückt.
-
Tumornekrosefaktor (α)-Analyse
-
Die
Konzentration von Tumornekrosefaktor (α)(TNF) wird mit einen ELISA-Kit
von Genzyme, Cambridge, MA, USA, bestimmt. Die Ergebnisse werden
in pg/ml ausgedrückt.
-
In
der nachstehenden Tabelle gibt "+" an, daß die Verbindung
bei der jeweiligen Konzentration das angegebene Cytokin induzierte, "–" gibt an, daß die Verbindung bei der jeweiligen
Konzentration das angegebene Cytokin nicht induzierte und "±" gibt an, daß die Ergebnisse bei der jeweiligen
Konzentration unklar waren.
-
-
-
-
-
-
-
-
INTERFERON (α)-INDUKTION
IN HUMANEN ZELLEN
-
Zur
Beurteilung der Interferoninduktion durch die erfindungsgemäßen Verbindungen
diente ein in-vitro-Humanblutzellensystem.
Die Aktivität
gründet
sich auf die Messung von in Kulturmedium abgegebenem Interferon.
Die Bestimmung des Interferons erfolgt mittels Bioassay.
-
Blutzellenvorbereitung
zur Kultur
-
Durch
Venenpunktion wurde Vollblut in EDTA-Vacutainer-Röhrchen
gesammelt. Aus dem Vollblut wurden entweder mittels LeucoPREPTM Brand Cell Separation Tubes (von Becton
Dickinson) oder Ficoll-Paque®-Lösung (von Pharmacia LKB Biotechnology
Inc., Piscataway, NJ, USA) periphere mononukleäre Blutzellen (PBMs) abgetrennt.
Die PBMs wurden in einer Konzentration von 1 × 106/ml
in RPMI-1640-Medium (von GIBCO, Grand Island, NY, USA) mit 25 mM
HEPES (N-2-Hydroxyethylpiperazin-N'-2-ethansulfonsäure) und
L-Glutamin (mit Zusatz von 1% Penicillin-Streptomycin-Lösung) mit
einem Zusatz von 10% hitzeinaktiviertem (56°C über 30 Minuten) autologem Serum
suspendiert. 200-μl-Portionen
der PBM-Suspension wurden in sterile Gewebekulturplatten MicroTest
III mit 96 Vertiefungen (Flachboden) gefüllt.
-
Vorbereitung
der Verbindung
-
Die
Verbindungen wurden in Ethanol, Dimethylsulfoxid oder Gewebekulturwasser
solubilisiert und dann mit Gewebekulturwasser, 0,01 N Natronlauge
oder 0,01 N Salzsäure
verdünnt
(die Wahl des Lösungsmittels
hängt von
den chemischen Eigenschaften der geprüften Verbindung ab). Die Ethanol-
bzw. DMSO-Konzentration sollte eine Endkonzentration von 1% für die Zugabe
zu den Kulturvertiefungen nicht überschreiten. Die
Verbindungen wurden zunächst
in einem Konzentrationsbereich von 0,1 μg/ml bis etwa 5 μg/ml geprüft. Verbindungen,
die bei einer Konzentration von 0,5 μg/ml Induktion zeigten, wurden
dann in einem breiteren Konzentrationsbereich geprüft.
-
I nkubation
-
Die
Lösung
der Testverbindung wurde in einem Volumen (kleiner gleich 50 μl) in die
Vertiefungen mit 200 μl
verdünntem
Vollblut oder PBMs in Medium gegeben. In Kontrollvertiefungen (Vertiefungen
ohne Testverbindung) wurde durch Zugabe von Lösungsmittel und/oder Medium
ein Endvolumen von jeweils 250 μl
eingestellt. Die Platten wurden mit Kunststoffdeckeln verschlossen,
vorsichtig verwirbelt und dann mit einer 5% Kohlendioxid enthaltenden
Atmosphäre
48 Stunden bei 37°C
inkubiert.
-
Abtrennung
-
Nach
der Inkubation wurden die Platten mit Parafilm abgedeckt und dann
in einer Zentrifuge der Bauart Damon IEC Modell CRU-5000 bei 1000
U/Min. 10 bis 15 Minuten bei 4°C
zentrifugiert. Aus 4 bis 8 Vertiefungen wurde Medium (etwa 200 μl) entnommen
und in sterilen 2-ml-Gefrierphiolen
zusammengegeben. Die Proben wurden bis zur Analyse bei –70°C gehalten.
-
Interferon-Analyse/Berechnung
-
Die
Bestimmung von Interferon erfolgt mittels Bioassay unter Verwendung
von mit Encephalomyocarditis provozierten Humanlungenkarzinomzellen
A549. Die Einzelheiten dieser Bioassay-Methode sind von G.L. Brennan
und L.H. Kronenberg in "Automated
Bioassay of Interferons in Micro-test Plates", Biotechniques, Juni/Juli, 78, 1983,
beschrieben worden, worauf hiermit ausdrücklich Bezug genommen wird.
Kurz gesagt geht man hierbei folgendermaßen vor: Interferonverdünnungen
und A549-Zellen werden 12 bis 24 Stunden bei 37°C inkubiert. Die inkubierten
Zellen werden dann mit einem Inoculum des Encephalomyocarditis-Virus
infiziert. Die infizierten Zellen werden eine weitere Periode bei
37°C inkubiert,
wonach die cytopathische Wirkung des Virus quantitativ bestimmt
wird. Die quantitative Bestimmung der cytopatischen Wirkung des
Virus erfolgt durch Anfärbung
und anschließende
spektralphotometrische Extinktionsmessungen. Die Ergebnisse werden als
Alpha-Referenzeinheiten/ml
auf der Basis des für
NIH-HU-IF-L-Standard
erhaltenen Werts ausgedrückt. Durch
Prüfung
in Schachbrett-Neutralisationsassays gegen Hase-Antihumaninterferon (beta) und Ziege-Antihumaninterferon
(alpha) unter Verwendung von mit Encephalomyocarditis-Virus provozierten
A549-Zellenmonoschichten
wurde festgestellt, daß es
sich bei dem Interferon im wesentlichen ausschließlich um
Interferon alpha handelte.
-
In
der nachstehenden Tabelle gibt "+" an, daß die Verbindung
bei der jeweiligen Konzentration Interferon α induzierte, "–" gibt an, daß die Verbindung bei der jeweiligen
Konzentration Interferon α nicht
induzierte, und "±" gibt an, daß die Ergebnisse
bei der jeweiligen Konzentration zweideutig waren.
-
-
Die
vorliegende Erfindung ist an Hand von einigen Ausführungsformen
beschrieben worden. Die vorhergehende ausführliche Beschreibung und die
Beispiele wurden lediglich zum Zweck der Klarheit des Verständnisses
angeführt
und sollen die Erfindung nicht unnötig einschränken. Wie für den Fachmann leicht ersichtlich
ist, können
an den beschriebenen Ausführungsformen Änderungen
vorgenommen werden, ohne dabei den Grundgedanken und den Schutzbereich
der Erfindung zu verlassen. Daher sollte der Schutzbereich der Erfindung
nicht auf die genauen Einzelheiten der hier beschriebenen Zusammensetzungen
und Strukturen, sondern vielmehr durch den Wortlaut der folgenden
Ansprüche
beschränkt
sein.