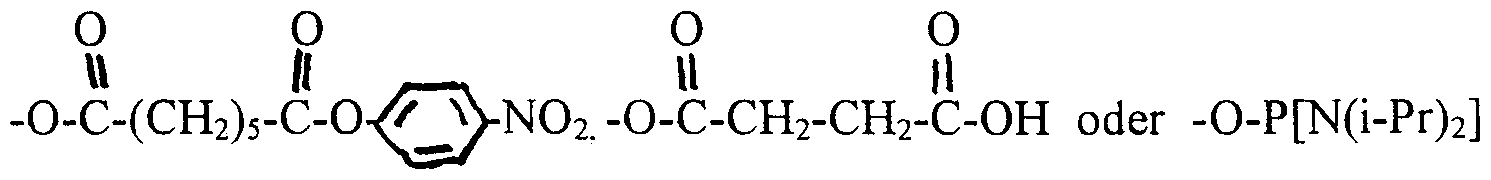Pentopyranosyl-Nucleosid, seine Herstellung und Verwendung
ie vorliegende Erfindung betrifft ein Pentopyranosyl-Nucleosid der Formel (I) oder der Formel (II)
(I) (II),
deren Herstellung und Verwendung zur Herstellung eines Therapeutikums, Diagnostikums und/oder elektronischen Bauteils
Pyranosyl-Nucleinsauren (p-NA's) sind im allgemeinen zur naturlichen RNA isomere Strukturtypen, bei denen die Pentose-Einheiten in der Pyranoseform vorliegen und durch Phosphodiestergruppen zwischen den Positionen C-2' und C-4' repetitiv verknüpft sind (Fig 1) Unter "Nucleobase" werden dabei die kanonischen Nucleobasen A, T, U, C, G, aber auch die Paare Isoguanin/Isocytosin und 2,6-Diamιnopuπn/Xanthin und im Sinne der vorliegenden Erfindung auch andere Purine und Pyrimidine verstanden p-NA's, und zwar die von der Ribose abgeleitete p-RNA's, wurden zum erstenmal von Eschenmoser et al beschrieben (siehe Pitsch, S et al Helv Chim Acta 1993, 76, 2161, Pitsch, S et al. Helv Chim Acta 1995, 78, 1621, Angew Chem 1996, 108, 1619-1623) Sie bilden ausschließlich sogenannte Watson-Crick-gepaarte, d h Purin-Pyrimidin- und Puπn-Purin-gepaarte, antiparallele, reversibel „schmelzende", quasi-lineare und stabile Duplices Homochirale p- RNA-Strange entgegengesetzten Chiralitatssinns paaren ebenfalls kontrollierbar und sind in
der gebildeten Duplex streng mcht-hehcal. Diese für den Aufbau supramolekularer Einheiten wertvolle Spezifitat hangt mit der relativ geringen Flexibilität des Ribopyranosephosphat-Ruckgrats sowie mit der starken Neigung der Basenebene zur Strangachse und der hieraus folgenden Tendenz zu mtercatenarer Basenstapelung im resultierenden Duplex zusammen und laßt sich letzlich auf die Teilnahme eines 2',4'-cis- disubstituierten Ribopyranoserings am Aufbau des Ruckgrates zurückfuhren Diese wesentlich besseren Paarungseigenschaften machen p-NA's gegenüber DNA und RNA für die Anwendung des Aufbaus supramolekularer Einheiten zu bevorzugten Paarungssystemen Sie bilden ein zu naturlichen Nucleinsauren orthogonales Paarungsystem, d h sie paaren nicht mit in der natürlich Form vorkommenden DNA's und RNA's, was im besonderen im diagnostischen Bereich von Bedeutung ist
Eschenmoser et al (1993, supra) hat zum ersten Mal eine p-RNA, wie in Fig 2 dargestellt und nachstehend erläutert, hergestellt
Ffierbei wurde eine geeignete geschützte Nucleobase mit dem Anomerengennsch der Tetrabenzoyl-Ribopyranose durch Einwirken von Bis(tπmethylsilyl)acetamιd und einer Lewis-Saure wie z B Tπmethylsilyl-tπfluormethansulfonat zur Reaktion gebracht (analog H Vorbruggen, K Krolikiewicz, B Bennua. Chem Ber 1981, 1 14, 1234 ) Unter Baseneinwirkung (NaOH in THF/Methanol/Wasser im Falle der Purine, gesättigter Ammoniak in MeOH im Falle der Pyπmidine) wurden die Acylschutzgruppen vom Zucker abgespalten, und das Produkt unter saurer Katalyse mit p-Anisaldehyddimethylacetal in 3',4'-Posιtιon geschützt Das Diastereomerengemisch wurde in 2'-Stellung acyliert. das 3',4'- methoxybenzylidengeschutzte 2'-Benzoat durch saure Behandlung, z B mit Trifluoressigsaure in Methanol deacetalisiert, und mit Dimethoxytπtylchloπd umgesetzt Die 2'- 3 '-Wanderung des Benzoats wurde durch Behandlung mit p-Nitrophenol/4- (Dimethylamino)pyridin/Triethylamin/Pyridin/n-Propanol eingeleitet Fast alle Reaktionen wurden durch Säulenchromatographie aufgearbeitet Der so synthetisierte Schlusselbaustein, das 4'-DMT-3'-benzoyl-l'-Nucleobasen-Derivat der Ribopyranose, wurde dann zum Teil phosphityhert bzw über einen Linker an eine feste Phase gebunden
Bei der anschließenden automatisierten Oligonucleotidsynthese wurde die tragergebundene Komponente in 4'-Positιon wiederholt sauer entschutzt, ein Phosphoramidit unter Einwirkung eines Kupplungsreagenz, z B ein Tetrazoldeπvat, angekuppelt, noch freie 4'- Sauerstoffatome acetyliert und das Phosphoratom oxidiert, um so das oligomere Produkt zu erhalten Anschließend wurden die restlichen Schutzgruppen abgespalten, das Produkt über HPLC gereinigt und entsalzt.
Das beschriebene Verfahren von Eschenmoser et al (1993, supra) zeigt jedoch folgende Nachteile
1 Der Einsatz nicht anomerenreiner Tetrabenzoyl-pentopyranosen (H G Fletcher J Am Chem Soc 1955, 77, 5337) zur Nucleosidierungsreaktion mit Nucleobasen verringert durch die Notwendigkeit rigoros geschnittener Chromatographien in den nachfolgenden Arbeitsschritten die Ausbeuten des Endproduktes
2. Die Synthese ist mit fünf Reaktionsstufen, ausgehend von Ribopyranosen, die in 1'- Stellung eine Nucleobase aufweisen, bis zum geschützten 3'-Benzoat, sehr langwierig und eine Durchführung im industriellen Maßstab ist kaum möglich Zusatzlich zu dem hohen Zeitaufwand sind die erhaltenen Ausbeuten an Monomerbausteinen gering 29 % im Falle des Puπnbausteins Adenin, 24 % im Falle des Pyπmidinbausteins Uracil
3 Bei der Synthese der Oligonucleotide wird 5-(4-Nιtrophenyl)-lH-tetrazol als Kupplungsreagenz in der automatisierten p-RNA- Synthese eingesetzt Die Konzentration dieses Reagenz in der Losung von Tetrazol in Acetonitπl ist dabei so hoch, daß regelmäßig das 5-(4-Nιtrophenyl)-lH-tetrazols in den dünnen Schlauchen des Synthesizers auskristallisiert und die Synthese somit zu einem vorzeitigen Ende kommt Zudem wurde beobachtet, daß die Oligomeren mit 5-(4-Nitrophenyl)-lH-tetrazol verunreinigt waren
4 Die beschriebene Aufarbeitung von p-RNA-Oligonucleotiden, im speziellen die Abspaltung der basenlabilen Schutzgruppen mit Hydrazinlosung, gelingt bei hohem
Thymidin- Anteil im Oligomeren nicht immer
Aufgabe der vorliegenden Erfindung war es daher, neue Pentopyranosyl-Nucleoside und ein Verfahren zu deren Herstellung bereitzustellen, bei dem die Herstellung der Pentopyranosyl- Nucleoside im größeren Maßstab als nach bekannten Verfahren ermöglicht werden soll und die oben beschriebenen Nachteile vermieden werden.
Ein Gegenstand der vorliegenden Erfindung ist daher ein Pentopyranosyl-Nucleosid der Formel (I),
(I), worin
R1 gleich H. OH. Hai mit Hai gleich Br oder Cl, oder ein Rest ausgewählt aus
-OH oder -O-P[N(i-Pr)
2] (OCH
2CH
2CN)
mit i-Pr gleich Isopropyl, R
2, R
3 und R
4 unabhängig voneinander, gleich oder verschieden, jeweils H, Hai mit Hai gleich Br oder Cl, NR
5R
6, OR
7, SR
8, =O, C
nH
2n+ι mit n eine ganze Zahl von 1-12, vorzugsweise 1-8, insbesondere 1-4, eine ß-eliminierbare Gruppe, vorzugsweise eine Gruppe der Formel -OCH
2CH R
18 mit R
18 gleich ein Cyano- oder p- Nitrophenylrest oder ein Fluorenylmethyloxycarbonyl-(Fmoc)-Rest, oder (C
nH
2n)NR
10R
n mit R
,0R
n gleich H,
oder R
10R
π verbunden über einen Rest der Formel
(in), woπn R12, R13, R14 und R15 unabhängig voneinander, gleich oder verschieden, jeweils H, OR7, wobei R7 die oben genannte Bedeutung hat, oder CnH2n+ι, oder CnH2n-ι, wobei n die oben genannte Bedeutung hat. bedeuten und
R3, R6, R und R8 unabhängig voneinander, gleich oder verschieden jeweils H, CnH n. i, oder CnH2n-ι, wobei n die oben genannte Bedeutung hat, -C(O)R9 mit R9 gleich ein linearer oder verzweigter, gegebenenfalls substituierter Alkyl-, Aryl-, vorzugsweise Phenyl-Rest, X, Y und Z unabhängig voneinander, gleich oder verschieden, jeweils =N-, =C(R16)- oder - N(R17)- mit R16 und R17 unabhängig voneinander, gleich oder verschieden, jeweils H oder CnH2n+ι oder (CnH n)NR10Rn mit den oben genannten Bedeutungen, bedeutet, und Sei und Sc2 unabhängig voneinander, gleich oder verschieden, jeweils H oder eine Schutzgruppe ausgewählt aus einer Acyl-, Tπtyl- oder Allyloxycarbonylgruppe, - orzugsweise eine Benzoyl- oder 4, 4'-Dιmethoxytπtyl-(DMT-)gruppe,
oder der Formel (II)
(II),
woπn R1 gleich H, OH , Hai mit Hai gleich Br oder Cl oder oder ein Rest ausgewählt aus
-OH oder -O-P[N(ι-Pr)
2] (OCH
2CH
2CN)
mit l-Pr gleich Isopropyl, R ,R und R
4 unabhängig voneinander, gleich oder verschieden, jeweils H, Hai mit Hai gleich Br oder Cl, =O, C
nH
2n+ι oder C
nH
2n-ι, eine ß-elimmierbare Gruppe, vorzugsweise eine Gruppe der Formel -OCH
2CH
2R
18 mit R
18 gleich ein Cyano- oder p-Nitrophenylrest oder ein Fluorenylmethyloxycarbonyl-(Fmoc)-Rest oder (C
nH
2n)NR R , wobei R , R , unabhängig voneinander die oben genannte Bedeutung von R
I0 bzw R
11 hat, und X', jeweils =N-, =C(R
16 )- oder -N(R
17')- bedeutet, wobei R
16 und R
17 unabhängig voneinander die oben genannte Bedeutung von R
16 bzw R
17 haben, und S
ci bzw S
L2 die oben genannte Bedeutung von S
c] bzw S
c2 haben ausgenommen 4'-DMT-3 '-benzoyl-πbopyranosyl-N-benzoyl-adenosin, N
6,N
6-Dιbenzoyl-9- (2'-O-benzoyl-ß-D-πbo-pyranosyl)-adenosιn, Ribopyranosyl-N-benzoyl-adenosin, 4 -DMT- 3'-benzoyl-πbopyranosyl-urazιl und Ribopyranosyl-urazil
Das erfindungsgemaße Pentopyranosyl-Nucleosid ist im allgemeinen ein Ribo-, Arabino-, Lyxo- und/oder Xylo-pyranosyl-Nucleosid, vorzugsweise ein Ribopyranosyl-Nucleosid, wobei der Pentopyranosyl-Teil D-konfiguπert aber auch L-konfiguπert sein kann
Üblicherweise handelt es sich bei dem erfindungsgemaßen Pentopyranosvl-Nucleosid um ein Pentopyranosyl-puπn, -2,6-dιamιnopuπn, -6-puπnthιol, -pyπdin, -pyπmidin, -adenosin, - guanosin, -isoguanosin, -6-thιoguanosιn, -xanthin, -hypoxanthin, -thymidin, -cytosin, - isocytosin , -mdol, -tryptamm, -N-phthaloyltryptamin, -uracil, -coffein, -theobromm, - theophyl n, -benzotπazol oder -acπdin, insbesondere um ein Pentopyranosyl-puπn, - pyπmidin, -adenosin, -guanosin, -thymidin, -cytosin, tryptamm, -N-phthalotryptamin oder - uracil
Unter die erfindungsgemaßen Verbindungen fallen auch Pentopyranosyl-Nucleoside, die als Linker verwendet werden können, d h als Verbindungen mit funktioneilen Gruppen, die kovalent an Biomolekule, wie z B in ihrer natürlichen Form vorkommende oder
modifizierte Nucleinsauren, wie DNA, RNA aber auch p-NA's, vorzugsweise pRNA's, binden können Dies ist überraschend, da für p-NA's noch keine Linker bekannt sind
Beispielsweise fallen hierunter Pentopyranosyl-Nucleoside, bei denen R2, R3, R4, R2 , R3 und/oder R4 ein 2-Phthalιmidoethyl- oder Allyloxy-Rest bedeutet Bevorzugt sind gemäß der vorliegenden Erfindung beispielsweise Uracil-basierende Linker, bei denen vorzugsweise die 5 -Position des Uracils modifiziert wurde, z B N- Phthaloylaminoethyluracil, aber auch Indol-basierende Linker, vorzugsweise Tryptamindeπvate, wie z B N-Phthaloyltryptamin
Überraschenderweise werden durch die vorliegende Erfindung auch besser handhabbare Pentopyranosyl-N,N-Dιacylnucleoside, vorzugsweise Puπne, insbesonders Adenosin, Guanosin oder 6-Thιoguanosιn, bereitgestellt, deren Nucleobase auf einfache Weise vollkommen entschutzt werden können Daher gehören zu der Erfindung auch erfindungsgemaße Pentopyranosyl-Nucleoside, bei denen R2, R3, R4, R2 , RJ und/oder R4 ein Rest der Formel -N[C(O)R9]2 bedeutet, insbesondere N6, N6-Dibenzoyl-9-(ß-D- ribopyranosyl)-adenosιn
Weiterhin ist es überraschend, daß die vorliegende Erfindung Pentopyranosyl-Nucleoside bereitstellt, die ausschließlich am 3 '-Sauerstoffatom des Pentopyranosid-Teils eine Schutzgruppe, vorzugsweise eine basen- oder metallkatalysiert abspaltbare Schutzgruppe, insbesondere eine Acylgruppe, besonders bevorzugt eine Benzoylgruppe, tragen Diese Verbindungen dienen z B als Ausgangsstoffe zur direkten Einführung einer weiteren Schutzgruppe, vorzugsweise einer saure- oder basenlabilen Schutzgruppe, insbesondere einer Tritylgruppe, besonders bevorzugt eine Dimethoxytπtylgruppe, an das 4'- Sauerstoffatom des Pentopyranosid-Teils ohne zusatzliche, die Ausbeute verringernde Schritte, wie z B zusatzliche Reinigungsschritte
Daruberhinaus stellt die vorliegende Erfindung Pentopyranosyl-Nucleoside bereit, die ausschließlich am 4' -Sauerstoffatom des Pentopyranosid-Teils eine Schutzgruppe, vorzugsweise einer saure- oder basenlabilen Schutzgruppe, insbesondere einer Tritylgruppe, besonders bevorzugt eine Dimethoxytπtylgruppe, tragen Auch diese Verbindungen dienen
z. B. als Ausgangsstoffe zur direkten Einführung einer weiteren Schutzgruppe, vorzugsweise einer basen- oder metallkatalysiert abspaltbaren Schutzgruppe, insbesondere einer Acylgruppe, besonders bevorzugt einer Benzoylgruppe, z. B. an dem 2'- Sauerstoffatom des Pentopyranosid-Teils, ohne zusätzliche, die Ausbeute verringernde Schritte, wie z. B. zusätzliche Reinigungsschritte.
Im allgemeinen können die erfindungsgemäßen Pentopyranosid-Nucleoside in einer sogenannten Ein-Topf-Reaktion umgesetzt werden, was die Ausbeuten erhöht und daher besonders vorteilhaft ist.
Folgende Verbindungen stellen bevorzugte Beispiele der erfindungsgemäßen Pentopyranosyl-Nucleoside dar:
A) [2',4'-Di-O-Benzoyl)-ß-ribopyranosyl]-Nucleoside, insbesondere ein [2',4'-Di-O- Benzoyl)-ß-ribopyranosyl]-adenin, - guanin, -cytosin, -thymidin, -uracil, -xanthin oder - hypoxanthin, sowie ein N-Benzoyl-2',4'-di-O-benzoyl-ribopyranosyl-Nucleosid, insbesondere ein -adenin, - guanin oder -cytosin, sowie ein N-Isobutyroyl-2', 4'-di-O- benzoyl-ribopyranosyl-Nucleosid, insbesondere ein -adenin, -guanin oder -cytosin, sowie ein O6-(2-Cyanoethyl)-N2-isobutyroyl-2',4'-di-O-benzoyl-ribopyranosyl-Nucleosid, insbesondere ein -guanin, sowie ein O6 (2-(4-Nitrophenyl)ethyl)-N2-isobutyroyl-2'.4'-di-O- benzoyl-ribopyranosyl-Nucleosid, insbesondere ein -guanin.
B) ß-Ribopyranosyl-Nucleoside, insbesondere ein ß-Ribopyranosyl-adenin, -guanin, - cytosin, -thymidin oder -uracil, -xanthin oder hypoxanthin, sowie ein N-Benzoyl-, N- Isobutyroyl-, O6 -(2-Cyanoethyl)- oder O6-(2-(4-Nitrophenyl)ethyl)-N2-isobutylroyl-ß- ribopyranosyl-Nucleosid.
C) 4'-DMT-pentopyranosyl-Nucleoside, vorzugsweise ein 4'-DMT-ribopyranosyl- Nucleosid, insbesondere ein 4'-DMT-ribopyranosyl-adenin, -guanin, -cytosin, -thymidin, - uracil, -xanthin, oder -hypoxanthin, sowie ein N-Benzoyl-4'-DMT-ribopyranosyl-Nucleosid, insbesondere ein N-Benzoyl-4'-DMT-ribopyranosyl-adenin, -guanin oder -cytosin, sowie ein N-Isobutyroyl-4'-DMT-ribopyranosyl-Nucleosid, insbesondere ein N-Isobutyroyl-4'-
DMT-ribopyranosyl-adenin, -guanin oder -cytosin sowie ein O6-(2-Cyanoethyl)-N2- isobutyroyl-4'-DMT-ribopyranosyl-Nucleosid, insbesondere ein O6-(2-Cyanoethyl)-N2- isobutyroyl-4'-DMT-ribopyranosyl-guanin, sowie ein O6-(2-(-4-Nitrophenyl)ethyl)-N2- isobutyroyl-4'-DMT-ribopyranosyl-Nucleosid, insbesondere ein O6-(2-(-4- Nitrophenyl)ethyl)-N2-isobutyroyl-4'-DMT-ribopyranosyl-guanin.
D) ß-Ribopyranosyl-N,N'-dibenzoyl-adenosin oder ß-Ribopyranosyl-N,N'-dibenzoyl- guanosin.
Als Vorstufe für die Oligonucleotidsynthese eigenen sich beispielsweise 4'-DMT- pentopyranosyl-Nucleoside-2'-phosphitamid/-H-phosphonat, vorzugsweise ein 4'DMT- ribopyranosyl-Nucleosid-2'-phosphitamid/-H-phosphonat, insbesondere ein 4'-DMT- ribopyranosyl-adenin-, -guanin-, cytosin-, -thymidin-, -xanthin-, oder -hypoxanthin-, oder - uracil-2'-phosphitamid/-H-phosphonat sowie ein N-Benzoyl-4'-DMT-ribopyranosyl-adenin- , -guanin- oder -cytosin-2'-phosphitamid/-H-phosphonat sowie ein N-Isobutylroyl-4'-DMT- ribopyranosyl-adenin-, -guanin- oder -cytosin-2'-phosphitamid/-H-phosphonat, O6-(2- Cyanoethyl)-4'-DMT-ribopyranosyl-guanin-, -xanthin-, -hypoxanthin-2'-phosphitamid/-H- phosphonat oder O6-(2-(4-Nitrophenyl)ethyl)-N2-isobutyroyl-4'-DMT-ribopyranosyl-guanin und für die Kopplung an den festen Träger beispielsweise 4'-DMT-pentopyranosyl- \'ucleoside-2'-succinat, vorzugsweise ein 4'-DMT-ribopyranosyl-Nucleosid-2'-succinat, insbesondere ein 4'DMT-ribopyranosyl-adenin-, -guanin-, -cytosin-, -thymidin-, -xanthin-, - hypoxanthin- oder -uracil-2' -succinat sowie ein N-Benzoyl-4'-DMT-ribopyranosyl-adenin-, -guanin- oder -cytonsin-2'- succinat sowie ein N-Isobutyroyl-4'-DMT-ribopyranosyl-adenin- . -guanin- oder -cytosin-2'- succinat, O-(2-Cyanoethyl)-4'-DMT-ribopyranosyl-guanin-, - xanthin- oder -hypoxanthin-2'- succinat sowie ein O6-(2-(4-Nitrophenyl)ethyl)-N2- isobutyroyl-4'-DMT-ribopyranosyl-guanin-2'-succinat.
Ein weiterer Gegenstand der vorliegenden Erfindung ist ein Verfahren zur Herstellung eines erfindungsgemäßen Pentopyranosyl-Nucleosids der Formel (I) oder (II), bei dem ausgehend von dem ungeschützten Pentopyranosid
(a) in einem ersten Schritt zuerst die 2'-, 3'- oder 4'-Position des Pentopyranosids geschützt wird, und vorzugsweise
(b) in einem zweiten Schritt die andere Position an der 2'-, 3'- oder 4'-Position.
Das erfindungsgemaße Verfahren ist nicht auf die in der zitierten Literatur beschriebenen Nucleobasen beschränkt, sondern kann überraschenderweise mit einer Vielzahl von naturlichen und synthetischen Nucleobasen erfolgreich durchgeführt werden. Zudem ist es besonders überraschend, daß das erfindungsgemäße Verfahren im Vergleich zu dem literaturbekannten Verfahren in großen Ausbeuten und mit einer Zeitersparnis von durchschnittlich 60% durchgeführt werden kann, was für die industrielle Anwendung besonders vorteilhaft ist. Zusatzlich sind mit dem erfindungsgemaßen Verfahren die bei dem in der Literatur beschriebenen Verfahren notigen Reinigungsschritte, z B. chromatographische Zwischenreinigungen, nicht notwendig und die Reaktionen können teilweise als sogenannnte Ein-Topf-Reaktion durchgeführt werden, was die Raum/Zeit- Ausbeuten deutlich erhöht
In einer besonderen Ausführungsform erfolgt im Falle einer 2 '-geschützten Position eine Umlagerung der Schutzgruppe von der 2'-Position zur 3 '-Position, die im allgemeinen in Gegenwart einer Base, insbesondere in Gegenwart von N-Ethyldiisopropylamin und/oder Triethylamin durchgeführt wird Diese Reaktion kann gemäß der vorliegenden Erfindung besonders vorteilhaft in dem gleichen Reaktionsbehaltnis als Ein-Topf-Reaktion durchgeführt werden
In einer weiteren bevorzugten Ausführungsform ist das Pyranosyl-nucleosid durch eine saurelabile, basenlabile oder metallkatalysiert abspaltbare Schutzgruppe Scι, Sc2, Scr oder Sc2- geschützt, wobei vorzugsweise die Schutzgruppen Sc! und Scr von den Schutzgruppen So2 bzw Sc2- verschieden sind.
Im allgemeinen handelt es sich bei den genannten Schutzgruppen um eine Acylgruppe, vorzugsweise um eine Acetyl-, Benzoyl-, Nitrobenzoyl- und/oder Methoxybenzoyl-Gruppe, um Tritylgruppen, vorzugsweise um eine 4, 4'-Dimethoxytrityl-(DMT)-Gruppe oder um eine ß-eliminierbare Gruppe, vorzugsweise eine Gruppe der Formel -OCH2CH2R18 mit R18 gleich ein Cyano- oder p-Nitrophenylrest oder eine Fluorenylmethyloxycarbonyl- (Fmoc)Gruppe.
Besonders bevorzugt ist es, wenn die 2'- oder 3 '-Position durch eine basenlabile oder metallkatalysiert abspaltbare Schutzgruppe, vorzugsweise durch eine Acylgruppe, insbesondere durch eine Acetyl-, Benzoyl-, Nitrobenzoyl- und/oder Methoxybenzoylgruppe, geschützt wird und/oder die 4' -Position durch eine saure- oder basenlabile Schutzgruppe, vorzugsweise durch eine Trityl- und/oder Fmoc-Gruppe, insbesondere durch eine DMT- Gruppe geschützt wird.
Das erfindungsgemaße Verfahren kommt folglich im Gegensatz zu dem literaturbekannten Verfahren ohne acetalische Schutzgruppen, wie Acetale oder Ketale, aus, was zusatzliche chromatographische Zwischenreinigungen vermeidet und folglich die Reaktionen als EinTopf-Reaktionen mit überraschend hohen Raum/Zeit-Ausbeuten durchführen laßt
Die Einführung der genannten Schutzgruppen erfolgt vorzugsweise bei tiefen Temperaturen, da diese hierdurch überraschenderweise selektiv eingeführt werden können.
So erfolgt beispielsweise die Einführung einer Benzoylgruppe durch Umsetzen mit Benzoylchlorid in Pyridin bzw in einem Pyridin/Methylenchlorid-Gemisch bei tiefen Temperaturen Die Einführung einer DMT-Gruppe kann beispielsweise durch Umsetzen mit DMTCl in Anwesenheit einer Base, z B von N-Ethyldiisopropylamin (Hunig-Base), und z B von Pyridin, Methylenchlorid oder einem Pyridin/Methylenchloπd-Gemisch bei Raumtemperatur erfolgen
Es ist auch vorteilhaft, wenn nach der Acylierung und/oder nach der gegebenenfalls erfolgten Umlagerung von der 2'- zu der 3'-Position die Reaktionsprodukte chromatographisch gereinigt werden Eine Reinigung nach der Tritylierung ist gemäß dem erfindungsgemaßem Verfahren nicht notwendig, was besonders vorteilhaft ist.
Das Endprodukt kann, falls notwendig, noch durch Kristallisation weiter gereinigt werden.
Ein anderer Gegenstand der vorliegenden Erfindung ist ein Verfahren zur Herstellung eines R bopyranosyl-nucleosids, bei dem
(a) eine geschützte Nucleobase mit einer geschützten Ribopyranose umgesetzt wird,
(b) die Schutzgruppen von dem Ribopyranosyl-Teil des Produktes aus Schritt (a) abgespalten werden, und
(c) das Produkt aus Schritt (b) gemäß dem oben naher beschriebenen Verfahren umgesetzt wird.
Hierbei ist es zur Vermeidung weiterer zeit- und materialaufwendiger Chromatographien vorteilhaft, nur anomerenreine geschützte Pentopyranosen, wie z. B Tetrabenzoyl- pentopyranosen, vorzugsweise ß-Tetrabenzoyl-ribopyranosen (R. Jeanloz, J Am. Chem. Soc 1948. 70, 4052), einzusetzen.
In einer weiteren Ausführungsform wird ein Linker gemäß Formel (II), worin R4 (CnH2n)NR10,Ru' bedeutet und RltrRι r über einen Rest der Formel (III) mit der bereits bezeichneten Bedeutung verbunden ist, durch folgendes Verfahren auf vorteilhafte Weise hergestellt:
(a) eine Verbindung der Formel (II) mit R4 gleich (CnH2n)OSc3 oder (CnH2n)Hal, worin n die oben genannte Bedeutung hat, Sc3 eine Schutzgruppe, vorzugsweise eine Mesylat-Gruppe, und Hai Chlor oder Brom bedeutet, wird mit einem Azid, vorzugsweise in DMF, umgesetzt, anschließend wird (b) das Reaktionprodukt aus (a), vorzugsweise mit Triphenylphosphin z B in Pyridin reduziert, dann
(c) das Reaktionsprodukt aus (b) mit einem entsprechenden Phthalimid, z B N- Ethoxycarbonylphthalimid, umgesetzt, und
(d) das Reaktionsprodukt aus (c) mit einer entsprechenden geschützten Pyranose, z. B. Ribosetetrabenzoat, umgesetzt, und schließlich
(e) werden die Schutzgruppen, z. B mit Methylat, abgespalten, und
(f) die weiteren Schritte, wie oben bereits beschrieben, durchgeführt.
Daneben weisen Indolderivate als Linker den Vorzug der Fluoreszenzfahigkeit auf und sind daher für Nanotechnologie-Anwendungen, bei denen es ggf. um den Nachweis kleinster
Substanzmengen geht, besonders bevorzugt. So wurden Indol-1-riboside bei N. N Suvorov et al., Biol. Aktivn. Soedin., Akad. Nauk SSSR 1965, 60 und Tetrahedron 1967, 23, 4653
bereits beschrieben. Allerdings gibt es kein analoges Verfahren, 3 -substituierte Derivate herzustellen.. Im allgemeinen erfolgt ihre Herstellung über die Bildung eines Aminals der ungeschützten Zuckerkomponente und einem Indolin, welches dann durch Oxidation in das Indol-1-ribosid übergeführt wird. Beschrieben wurden z. B. Indol-1-glucoside und -1- arabinoside (Y. V. Dobriynin et al, Khim.-Farm. Zh. 1978, 12, 33), deren 3 -substituierte Derivate meist über Vielsmeier-Reaktion hergestellt wurden. Dieser Weg der Einführung von Aminoethyl-Einheiten in 3 -Position des Indols ist für eine industrielle Anwendung jedoch zu aufwendig.
In einer weiteren besonderen Ausführungsform wird daher ein Linker gemäß Formel (I), worin X und Y unabhängig voneinander, gleich oder verschieden, jeweils =C(R16) mit R16 gleich H oder C„H2n und Z =C(R16)- mit R16 gleich (CnH2n)NR10Ru durch folgendes Verfahren auf vorteilhafte Weise hergestellt:
(a) das entsprechende Indolin, z. B. N-Phthaloyltryptamin, wird mit einer Pyranose, z. B. D-Ribose, zum Nucleosidtriol umgesetzt, dann werden
(b) die Hydroxylgruppen des Pyranosyl-Teils des Produktes aus (a) vorzugsweise mit Acylgruppen, z. B. mittels Essigsäureanhydrid, geschützt, anschließend wird
(c) das Produkt aus (b), z. B. durch 2,3-Dichlor-5,6-dicyanoparachinon, oxidiert, und
(d) die Hydroxyl-Schutzgruppen des Pyranosyl-Teils des Produktes aus (c) werden z. B. mittels Methylat abgespalten und anschließend werden
(e) die weiteren Schritte, wie oben bereits beschrieben, durchgeführt.
Dieses Verfahren läßt sich jedoch nicht nur bei Ribopyranosen anwenden, sondern auch bei Ribofüranosen und 2'-Deoxyribofüranosen bzw. 2'-Deoxyribopyranosen, was besonders vorteilhaft ist. Als Nucleosidierungspartner der Zucker wird vorzugsweise Tryptamin, insbesondere N-Acylderivate des Tryptamins, vor allem N-Phthaloyltryptamin verwendet.
In einer weiteren Ausführungsform werden die 4'- geschützten, vorzugsweise, die 3', 4'- geschützten Pentopyranosyl-Nucleoside in einem weiteren Schritt phosphityliert oder an eine feste Phase gebunden.
Die Phosphitylierung erfolgt beispielsweise durch Phosphorigsäuremonoallylester- diisopropyl-amidchlorid in Anwesenheit einer Base, z. B. N-Ethyldiisopropylamin oder durch Phosphortrichlorid und Imidazol bzw. Tetrazol und nachfolgender Hydrolyse unter Basenzusatz. Im ersten Fall ist das Produkt ein Phosphoramidit und im zweiten Fall ein H- Phosphonat. Die Bindung eines geschützten erfindungsgemäßen Pentopyranosyl-Nucleosids an eine feste Phase, z. B. „long-chain-alkylamino-controlled pore glass" (CPG, Sigma Chemie, München) kann beispielsweise wie bei Eschenmoser et al. (1993) beschrieben erfolgen.
Die erhaltenen Verbindungen dienen z. B. für die Herstellung von Pentopyranosyl- Nucleinsäuren.
Ein weiterer Gegenstand der vorliegenden Erfindung ist daher ein Verfahren zur Herstellung einer Pentopyranosyl-Nucleinsäure, mit folgenden Schritten: (a) in einem ersten Schritt wird ein geschütztes Pentopyranosyl-Nucleosid, wie oben bereits beschrieben, an eine feste Phase gebunden wird und
(b) in einem zweiten Schritt wird das gemäß Schritt (a) an eine feste Phase gebundene 3'-, 4'-geschützte Pentopyranosylnukleosid um ein phosphityliertes 3'-, 4 '-geschütztes Pentopyranosyl-Nucleosid verlängert und anschließend z. B. durch eine wäßrige Jodlösung oxidiert wird, und
(c) Schritt (b) solange mit gleichen oder unterschiedlichen phosphitylierten 3'-, 4'- geschützten Pentopyranosyl-Nucleosiden wiederholt, bis die gewünschte Pentopyranosyl- Nucleinsäure vorliegt.
Als Kupplungsreagenz bei Einsatz von Phosphoramiditen eignen sich saure Aktivatoren wie Pyridinium-Hydrochlorid besonders Benzimidazoliumtriflat, vorzugsweise nach Umkristallisieren in Acetonitril und nach Lösen in Acetonitril, da im Gegensatz zu 5-(4- Nitrophenyl)-lH-tetrazol als Kupplungsreagenz keine Verstopfung der Kupplungsreagenz- Leitungen und eine Verunreinigung des Produktes erfolgt.
Als Kupplungsreagenz beim Einsatz von H-Phosphonaten eignen sich besonders Arylsulfonylchloride, Diphenylchlorophosphat, Pivaloylchlorid oder Adamantoylchlorid.
Weiterhin ist es vorteilhaft durch Zusatz von einem Salz, wie Natπumchlorid, zur schutzgruppenabspaltenden Hydrazinolyse von Oligonukleotiden, insbesondere von p-NA's, vorzugsweise von p-RNA's, Pyrimidinbasen, vor allem Uracil und Thymin, vor einer Ringofϊhung zu schützen, die das Oligonukleotid zerstören wurde Allyloxygruppen können vorzugsweise durch Palladium [Pd(0)]-Komplexe z B vor der Hydrazinolyse abgespalten werden
In einer weiteren besonderen Ausführungsform können in Schritt (a) und/oder Schritt (b) auch Pentofüranosyl-nucleoside, z B das in ihrer naturlichen Form vorkommende Adenosin, Guanosin. Cytidin, Thymidin und/oder Uracil. eingebaut werden, was z B zu einer gemischten p-NA-DNA bzw p-NA-RNA führt
In einer anderen besonderen Ausführungsform kann in einem weiteren Schritt ein Allyloxy- Linker der Formel
Sc4NH(CnH n)CH(OP SC5 SQ6)CnH2nSc7
(IV),
worin SL4 und S 7 unabhängig voneinander, gleich oder verschieden, jeweils eine Schutzgruppe insbesondere ausgewählt aus Fmoc und/oder DMT,
SC5 und Sc6 unabhängig voneinander, gleich oder verschieden, jeweils eine Allyloxy- und/oder Diisopropylamino-Gruppe bedeuten, eingebaut werden n hat die bereits oben genannte Bedeutung
Ein besonders bevorzugter Allyloxy-Linker ist (2-(S)-N-Fmoc-O1-DMT-O - allyloxydιisopropylamιnophosphinyl-6-amιno- 1 ,2-hexandiol)
Ausgehend von z B Lysin können somit in wenigen Reaktionsschritten amino-terrmnale Linker aufgebaut werden, die sowohl eine aktivierbare Phosphorverbindung als auch eine
saurelabile Schutzgruppe, wie DMT, tragen und daher leicht in der automatisierbaren Oligonucleotidsynthese verwendet werden können (siehe z B P. S. Nelson et al., Nucleic Acid Res. 1989, 17, 7179, L. J. Arnold et al., WO 8902439) Das Repertoire wurde in der vorliegenden Erfindung durch einen Lysin-basierender Linker erweitert, bei dem anstelle der sonst üblichen Cyanoethyl-Gruppe am Phosphoratom eine Allyloxy-Gruppe eingebracht wurde, und welcher daher in vorteilhafter Weise in der Noyori-Oligonucleotid-Methode eingesetzt werden kann (R Noyori, J Am. Chem. Soc. 1990, 112, 1691-6)
Ein weiterer Gegenstand der vorliegenden Erfindung ist daher auch eine Pentopyranosyl- Nucleinsaure. die mindestens ein erfindungsgemaßes Pentopyranosyl-Nucleosid und gegebenenfalls mindestens einen Allyloxy-Linker enthalt.
p-NA's und insbesondere die p-RNA's bilden untereinander stabile Duplices und paaren im allgemeinen nicht mit den in ihrer naturlichen Form vorkommenden DNA's und RNA's. Diese Eigenschaft macht p-NA's zu bevorzugten Paarungssystemen.
Solche Paarungssysteme sind supramolekulare Systeme nicht kovalenter Wechselwirkung, die sich durch Selektivität, Stabilität und Reversiblitat auszeichnen, und deren Eigenschaften bevorzugt thermodynamisch, d h durch Temperatur, pH-Wert und Konzentration beeinflußt werden Solche Paarungssysteme können z B aufgrund ihrer selektiven Eigenschaften auch als „molekularer Klebstoff' für die Zusammenführung von unterschiedlichen Metallclustern zu Cluster- Verbanden mit potentiell neuen Eigenschaften verwendet werden [siehe z B R L Letsinger, et al , Nature 1996, 382, 607-9, P G Schultz et al, Nature 1996, 382, 609-11] Folglich eignen sich die p-NA's auch für die Anwendung im Bereich der Nanotechnologie, beispielsweise zur Herstellung neuer Materialien, Diagnostika und Therapeutika sowie mikroelektronischer, photonischer bzw optoelektronischer Bauteile und für das kontrollierte Zusammenführen molekularer Species zu supramolekularen Einheiten, wie z. B. für den (kombinatorischen) Aufbau von Proteinassemblies [siehe z. B. A Lombardi, J W Bryson, W F. DeGrado, Biomolekuls (Pept. Sei.) 1997, 40, 495-504], da p-NA's Paarungssysteme bilden, die stark und thermodynamisch kontrollierbar sind. Eine weitere Anwendung ergibt sich daher gerade im diagnostischen und drug discovery-B ereich durch die Möglichkeit, fünktionelle, bevorzugt
biologische Einheiten wie Proteine oder DNA/RNA- Ab schnitte, mit einem p-NA-Code zu versehen, der nicht mit den naturlichen Nucleinsauren interferiert (siehe z. B. WO93/20242).
Ein anderer Gegenstand der Erfindung ist daher die Verwendung eines erfindungsgemäßen Pentopyranosyl-Nucleosid der Formel (I) oder (II) oder einer erfindungsgemaßen Pentopyranosyl-Nucleinsäure zur Herstellung eines Arzneimittels, wie z B eines Therapeutikums, eines Diagnostikums und/oder eines elektronischen Bauteils
Ein Biomolekul, z B DNA oder RNA, kann zum mcht-kovalenten Verbinden (Linken) mit einem anderen Biomolekul. z B DNA oder R A, verwendet werden, wenn beide Biomolekule Abschnitte enthalten, die aufgrund komplementärer Sequenzen von Nucleobasen durch Ausbildung von Wasserstofϊbrucken aneinander binden können Derartige Biomolekule finden z B in analytischen Systemen zur Signalamplifizierung Verwendung, wo ein in seiner Sequenz zu analysierendes DNA-Molekul über einen solchen nicht-kovalenten DNA-Linker zum einen an einen festen Trager immobilisiert, und zum anderen an ein signalverstarkendes branchedDNA-Molekul (bDNA) gebunden werden soll (siehe z B S Urdea, Bio/Technol 1994, 12, 926 oder US-Patent Nr 5,624,802) Ein wesentlicher Nachteil der zuletzt beschriebenen Systeme ist, daß sie den Verfahren zur Nucleinsaure-Diagnostik durch Polymerase-Chain-Reaction (PCR) (K Muliis. Methods Enzymol 1987, 155, 335) hinsichtlich der Empfindlichkeit bis jetzt unterlegen sind Das ist u a. darauf zurückzuführen, daß die nicht-kovalente Bindung vom festen Trager an das zu analysierende DNA-Molekul ebenso wie die nicht-kovalente Bindung des zu analysierenden DNA-Molekuls nicht immer spezifisch erfolgt, wodurch es zu einer Vermischung der Funktionen „Sequenzerkennung" und „nicht-kovalente Bindung" kommt Die Verwendung von p-NA's als orthogonales Paarungssystem, welches nicht in das DNA- bzw RNA- Paarungsgeschehen eingreift, lost dieses Problem auf vorteilhafte Weise, wodurch die Empfindlichkeit der beschriebenen analytischen Verfahren deutlich erhöht werden kann.
Ein weiterer Gegenstand der vorliegenden Erfindung ist daher die Verwendung eines erfindungsgemaßen Pentopyranosyl-Nucleosids der Formel (I) oder (II) oder einer erfindungsgemaßen Pentopyranosyl-Nucleinsäure zur Herstellung eines Koηjugates
enthaltend ein erfindungsgemaßes Pentopyranosyl-Nucleosid der Formel (I) oder (II) oder eine erfindungsgemaße Pentopyranosyl-Nucleinsäure und ein Biomolekul
Konjugate sind im Sinne der vorliegenden Erfindung kovalent gebundene Hybπde aus p- NA's und anderen Biomolekulen, vorzugsweise em Peptid, Protein oder eine Nucleinsaure, beispielsweise ein Antikörper oder ein fünktioneller Teil davon oder eine in ihrer natürlichen Form vorkommende DNA und/oder RNA Funktioneile Teile von Antikörper sind beispielsweise Fv-Fragmente (Skerra & Pluckthun (1988) Science 240, 1038), einzelkettige Fv-Fragmente (scFv, Bird et al (1988), Science 242, 423, Huston et al (1988) Proc Natl Acad Sei U S A , 85, 5879) oder Fab-Fragmente (Better et al (1988) Science 240, 1041)
Unter Biomolekul versteht man im Sinne der vorliegenden Erfindung eine natürlich vorkommende Substanz oder eine von einer naturlich vorkommenden Substanz abgeleitete Substanz
In einer bevorzugten Ausführungsform handelt es sich dabei um p-RNA/DNA- bzw p- RNA/RNA-Konjugate
Konjugate werden dann vorzugsweise verwendet, wenn die Funktionen „Sequenzerkennung und , nicht-kovalente Bindung in einem Molekül realisiert werden müssen, da die erfindungsgemaßen Konjugate zwei zueinander orthogonale Paarungssysteme enthalten
Für die Herstellung von Konjugaten sind sowohl sequentielle als auch konvergente Verfahren geeignet
In einem sequentiellen Verfahren wird z B nach erfolgter automatisierter Synthese eines p- RNA-O gomeren direkt am gleichen Synthesizer - nach Umstellung der Reagenzien und des Kupplungsprotokolls - z B ein DNA-Oligonukleotid weitersynthetisiert Dieser Vorgang laßt sich auch in umgekehrter Reihenfolge durchführen
In einem konvergenten Verfahren werden z. B. p-RNA-Oligomere mit Aminoterminalen- Linkern und z. B. DNA-Oligomere mit z. B. Thiol-Linkern in getrennten Vorgängen synthetisiert. Anschließend erfolgt vorzugsweise eine Jodacetylierung des p-RNA- Oligomeren und die Kupplung der beiden Einheiten nach literaturbekannten Protokollen (T. Zhu et al, Biocoηjug. Chem. 1994, 5, 312).
Konvergente Verfahren erweisen sich aufgrund ihrer Flexibilität als besonders bevorzugt.
Unter dem Begriff Konjugat im Sinne der vorliegenden Erfindung sind auch sogenannte Arrays zu verstehen. Arrays sind Anordnungen von immobilisierten Erkennungsspecies, die speziell in der Analytik und Diagnostik eine wichtige Rolle bei der simultanen Bestimmung von Analyten spielen. Beispiele sind Peptide- Arrays (Fodor et al., Nature 1993, 364, 555) und Nucleinsaure- Arrays (Southern et al. Genomics 1992, 13, 1008; Heller, US-Patent Nr. 5,632,957). Eine höhere Flexibilität dieser Arrays kann dadurch erreicht werden, daß die Erkennungsspecies an codierende Oligonucleotide gebunden werden und die zugehörigen, komplementären Stränge an bestimmte Positionen auf einem festen Träger. Durch Aufbringen der codierten Erkennungsspecies auf den „anti-codierten" festen Träger und Einstellung von Hybridisierungsbedingungen werden die Erkennungsspecies an den gewünschten Positionen nicht-kovalent gebunden. Dadurch können verschiedene Typen von Erkennungsspecies, wie z. B. DNA- Abschnitte, Antikörper, nur durch Anwendung von Hybridisierungsbedingungen gleichzeitig auf einem festen Träger angeordnet werden (siehe Fig. 3.). Voraussetzung hierzu sind aber äußerst starke, selektive - um die codierenden Abschnitte möglichst kurz zu halten - und mit natürlicher Nucleinsaure nicht interferierender Codons und Anticodons notwendig. p-NA's, vorzugsweise p-RNA's eignen sich hierzu in besonders vorteilhafter Weise.
Unter dem Begriff „Träger" versteht man im Sinne der vorliegenden Erfindung Material, insbesondere Chipmaterial, das in fester oder auch gelartiger Form vorliegt. Als Trägermaterialien eignen sich beispielsweise Keramik, Metall, insbesondere Edelmetall, Gläser, Kunststoffe, kristalline Materialien bzw. dünne Schichten des Trägers, insbesondere der genannten Materialien bzw. dünne Schichten des Trägers, insbesondere der genannten Materialien, oder (bio)molekulare Filamente wie Cellulose, Gerüstproteine.
Die vorliegende Erfindung betrifft daher auch die Verwendung der erfindungsgemaßen Pentopyranosyl-Nucleinsauren, vorzugsweise Ribopyranosyl-Nucleinsauren zur Codierung von Erkennungsspecies, bevorzugt naturliche DNA- oder RNA-Strange oder Proteine, insbesondere Antikörper oder fünktionelle Teile von Antikörpern Diese können dann gemäß Fig 3 mit den zugehörigen Codons auf einem festen Trager hybridisiert werden Damit kann auf einem festen Trager, der in Form eines Arrays mit Codons ausgestattet ist, nur durch Einstellung von Hybridisierungsbedingungen mit immer neuen Kombinationen von Erkennungsspecies an den gewünschten Positionen immer neue, diagnostisch nutzliche Arrays aufgebaut werden Wird dann der Analyt, beispielsweise eine biologische Probe wie Serum o a aufgebracht, dann werden die zu detektierenden Species in einem bestimmten Muster auf dem Array gebunden, welches dann indirekt (z B durch Fluoreszenzmarkierung der Erkennungsspecies) oder direkt (z B durch Impedanzmessung am Anknüpfungspunkt der Codons) registriert wird Dann wird die Hybridisierung durch geeignete Bedingung aufgehoben (Termperatur, Salze, Lösungsmittel, elektrophoretische Vorgange) so daß wieder nur der Trager mit den Codons zurückbleibt Dieser wird dann erneut mit anderen Erkennungsspecies beladen und wird z. B für den gleichen Analyten für die Ermittlung eines anderen Musters verwendet Die immer neue Anordnung von Erkennungsspecies im Array-Format und die Verwendung von p-NA's als Paarungssysteme ist gegenüber anderen Systemen, siehe z B WO 96/13522 (s 16, unten), besonders vorteilhaft
Ein weiterer Gegenstand der vorliegenden Erfindung bezieht sich daher insbesondere auch auf ein Diagnostikum enthaltend ein oben beschriebenes Pentopyranosyl-Nucleosid oder ein erfindungsgemaßes Konjugat, wie oben bereits naher beschrieben
Die folgenden Figuren und Beispiele sollen die Erfindung naher beschreiben, ohne sie zu beschranken
BESCHREIBUNG DER FIGUREN
Fig. 1 zeigt einen Ausschnitt aus der Struktur von RNA in ihrer natürlich vorkommenden Form (links) und in Form einer p-NA (rechts).
Fig. 2 zeigt schematisch die Synthese eines ρ-Ribo(A,U)-Oligonucleotids nach Eschenmoser et al. (1993).
Fig. 3 zeigt schematisch eine Anordnung von immobilisierten Erkennungsstrukturen (Arrays) auf einem festen Träger.
BEISPIELE
Beispiel Synthese des l-{3'-0-Benzoyl-4'-0-[(4,4'-dimethoxytriphenyl)-methyl]- ß-D-ribo-pyranosylj-thymins
Zuerst 4'-Substitution, dann 2 '-Substitution, dann Wanderungsreaktion:
Schema 1 Unter Argonatmosphäre wurden 51,6 g (200 mmol) l-(ß-D-Ribo-pyranosyl)-thymin A in 620 ml wasserfreiem Pyridin gelöst, 71,4 ml (2,1 eq.) N-Ethyldiisopropylamin und 100 g Molsieb (4 Ä) zugesetzt und 15 min lang mit KPG-Rührer gerührt. Man löste 92 g (272 mmol; 1,36 eq.) Dimethoxytritylchlorid (DMTCl) in 280 ml (frisch von festem NaHCO3 destilliertem) Chloroform, und tropfte diese Lösung innerhalb von 30 min bei -6 bis -5 °C
der Triollosung zu Es wurde 1 h bei dieser Temp , dann über Nacht bei Raumtemperatur (RT ) gerührt, wieder gekühlt, und weitere 25 g (74 mmol, 0,37 eq ) DMTCl in 70 ml Chloroform zugesetzt Man ließ auf RT kommen und rührte 4 h nach Eine kleine Probe wurde entnommen, waßπg aufgearbeitet und Chromatographien:, um die analytischen Daten des l-{4'-O-[(4,4'-dimethoxytriphenyl)-methyl]-ß-D-πbo-pyranosyl}- thymins zu erhalten.
1H-NMR (300 MHz, CDC13): 1,70 (bs, 2H, OH), 1,84 (d, 3H, Me), 2,90 (bs, 1 H, OH), 3, 18, 3,30 (2m, 2H, H(5')), 3,62 (bs, IH, H(3')), 3,70-3,82 (m, 8 H, 2 OMe, H(4'), H(2')), 5,75 (d, J = 9,5 Hz, IH, H(l ')), 6,85 (m, 4H, Harom), 6,96 (m, 1 H, Harom), 7,20 (m, 9H, Harom, H(6)), 8,70 (bs, IH H(3) )
Das Reaktionsgemisch wurde mit 2,46 g (20,5 mmol, 0, 1 eq ) 4-Dimethylamιnopyπdin (DMAP) versetzt, auf -6 °C gekühlt und zwischen -6 und -1 °C innerhalb von 15 min 27,9 ml (0,24 mol, 1,2 eq ) Benzoylchloπd (BzCl) in 30 ml Pyπdm zugetropft und 10 min nachgeruhrt Zur vollständigen Umsetzung wurden dann im Abstand von 25 mm noch jeweils 2,8 ml (24 mmol, 0,12 eq ) BzCl unter Kühlung zugesetzt und schließlich 20 min gerührt
Man setzte bei RT 460 ml wasserfreies Pyridin, 841 ml (1 1 ,2 mol. 56 eq ) n-Propanol, 44 g (0,316 mol, 1,58 eq ) p-Nitrophenol, 21,7 g (0, 18 mol, 0,9 eq ) DMAP und 136 ml (0,8 mol, 4 eq ) N-Ethyldiisopropylamin zu und rührte bei 61 - 63 °C 48 h lang Dann blieb der Ansatz bei RT 60 h stehen Das Reaktionsgemisch wurde noch 24 h lang auf 61 - 63 °C erwärmt, auf RT abgekühlt und am Rotavapor eingeengt Der Ruckstand wurde in 2 1 Ethylacetat aufgenommen, das Molsieb abfiltriert, die org Phase dreimal mit je 1 1 Wasser extrahiert, einmal mit 1,2 1 10 %ιger Citronensaure 5 min ausgeruhrt und die org Phase wieder abgetrennt, einmal mit 1 1 Wasser und zum Abschluß mit 1 1 gesättigter NaHCO3- Losung extrahiert Die org. Phase wurde mit Natriumsulfat getrocknet, filtriert und eingeengt (220 g Ruckstand)
Man filtrierte zuerst über Kieselgel 60 (20 x 10 cm) mit Stufengradienten Heptan/Ethylacetat, 1 1 bis 0 1) zur Vorreinigung, dann wurde an Kieselgel 60 chromatographiert (30 x 10 cm; Stufengradient Dichlormethan/Ethylacetat, 1 0 bis 1.1)
Man erhielt: 40 g unpolare Fraktionen
52,9 g l-{3,-O-Benzoyl-4'-O-[(4,4'-dimethoxytriphenyl)-methyl]-ß- D-ribo-pyranosyl}-thymin B 34,5 g verunreinigtes B 3,4 g polare Fraktionen
Die verunreinigte Fraktion wurde erneut chromatographiert (KG 60, 45 x 10 cm, Dichlormethan/Ethylacetat, 3 1 ) und lieferte weitere 1 1,3 g B
Gesamtausbeute 64,2 g (97 mmol) B, d s 48 % Ausbeute Η-NMR entspricht.
Beispiel 2
Synthese des N*-Benzoyl-l-{3 '-0-benzoyl-4'-0-[(4,4'-dιmethoxytrιphenyl)-methyl]-ß-D- rώo-pyranosylj-cytosins
Zuerst 2'-Substιtutιon, dann 4'-Substιtutιon, dann Wanderunusreaktion
Schema 2
Alle Ansätze wurden unter N2-Atmosphare durchgeführt
N τ4 -Benzoyl-l-(2'-O-benzoyI-ß-D-ribo-pyranosyI)-cytosin 2
54,0 g (0,155 mol) N τ4 -Benzoyl-l-(ß-D-ribo-pyranosyl)-cytosin 1 wurden in 830 ml Dimethylformamid (DMF) und 1,5 1 Pyridin (beide Losungsm. getrocknet und gelagert über Molsieb 3 Ä) unter Erwarmen auf 124 °C gelost Bei -58° bis -63 °C wurden 23,0 g (0,163 mol, 1,05 eq ) BzCl, gelost in 210 ml Pyridin, in 3,5 h zugetropft Der Ansatz wurde im Kuhlbad über Nacht gerührt 90,3 g (1,5 mol, 10 eq.) n-Propanol wurden eingerührt und der Ansatz bei 40 °C im HV eingeengt. Durch zweimalige Zugabe von 150 ml Toluol und erneutes Einengen wurden Pyridinreste entfernt 124,3 g Ruckstand wurden in 500 ml CH2C1 gelost, zweimal mit je 300 ml halbkonzentrierter NaHCO^-Losung ausgeruhrt, und der ausgefallene Feststoff abfiltriert und getrocknet 60,7 g Ruckstand Die CH C12-Phase wurde eingeengt. 25,0 g Getrennte Chromatographie an Kieselgel 60 (40 x 10 cm) mit Gradienten (AcOEt/iso-Hexan, 4 1, dann reines AcOEt, dann AcOEt/MeOH, 19 1 bis 2.1) lieferte (DC (Kieselgel, AcOEt))
16,8 g 2',4'-Dibenzoat (24 %) Rf 0,5
12,4 g 1 (23 %) Rf 0,0
35,4 g 2 (51 %) Rf 0, 14
N4-Benzoyl-l-{3'-O-benzoyl-4'-O-[(4,4'-dimethoxytriphenyl)-methyl]-ß-D-ribo- pyranosyI}-cytosin 3:
35,4 g (78 mmol) 2 wurden in 390 ml CH2C12 und 180 ml Pyridin (beides wasserfrei) gelost und 0,94 (7,8 mmol, 0,1 eq.) DMAP, 34,6 ml (203 mmol, 2,6 eq ) N-Ethyldiisopropylamin und 33,1 g (98 mmol; 1,25 eq.) DMTCl zugegeben und 2 h bei RT gerührt DC (Kieselgel, AcOEt). Rf 0,6 CH2C12 wurde bei 30 °C abgezogen, der Rückstand mit 640 ml Pyridin, 9,37 (78 mmol, 1,0 eq.) DMAP, 32,5 ml (234 mmol; 3,0 eq.) Et3N, 21,7 g (156 mmol, 2,0 eq.) p-Nitrophenol und 93,8 g (1,56 mol, 20 eq ) n-Propanol versetzt und 42 h bei 65 °C gerührt. Der Ansatz wurde am HV bei 50 °C eingeengt, zweimal mit je 250 ml Toluol versetzt und eingeengt.
Der Rückstand wurde in 1 1 CH2C12 aufgenommen, dreimal mit je 500 ml verdünnter NaHCO3-Lsg. ausgerührt, die org. Phase mit Na2SO4 getrocknet und eingeengt: 92,5 g Rückstand.
Chromatographie an Kieselgel 60 (50 x 10 cm) mit Gradienten (Methyl-tert. Butylether/iso- Hexan, 2: 1 bis 4: 1, dann Methyl-tert. Butylether/ AcOEt, 1 :4, dann AcOEt/MeOH, 1 : 1 bis 1 :3) lieferte 44,7 g Produkt-haltige Fraktion, die aus 540 ml CH2Cl2/Methyl-tert. Butylether, 1 :5, umkristallisiert wurde. Das Kristallisat wurde erneut aus 300 ml CH2Cl2/Methyl-tert. Butylether, 1 : 1, umkristallisiert. 3: DC (Kieselgel, CHCl3/i-PrOH 49: l): Rf 0,14.
Man erhielt: 30,0 g N4-Benzoyl-l-{3'-O-benzoyl-4'-O-[(4,4'-dimethoxytriphenyl)- methyl]-ß-D-ribo-pyranosyl } -cytosin 3 d. s. 51 % Ausbeute bezogen auf 2. Η-NMR entspricht.
Beispiel 3
Synthese des Is -Benzoyl-9-{3 '-O-benzoyl-4 '-0-[(4, 4 '-dimethoxytriphenyl)-methyl]-ß-D- ribo-pyranosylj-adenins
Zuerst 2 '-Substitution, dann 4'-Substitution, dann Wanderungsreaktion:
Schema 3
9-(ß-D-Ribo-pyranosyl)-adenin 2:
68,37 g (100 mmol) N6-Benzoyl-9-(2',3',4'-tri-O-benzoyl-ß-D-ribo-pyranosyl)-adenin 1 wurde in 300 ml NH3-gesättigtem MeOH über Nacht bei RT. gerührt und das Kristallisat abfiltriert: 23,5 g (88 %) 2.
DC (Kieselgel, AcOEt/MeOH 2: 1): Rf 0,23. 'H-NMR (300 MHz, DMSO): 3,56-3,78 (m, 3H, H(4'), H(5')); 4,04 (m, IH, H(3')); 4.23
(ddd, J - 2,5, 8, 9,5 Hz, H(2')), 4,89 (d, J = 6 Hz, IH, OH), 5,07 (d, J = 7 Hz, IH, OH),
5, 12 (d, J = 4 Hz, IH, OH), 5,63 (d, J = 9,5 Hz, IH, H(l ')), 7,22 (s, 2H, NH2), 8,14 (s,
IH, H(2)), 8,29 (s, IH, H(8)).
13C-NMR (75 MHz, DMSO): 65,0 (t, C(5')); 66,6 (s, C(4')), 68, 1 (s, C(3')), 71, 1 (s, C(2')); 79,6 (s, C(l ')); 118.6 (C(5)); 139,5 (s, C(8)), 149,9 (s, C(4)), 152,5
(s, C(2)), 155,8 (s, C(6)).
N6,N6-Dibenzoyl-9-(ß-D-ribo-pyranosyI)-adenin 3 :
Unter N2- Atmosphäre wurden 16,8 g (62,9 mmol) 2 in 500 ml wasserfreiem Pyridin suspendiert und auf -4 bis - 10 °C gekühlt. Innerhalb von 20 min wurden 40 ml (199 mmol; 5 eq.) Trimethylchlorsilan zugetropft und 2,5 h unter Kühlung gerührt. Bei -10 bis -15 °C wurden 36,5 ml (199 mmol; 5 eq.) Benzoylchlorid, gelöst in 73 ml Pyridin, innerhalb von 25 min zugesetzt, 10 min unter Kühlung und 2 h bei RT. gerührt (DC-Kontrolle (Kieselgel, AcOEt Heptan 1 : 1): Rf 0,5). Man kühlte wieder auf -10 °C, ließ 136 ml H2O (Temp. max. +8 °C) zulaufen und rührte über Nacht bei RT. Nach vollständigem Umsatz wurde das Lösungsmittel abgezogen und der Rückstand zweimal in je 200 ml Toluol aufgenommen und wieder eingedampft. Man versetzte mit je 500 ml Et2O und H2O, ließ mechanisch 2 h rühren, filtrierte das in beiden Phasen nur wenig lösliche Produkt ab, wusch mit Et2O und H2O und trocknete über P2O5 am HV. : 23,8 g (80 %) 3. DC (Kieselgel, AcOEt/MeOH 9: 1): Rf 0,35.
Η-NMR (300 MHz, DMSO): 3,60-3,80 (m, 3H, H(4'), H(5')); 4,06 (bs, IH, H(3')); 4.30 (ddd, J = 2,5, 8, 9,5 Hz, H(2')), 4,93 (d, J = 6 Hz, IH, OH), 5,20 (d, J = 4 Hz, IH, OH), 5,25 (d, J = 4 Hz, IH, OH), 5,77 (d, J - 9,5 Hz, IH, H(l')), 7,47 (m, 4 H, Harom), 7,60 (m, 2H, Harom), 7,78 (m, 4H, Harom), 8,70 (s, IH, H-C(2), 8,79 (s, IH, H(8)).
1 C-NMR (75 MHz, DMSO): 66,2 (t, C(5')); 66,5 (s, C(4')), 68,0 (s, C(3')), 71,0 (s, C(2')), 80,4 (s, C(l')); 112.42 (C(5)); 126,9 (s, C(5)), 126,9, 128,9, 133,3,
133,4 (arom. C), 146,0 (s, C(8)), 150,7 (s, C(4)), 151,8 (s, C(2)), 153,3 (s, C(6)), 172,0 (s, C=O)).
N6, N6-Dibenzoyl-9-(2'-O-benzoyl-ß-D-ribo-pyranosyI}-adeniιι 4:
Unter N2- Atmosphäre wurden 26,4 g (55,5 mmol) 3 in 550 ml wasserfreiem CH2Cl2und 55 ml Pyridin (jeweils gelagert über Molsieb) gelöst, mit 0,73 g (5,55 mmol; 0,1 eq.) DMAP versetzt und auf -87 bis -90 °C abgekühlt. Innerhalb von 1 h wurden 8,58 g (61 mmol; 1,1 eq.) BzCl in 14 ml Pyridin zugetropft und über 60 h (Wochenende) bei -78 °C belassen. Der Ansatz wurde eingeengt, zweimal mit je 100 ml Toluol versetzt und eingedampft, um Pyridin zu entfernen. Chromatographie an Kieselgel 60 (20 x 10 cm) mit Gradienten (AcOEt/Heptan, 1 : 1 bis 9: 1) lieferte 23,2 g 4. 4: DC (Kieselgel, AcOEt): Rf 0,34.
N6-Benzoyl-9-{3'-O-benzoyl-4'-O-[(4,4'-dimethoxytriphenyl)-methyl]- ß-D-ribo-pyranosyl}-adenin 5:
23,2 g (40 mmol) 4 wurden in 160 ml wasserfreiem CH2C12 gelöst und in Folge mit 14,9 g (56 mmol; 1,1 eq.) DMTCl und 17,7 ml (104 mmol; 2,6 eq.) N-Ethyldiisopropylamin versetzt. Nach 2 h Rühren bei RT wurden weitere 4,0 g (11,8 mmol; 0,3 eq.) DMTCl zugefügt und weitere 40 min gerührt. Der Ansatz wurde bei 350-520 mbar und 35 °C am Rotavapor eingeengt.
DC (Kieselgel, AcOEt/Heptan 1 :1): Rf 0,18. Der Rückstand wurde in 260 ml wasserfreiem Pyridin gelöst und in Folge mit 51 ml (679 mmol; 17 eq.) n-Propanol, 16,6 ml (120 mmol; 3 eq.) Et3N, 11,1 g (80 mmol; 2 eq.) p- Nitrophenol und 5,3 g (44 mmol; 1,1 eq.) DMAP versetzt und bei 60-63 °C 23 h lang gerührt. Dann blieb der Ansatz bei RT. 21 h stehen. Das Reaktionsgemisch wurde am Rotavapor eingeengt. Der Rückstand wurde zweimal mit je 200 ml Toluol versetzt und eingeengt, in CH2C12 gelöst und dreimal mit Wasser extrahiert.
Chromatographie an Kieselgel 60 (30 x 10 cm) mit Gradienten (AcOEt/Heptan, 1 :2 bis 1:0; dann AcOEt/MeOH, 1:0 bis 9: 1) lieferte 13 g 5.
5: DC (Kieselgel, AcOEt/Heptan 4: 1): R* 0,2.
Man erhielt: 13 g N6-Benzoyl-9-{3'-O-benzoyl-4'-O-[(4,4'-dimethoxytriphenyl)- methyl]-ß-D-ribo-pyranosyl}-adenin 5 d. s. 30 % Ausbeute bezogen auf 3. Η-NMR entspricht. Zeitersparnis gegenüber literaturbekanntem Verfahren: 50 %.
Beispiel 4 Synthese von 9-[3'-0-Benzoyl-4'-0-((4,4'-dimethoxytriphenyl)-methyl)-ß-D- ribopyranosyl]-2-0-allyl-2-N-isobutyroyl-guanin
Zuerst 3 '-Substitution, dann 4' -Substitution:
9-[3'-O-Benzoyl-ß-D-ribopyranosyl]-2-O-allyI-2-N-isobutyroyl-guanin B
Das G-Triol A (393 mg, 1.0 mmol) wurde in 4 ml trockenem Dichlormethan gelöst. Man versetzte mit Benzoesäuretrimethylorthoester (0.52 ml, 3.0 mmol) und Camphersulfonsäure
(58 mg, 0.25 mmol) und rührte 15 h bei Raumtemperatur. Dann wurde die Mischung auf 0
°C abgekühlt und mit 2 ml einer auf 0 °C vorgekuhlten Mischung von Acetonitril, Wasser und Trifluoressigsaure (50:5 1) versetzt Man rührte 10 min und entfernte das Losungsmittel im Vakuum Der Ruckstand wurde durch Flashchromatographie an Kieselgel (2.3 x 21 cm) mit Dichlormethan/Methanol 100 3 gereinigt Man erhielt 25 mg (5%) 4-O- Benzoylverbindung 139 mg (28%) Mischfraktionen und 205 mg (41 %) der gewünschten 3- O-Benzoylverbindung B
1H-NMR (300 MHz, CDC13) 1 12, 1 14 (2 d, J = 7 0 Hz, 2 x 3 H, NHCOCHMeA 2.78 (hep, J = 7 Hz, 1 H, NHCOCHMe2), 3 85 (dd, J - 6 0, 11 0 Hz, 1 H, H-5'eq), 3 94 (app. T, J = 1 1 0 Hz, 1 H, H-5'„), 4 12 (ddd, J = 2 5, 6 0, 11 0 Hz, 1 H, H-4'), 4 52 (dd, J = 3 5, 9 5 hz, 1 H, H-2'), 5 00 (dt, J = 1 5, 6 0 Hz, 2 H, All), 5 19 (dq, J = 1 5, 10 0 Hz, 1 H, All), 5 39 (dq, 1 5, 16 5 Hz, 1 H, All), 5 85 (bt, J = 3 0 Hz, 1 H, H-3'), 5 97 (d, J = 9 5 Hz, 1 H, H-l'), 6 07 (ddd, J = 6 0, 10 0, 16 5 Hz, 1 H, All), 7 40-7 58 (m, 3 H, Bz), 8 10-8 16 (m, 2 H, Bz), 8 28 (s, 1 H, H-8)
9-[3,-O-Benzoyl-4'-O-((4,4'-dimethoxytriphenyI)-methyl)-ß-D-ribopyranosyl]-2-O- allyl-2-N-isobutyroyl-guanin C
Das Diol B (101 mg, 0 2 mmol) wurde in 3 2 ml trockenem Dichlormethan suspendiert Man versetzte mit 171 μl (1 0 mmol) N-Ethyldiisopropylamin, 320 μl (3 96 mmol) Pyridin und 102 mg (0 3 mmol) DMTCl und rührte bei Raumtemperatur Nach 24 h wurden weitere 102 mg (0 3 mmol) DMTCl zugegeben und nochmals 24 h gerührt Dann wurde mit 30 ml Dichlormethan verdünnt Die Losung wurde mit 20 ml 10%iger wassriger Citronensaurelosung und 10 ml gesättigter Natπumbicarbonatlosung gewaschen, über MgSO getrocknet und im Vakuum eingeengt Der Ruckstand wurde durch Flashchromatographie an Kieselgel (2 3 x 20 cm) mit Dichlormethan/Methanol 100 1 gereinigt Man erhielt 39 mg des bekannten, gewünschten Produkts C (24%)
Beispiel 5
Synthese von p-RNA-Linkersystemen
Im folgenden werden drei Wege beschrieben, die die Bereitstellung von Linkern, die einen Amino-Terminus aufweisen, der dann zum Anlinken fünktioneller Einheiten verwendet werden kann, ermöglichen:
5.1 Uracil-basierender Linker auf der Basis der Modifizierung der 5-Position des Uracils.
Die Herstellung von Hydroxyethyluracil 28 gelingt im großen Maßstab nach bekannter Methode (J.D. Fissekis, A. Myles, G.B. Brown, J. Org. Chem. 1964, 29, 2670) g- Butyrolacton 25 wurde mit Ameisensäuremethylester formyliert, das Natriumsalz 26 zum Harnstoffderivat 27 umgesetzt und dieses zum Hydroxyethyluracil 28 cyclisiert (Schema 4).
25 26 27 28
a) b) c)
25 S. 72 26 S. 74 ^ 27 S. 74 28 a) NaOMe. HCOOMe. Et,0, 72%; b) Harnstoff. H+, H20, 49%; c) NaOEt" EtOH. Δ, 36%.
Schema 4: Synthese von Hydroxyethyluracil 28.
a) b) c) d) 7
' ' 29 ιr
3 31 *- 32
"" S. 7 ° S. 82 1 S. 84 a) MsCl, py, 0°, 50%; b) NaN3, DMF, 60°, 71%; c) 1. PPh3, py; 2. NH3/H2O, 85%; d) PhtNCO2Et, Na^^, H2O, 91%.
Schema 5 : Synthese von N-Phthaloylaminoethyluracil 32.
Hydroxyethyluracil 28 wurde mit Methansulfonsäurechlorid in Pyridin mesyliert zu 29 (J.D. Fissekis, F. Sweet, J. Org. Chem. 1973, 38, 264).
Die folgenden Stufen wurden neu erfunden: Mit Natriumazid in DMF wurde 29 zum Azid 30 umgesetzt und dieses mit Triphenylphosphin in Pyridin zum Aminoethyluracil 31 reduziert. Die Aminofünktion in 31 wurde schließlich mit N-Ethoxycarbonylphtalimid geschützt (Schema 5). Nukleosidierung von Ribosetetrabenzoat 33 mit N- Phtaloylaminoethyluracil 32 lieferte das Ribosetribenzoat 34 in guten Ausbeuten. Das anomere Zentrum des Pyranoseringes ist, wie aus der Kopplungskonstanten zwischen H- C(l ') und H-C(2') von J = 9.5 Hz klar ersichtlich, ß-konfiguriert. Anschließende Abspaltung der Benzoatschutzgruppen mit NaOMe in MeOH lieferte das Linkertriol 35. 35 wurde bei - 78°C in Pyridin/Dichlormethan 1 : 10 in Gegenwart von DMAP mit Benzoylchlorid umgesetzt. Dabei erhielt man neben dem gewünschten 2'-Benzoat 36 (64%>) auch 2', 4'- dibenzoyliertes Produkt (22%), welches gesammelt und analog der Methanolyse von 34 nach 35 wieder in das Triol 35 umgewandelt wurde. Das 2'-Benzoat 36 wurde mit Dimethoxytritylchlorid in Gegenwart von Hünig-Base in Dichlormethan in 4'-Position in Ausbeuten größer 90%> trityliert. Die Umlagerung von 4'-DMT-2'-benzoat 37 zum 4'- DMT-3'-benzoat 38 erfolgte in Gegenwart von DMAP, p-Nitrophenol und Hünig-Base in
n-Propanol/Pyridin 5:2. Nach Chromatographie wird 38 erhalten. 4'-DMT-3 '-benzoat 38 wurde abschließend mit ClP(OAll)N(iPr)2 in Gegenwart von Hünig-Base zum Phosphoramidit 39 umgesetzt (Schema 6). Dieser läßt sich ohne Änderung der Syntheseprotokolle für die automatisierte Oligonucleotidsynthese einsetzen.
32 + 33 34 35 36 37
S. 86 S. 89 Ch.41 b Ch. 43/b e) f>
37 38 39
STS 192 STS 189 a) BSA, TMSOTf. CH3CN, 50°, 86%: b) NaOMe. MeOH. 93%: c) BzCl. pv/ CH2C1„ -78°: d) DMTCl. EtN/Pr2. CH C12; e) DMAP./>NO,Phenol. EtN Pr2. py, «PrOH. 70°: f) C1P(0A11)N/Pr2. EtN/Pr2, CH,C12.
Schema 6: Synthese des Linkerphosphoramidites 39.
Ausführung:
Synthese eines Uracil-Linker-Bausteins
5-(2-AzidoethyI)uracil (30)
a) b) c) d)
32 + 33 34 35 36 37
S. 86 S. 89 Ch.41/b Ch. 43/b e) 0
37 38 39
STS 192 STS 189 a) BSA. TMSOTf. CH3CN, 50°, 86%; b) NaOMe. MeOH, 93%, c) BzCl. py/ CH2C12. -78°. d) DMTCl, EtN;Pr2. CH,CI2, e) DMAP./>NO,PhenoL EtN/Pr2, pv. «PrOH, 70°. f) ClP(OAU)N;Pr,. EtN;Pr2, CH,C12
Schema 6 Synthese des Linkerphosphoramidites 39
Ausführung
Synthese eines Uracil-Linker-Bausteins
5-(2-AzidoethyI)uracil (30)
29 30
In einem mit Innenthermometer und Ruckflußkuhler ausgestatteten 500-ml-Dreihalskolben wurden 26 0 g (0 11 mol) 29 in 250 ml DMF gelost und mit 10 8 g (0 166 mol) Natπumazid versetzt Die Suspension wurde im Anschluß vier Stunden bei 60°C gerührt (DC-Kontrolle, CHCl3/MeOH 9 1) Das DMF wurde abdestilhert und der Ruckstand mit 150 ml Wasser verrührt Der Feststoff wurde abfiltriert, mit ca 50 ml Wasser gewaschen und über Nacht im Vakuum im Exsiccator über Phosphorpentoxid getrocknet Man erhielt 14 2 g (71%) 30 in Form eines farblosen Feststoffes vom Schmp 230-235°C (u Zers )
2. Analytische Daten
5-(2-Azιdoethyl)uracιl (30) Schmp.: 230-235°C u Zersetz
DC: CHCIVMeOH 9 1 , Rf 0 48
UV (MeOH): λmax 263 0 (7910)
IR (KBr): 3209s, 3038s, 2139s, 1741s, 1671s, 1452m, 1245m, 1210m
Η-NMR (300 MHz, d6-DMSO): 2 46 (t, 2H, J(CH2CH2N, CH2CH2N) = 7 0, CH2CH2N), 3 40 (t, 2H, J(CH2CH2N, CH2CH2N) - 7 0, CH2CH2N), 7 36 (s, H-C(6)),
11 00 (br s, 2H, H-N(l), H-N(3))
MS (ESI+): 180 0 [M+H]
5-(2-Aminoethyl)uracil (31)
30 31
30 31
1. Durchführung
In einem mit Innenthermometer und Ruckflußkuhler ausgestatteten 250-ml-Dreιhals-kolben wurden 14 2 g (78 0 mmol) 30 in 175 ml Pyridin suspendiert und mit 61 4 g (234 mmol) Triphenylphosphin versetzt2' Es wurde fünf Stunden auf 60°C erwärmt und über Nacht bei Raumtemp gerührt (DC-Kontrolle, CHCl3/MeOH 5 1) Zur Suspension wurden 40 ml einer 25%>igen Ammoniaklosung gegeben, die daraufhin aufklarte Die Losungsmittel wurden l v i.RV entfernt Der Ruckstand wurde in 200 ml CH2Cl2/MeOH 1 1 30 min bei Raumtemp gerührt, der Niederschlag abfiltπert und mit CH2C12 gewaschen Nach Trocknen im Vakuum im Exsiccator über Phosphorpentoxid erhielt man 10 0 g (85%>) 31 vom Schmp 214-220°C
2. Analytische Daten
5-(2-Amιnoethyl)uracιl (31)
Schmp.: 214-220°C u Gasentwicklung, vorher sintern
DC: CHCl3/MeOH/HOAc/H O 85 20 10 2, Rf 0 07
UV (MeOH): λ™* 263 0 (6400) o ER (KBr): 3430m, 3109s, 1628s, 1474m, 1394s, 1270s, 1176w, 1103m, 1021m, 966m, 908m, 838m
1H-NMR (300 MHz, d6-DMSO): 2.21 (t, 2H, J(CH2CH2N, CH2CH2N) = 6.8, CH2CH2N); 2.59 (t, 2H, J(CH2CH2N, CH2CH2N) = 6.8, CH2CH2N); 5.90 (v. br. s, 4H, H-N(l), H-N(3), NH2); 7.19 (s, H-C(6)).
MS (ESF): 153.9 [M-H].
5-(2-Phtalimidoethyl)uracil (32)
31 32
31 32
1. Durchführung
In einem 250-ml-Rundkolben wurden 9.6 g (61.8 mmol) 31 in 100 ml Wasser suspendiert und mit 6.64 g (62.6 mmol) Na2CO3 versetzt. Nach 15 min Rühren bei Raumtemp. gab man portionsweise 14.3 g (65 mmol) N-Ethoxycarbonylphtalimid zu und rührte drei Stunden bei Raumtemp. (DC-KontroUe, CHCl3/MeOH 5: 1). Die nunmehr zähe, weiße Suspension wurde vorsichtig1' mit konz. Salzsäure auf pH 4 eingestellt und der weiße Niederschlag abfiltriert. Nach Waschen mit Wasser wurde der Feststoff im Vakuum im Exsiccator über Phosphorpentoxid getrocknet. Dies lieferte 16.0 g (91%) 32 vom Schmp. 324-327°C.
2. Analytische Daten
5-(2-Phtalimidoethyl)uracil (32): Schmp.: 324-327°C u. Zersetz.
DC: CHCl3/MeOH 5 1 , Rf 0 51
UV (MeOH): λ™* 263 0 (5825), λ 298 0 (sh , 1380)
IR (KBr): 3446m, 3216m, 1772m, 1721s, 1707s, 1670s, 1390m
1H-NMR (300 MHz, d6-DMSO): 2 49 (t, 2H, J(CH2CH2N, CH2CH2N) = 6 0, CH2CH2N), 3 71 (t, 2H, J(CH2CH2N, CH2CH2N) = 6 0, CH2CH2N), 7 24 (s, H-C(6)), 7 84 (mc, 4H, NPht), 10 76 (br s, H-N(l), H-N(3))
MS (ESF): 284 0 [M-H]
l-(2, 3, 4-Tri-O-benzoyl-ß-D-ribopyranosyl)-5-(2-phtalimido-ethyl)uracil (34)
32 + 33 34
1. Durchführung
In einem 250-ml-Dreihalskolben, ausgestattet mit Argonuberleitung, Innenthermometer und Septum, wurden 7 00 g (24 mmol) 32 und 13 6 g (24 mmol) 33 in 120 ml Acetonitril suspendiert Dann wurden mittels Spritze zunächst 12 2 ml (50 mmol) BSA zugegeben und nach 30 min Ruhren nochmals 7 ml (28 mmol) BSA zugegeben Nach kurzzeitigem Erwarmen auf 40°C klarte sich die Reaktionsmischung auf Bei Raumtemp wurden 13 ml (72 mmol) TMSOTf mittels Spritze zugegeben Nach einer Stunde konnte noch keine Produktbildung beobachtet werden (DC-Kontrolle, AcOEt/n-Heptan 1 1) Daher wurden
weitere 13 ml (72 mmol) TMSOTf zugegeben Im Anschluß wurde der Reaktionsansatz auf 50°C erwärmt. Nach 2 5 h Ruhren bei 50°C (DC-Kontrolle) wurde auf RT gekühlt, auf eine eiskalte Mischung von 250 ml AcOEt und 190 ml ges NaHCO3-Losung und 10 min intensiv ausgeruhrt Man wusch nochmals mit 100 ml NaHCO -Losung und extrahierte die wäßrigen Phasen nochmals mit 100 ml AcOEt Die ver org. Phasen wurden mit MgSO4 getrocknet und die Losungsmittel i V i RV entfernt Nach Trocknen im OPV erhielt man 20 9 g Rohprodukt Chromatographie an Kieselgel (h = 25 cm, φ = 5 cm, AcOEt/n-Heptan 1 1) lieferte ein DC-einheit ches, schaumiges Produkt, das mit Et2O digeriert wurde Filtration und Trocknen im OPV ergab 15 g (86%) 34
2. Analytische Daten
l-(2, 3, 4-Tri-O-benzoyl-ß-D-ribopyranosyl)-5-(2-phtalimidoethyl)uracil (34)
Schmp.: 124°C (sintern) DC: AcOEt/n-Heptan 1 l, Rf 0 09
UV (MeOH): λmax 263 0 (11085), λ 299 0 (sh , 1530)
ER (KBr): 3238w, 3067w, 1772m, 1710s, 1452m, 1395m, 1266s. 1 1 10s, 1070m, 1026m
Η-NMR (300 MHz, CDC13): 2 79 (mc, 2H, CH2CH2N), 3 96 (m_, 2H, CH2CH2N), 4 06 (dd, J(Heq-C(5'), Hax-C(5')) = 1 1 0, J(He -C(5 '), H-C(4')) = 6 0, Heq-C(5')),
4 12 (t, J(Ha -C(5'), Heq-C(5')) = J(Ha,-C(5'), H-C(4')) = 11 0, Hax-C(5')),
5 39 (dd, J(H-C(2'), H-C(l ')) = 9 5, J(H-C(2'), H-C(3')) = 2 9, H-C(2')), 5 46 (ddd, J(H-C(4'), Hax-C(5')) = 11 0, J(H-C(4'), Heq-C(5')) = 6 0, J(H- C(4'), H-C(3')) = 2 9, H-C(4')), 6 26 (ψt, J * 2.6, H-C(3')), 6 36 (d, J(H- C(l '), H-C(2')) = 9 5, H-C(l ')), 7 24-7 40, 7 44-7 56, 7 61-7 66, 7 72-7 80,
7 84-7 90, 8 06-8 13 (6m, 16H, 3 Ph, H-C(6)), 7 70, 7 82 (2 ie, 4H, NPht),
8 37 (s, H-N(3))
13C-NMR (75 MHz, CDC13): 21 19 (CH2CH2N), 36 33 (CH2CH2N), 64 07 (C(5')), 66 81, 68.22 (C(4'), C(2')), 69 29 (C(3 ')), 78 59 (C(l ')), 1 12 42 (C(5)), 123 31,
132.05, 133.89 (6C, Pht); 128.33, 128.47, 128.47, 128.83, 128.86, 129.31, 129.83, 129.83, 129.94, 133.55, 133.62, 133.69 (18C, 3 Ph); 135.87 (C(6)); 150.39 (C(2)); 162.78 (C(4)); 164.64, 165.01, 165.41 (3C, O2CPh); 168.43 (2C, CO-Pht). MS (ESI+): 730.2 [M+H]. Anal.: ber. für C40H3ιN3OH (729.70): C 65.84, H 4.28, N 5.76; gef: C 65.63, H 4.46, N 5.53.
5-(2-PhtalimidoethyI)-l-(ß-D-ribopyranosyl)uracil (35)
1. Durchführung
In einem 1 -1-Rundkolben wurden 15 g (20 mmol) 34 in 500 ml MeOH gelöst, mit 324 mg (6 mmol) NaOMe versetzt und über Nacht unter Wasserausschluß bei Raum-temp. gerührt (DC-Kontrolle, AcOEt/n-Heptan 1 : 1). Es wurde solange Amberlite IR-120 zur entstandenen Suspension gegeben bis der pH- Wert <7 war. Es wurde der Feststoff in der Hitze gelöst, heiß vom Ionentauscher abfiltriert und mit MeOH gewaschen. Nach Entfernen der Lösungsmittel wurde der Rückstand zweimal mit je 150 ml Wasser coevaporiert. Dies lieferte 9 g Rohprodukt, das 10 min in 90 ml MeOH unter Rückfluß erhitzt wurde. Nach
Abkühlen auf Raumtemp. versetzte man mit 60 ml Et2O und bewahrte über Nacht bei 4°C auf. Filtration, Waschen mit Et2O und Trocknen im ÖPV lieferte 7.8 g (93%) 35.
2. Analytische Daten
5-(2-Phtalimidoethyl)-l-(ß-D-ribopyranosyl)uracil (35):
Schmp.: 137°C (sintern).
DC: CHCVMeOH 5: 1, Rf 0.21.
UV (MeOH): λmax 263.0 (8575); λ 299.0 (sh., 1545).
IR (KBr): 3458s, 1772w, 1706s, 1400m, 1364m, 1304m, 1045m. 'H-NMR (300 MHz, d6-DMSO + 2 Tr. D2O): 2.55 (nie, 2H, CH2CH2N); 3.28-3.61 (m, 4H, H-C(2'), H-C(4'), Hq-C(5'), Hax-C(5')); 3.73 (nie, 2H, CH2CH2N); 3.93 (m, H-C(3')); 5.50 (d, J(H-C(1 '), H-C(2')) = 9.3, H-C(l ')); 7.41 (s, H-C(6)); 7.84 (s, 4H, NPht).
,3C-NMR (75 MHz, d6-DMSO): 25.63 (CH2CH2N); 36.62 (CH2CH2N); 64.95 (C(5')); 66.29 (C(4'))i 67.37 (C(2')); 71.12 (C(3')); 79.34 (C(l ')); 1 10.39 (C(5));
122.85, 131.54, 134.08 (6C, Pht); 137.92 (C(6)); 150.84 (C(2)); 163.18 (C(4)); 167.74 (2C, CO-Pht).
MS (ESF): 416.1 [M-H].
l-(2'-O-Benzoyl-ß-D-ribopyranosyl)-5-(2-phtalimidoethyl)-uracil
In einem ausgeheizten und mit Argon begasten 1 -1- Vierhalskolben wurden 10.6 g (0.025 mmol) 5-(2-Phtalimidoethyl)-l-(ß-D-ribopyranosyl)uracil in 20 ml Pyridin gelöst und mit 200 ml Dichlormethan versetzt. Es wurde auf -70°C abgekühlt, unter Kühlung 3.82 ml (0.033 mmol) Benzoylchlorid in 5 ml Pyridin und 20 ml Dichlormethan langsam zugetropft und 35 min bei -70°C gerührt. Das Reaktionsgemisch wurde auf 600 ml gekühlte Ammoniumchlorid-Lösung gegossen und die wäßrige Phase mit Ethylacetat extrahiert. Die vereinigten organischen Phasen wurden mit Wasser gewaschen, getrocknet und im Vakuum
zur Trockene eingeengt. Chromatographie über Kieselgel (Ethylacetat/Heptan 1 1) lieferte 7 9 g (60%) l-(2'-O-Benzoyl-ß-D-ribopyranosyl)-5-(2-phtalimidoethyl)-uracil. DC. Rf 0 24 (Ethylacetat/Heptan 4.1)
Η-NMR (300 Mhz, d6-DMSO). 2.67 (nie, 2H, CH2CH2N); 3.66-3 98 (m, 5H, H-C(4'), H^-C^'), Hax-C(5'), CH2CH2N); 4.51 (t, IH, H-C(3')), 4 98 (dd, IH, H-C(2')), 6 12 (d, IH, H-C(l ')); 7 19 (s, IH, H-C(6)); 7.29-7 92 (m, 9H, OBz, NPht).
l-(2-O-Benzoyl-4-O-(4,4'-dimethoxytrityl)-ß-D-ribopyranosyl)-5-(2-phtalimido- ethyl)uracil
5.6 g (10 73 mmol) l-(2-O-Benzoyl-ß-D-ribopyranosyl)-5-(2-phtalimidoethyl)uracιl wurden in 60 ml Dichlormethan gelost, mit 4 72 g (13 95 mmol) 4,4'-Dimethoxytπtylchlorid und 2.4 ml (13 95 mmol) N-Ethyl-diisopropylamin versetzt und 20 min bei RT gerührt. Das Reaktionsgemisch wurde mit 100 ml Dichlormethan verdünnt, mit Natriumhydrogencarbonat-Losung und 20%> Zitronensaure-Losung gewaschen, getrocknet und im Vakuum zur Trockene eingeengt Chromatographie über Kieselgel (Ethylacetat/Heptan 1 1 + 2% Triethylamin) lieferte 7 7 g (87%) 1 -(2-O-Benzoyl-4-O- (4,4'-dimethoxytrityl)-ß-D-ribopyranosyl)-5-(2-phtalimidoethyl)uracil DC Rf 0 53 (Ethylacetat/Heptan 1 1 + 2% Triethylamin)
Η-NMR (300 MHz, CDC13) 2 64 (mc, 2H, CH2CH2N), 3 12 (mc, IH. H-C(4')), 3 59-3.63 und 3 72-3 92 (m, 5H, H-C(3'), Heq-C(5'), Ha -C(5'), CH2CH2N), 3 81 und 3 82 (s, 6H, CH3O), 4 70 (dd, IH, H-C(2')), 6 09 (d, IH, H-C(l ')), 7 05 (s, IH, H-C(6)), 6 84-7 90 (m, 22H, ODmt, OBz, NPht).
l-(3-O-Benzoyl-4-O-(4,4'-dimethoxytrityl)-ß-D-ribopyranosyI)-5-(2-phtalimido- ethyl)uracil
3 g (3 63 mmol) l-(2-O-Benzoyl-4-O-(4,4'-dimethoxytrityl)-ß-D-ribopyranosyl)-5-(2- phtalimidoethyl)uracil, 1 g (7 26 mmol) 4-Nitrophenol, 0 44 g (3 63 mmol) 4- (Dimethylamino)pyridin und 3.75 ml (21.78 mmol) N-Ethyl-diisopropylamin wurden in 5.6
ml iso-Propanol und 25 ml Pyridin gelöst, auf 65°C erhitzt und 3 Tage bei 65°C gerührt.
Die Lösung wurde im Vakuum zur Trockene eingeengt und der Rückstand in 150 ml
Dichlormethan gelöst. Nach Waschen mit 20% Zitronensäure-Lösung und
Natriumhydrogencarbonat-Lösung wurde über Magnesiumsulfat getrocknet. Chromatographie über Kieselgel (Ethylacetat/Dichlormethan/iso-Hexan 2: 1: 1) lieferte 2.27 g (76%) l-(3-O-Benzoyl-4-O-(4,4'-dimethoxytrityl)-ß-D-ribopyranosyl)-5-(2- phtalimidoethyl)uracil.
DC: Rf 0.27 (Ethylacetat/iso-Hexan 2: 1 + 1% Triethylamin).
Η-NMR (300 MHz, CDC13): 2.39 (mc, 2H, CH2CH2N); 2.53 (m,, IH, H^-C^')); 3.30 (dd, IH, H-C(2')); 3.55 (nie, IH, Hax-C(5')); 3.69 (n e, 2H, CH2CH2N); 3.78 und 3.79 (s, 6H,
CH3O); 3.79-3.87 (m, IH, H-C(4')); 5.74 (d, IH, H-C(l ')); 5.77 (m0, IH, H-C(3')); 6.92
(s, IH, H-C(6)); 6.74-8.20 (m, 22H, ODmt, OBz, NPht).
l-{2'-O-[(Allyloxy)(diisopropylamino)phosphino|-3O-benzoyl-4'-O-[(4,4'- dimethoxytriphenyl)-methyl]- ß-D-ribo-pyranosyI}-5-(2-phtalimidoethyl)- uracil
88 mg (0.11 mmol) l-(3-O-Benzoyl-4-O-(4,4'-dimethoxytrityl)-ß-D-ribopyranosyl)-5-(2- phtalimidoethyl)uracil wurden in 5 ml Dichlormethan gelöst, mit 75 μl (0.44 mmol) N- Ethyl-diisopropylamin und 70 μl (0.3 mmol) Allyloxy-chlor-(diisopropylamino)phosphin versetzt und 3 h bei Raumtemperatur gerührt. Nach Zugabe von weiteren 35 μl (0.15 mmol) Allyloxy-chlor-(diisopropylamino)phosphin zur Vervollständigung der Reaktion wurde noch 1 h bei Raumtemperatur gerührt und das Reaktionsgemisch im Vakuum eingeengt. Chromatographie an Kieselgel (Ethylacetat/Heptan: Gradient 1 :2 auf 1 : 1 auf 2: 1, jeweils mit 2% Triethylamin) lieferte 85 mg (76%) l-{2'-O- [(Allyloxy)(diisopropylamino)phosphino]-3'O-benzoyl-4'-O-[(4,4'-dimethoxytriphenyl)- methyl]- ß-D-ribo-pyranosyl}-5-(2-phtalimidoethyl)- uracil. DC : Rf 0.36 (Ethylacetat/Heptan 2: 1).
Η-NMR (CDC13, 300 MHz): Ausgewählte charakteristische Lagen: 2.28, 2.52 (2 dd, J = 5.0, 11.0 Hz, 2 H, 2 H-5'), 3.79, 3.78 (app. 2 s, 12 H, OMe), 6.14 (1 bs, 1 H, H-3'). 31P-NMR (CDC13): 149.8, 150.6
5.2 Indol-basierender Linker
N-Phthaloyltryptamin wird wie beschrieben aus Phthalsaureanhydrid und Tryptamm erhalten (Kuehne et al J Org. Chem 43, 13, 1978, 2733-2735) Dieses wird mit Boran-THF zum Indolin reduziert (analog A Giannis, et al , Angew Chem 1989, 101, 220)
Das 3 -substituierte Indolin wird zuerst mit Ribose zum Nucleosidtriol und dann mit Essigsaureanhydrid zum Triacetat umgesetzt Man oxidiert mit 2,3-Dichlor-5,6- dicyanoparachinon und spaltet die Acetate mit Natπummethylat, benzoyliert selektiv in 2'- Position, DM-tπtyliert selektiv in 4'-Posιtion, und führt die Wanderungsreaktion zum 3'- Benzoat durch Die Bildung des Phosphoramidits erfolgt wie üblich Dieser laßt sich ohne Änderung der Syntheseprotokolle für die automatisierte Oligonucleotidsynthese einsetzen
Durchführung
3 -(N-PhthaloyI-2-aminoethyl)-indolin Phth
A B
Unter Stickstoffatmosphare wurden 51 4 g (177 mmol) Phthaloyltryptamin A in 354 ml IM Boran-THF-Losung (2 eq ) gelost und auf 0 °C abgekühlt Bei 0 °C wurde langsam 354 ml Trifluoressigsaure zugetropft (Vorsicht Gasentwicklung) und 30 min nachgeruhrt (DC- Kontrolle EtOAc) Dann wurden 17 3 ml Wasser zugegeben, 10 min gerührt und im Vak eingeengt Der Ruckstand wurde in 10%iger NaOH-Losung / Dichlormethan gelost, die organische Phase wurde abgetrennt, über NaSO4 getrocknet, filtriert und im Vak eingeengt Der Ruckstand (50 9 g) wurde aus heißem Ethanol (3 1) umkristallisiert Man erhielt 41 4 g B, Smp 161-162°C Die Mutterlauge wurde im Vakuum eingeengt und der Ruckstand erneut aus Ethanol umkristallisiert Man erhielt weitere 3 2 g B, Smp. 158-159 °C Gesamtausbeute 44 6 g (153 mmol) B, d s 86%
1H-NMR (CDC13, 300 MHz): 1.85-2.00, 2.14-2.28 (2 m, 2 x 1 H, CH2CH2NPhth), 2.70
(bs, 1 H, NH), 3.24-3.38, 3.66-3.86 (2 m, 5 H, CH2CH2NPhth, H-2a, H-2b, H-3), 6.62 (d, J
= 8.0 Hz, 1 H, H-7), 6.66-6.72 (m, 1 H, H-5), 6.99 (app t, J = 7.5 Hz, 1 H, H-6), 7.14 (d, J
= 8.0 Hz, 1 H, H-4), 7.64-7.74, 7.78-7.86 (2 m, 2 x 2 H, Phth).
13C-NMR (CDC13, 75 MHz): 32.70, 36.10 (2 t, C-2, CH2CH2NPhth), 39.62 (d, C-3), 53.04
(t, CH2NPhth), 109.65 (d, C-7), 118.74 (d, C-5), 123.25 (d, Phth), 123.92, 127.72 (2 d, C-
4, C-6), 131.81 (s, C-3a), 132.14 (s, Phth), 133.99 (d, Phth), 151.26 (s, C-7a), 168.38 (s,
C=O).
Ber: C: 73.96, H: 5.52, N: 9.58; gef : C: 73.89, H: 5.57, N: 9.55.
MS (EST): 293 (MH+, 100%)
3-(N-Phthaloyl-2-aminoethyl)-l-(2,,3',4'-tri-O-acetyl-ß-D-ribo-pyranosyl)-indol
Unter Stickstoffatmosphäre wurden 45.2 g (155 mmol) A und 23.2 g (155 mmol; 1.0 eq.) D-Ribose in 750 ml trockenem Ethanol suspendiert und 4 h zum Rückfluß erhitzt (DC- Kontrolle: CH2Cl2/MeOH 10: 1). Nach abkühlen auf RT wurde im Vak. eingeengt. Der Rückstand wurde in 300 ml Pyridin gelöst und unter Eiskühlung mit 155 ml Essigsäureanhydrid versetzt. Nach 15 min. wurde das Eisbad entfernt und 18 h bei RT gerührt (DC-Kontrolle: EtOAc/iso-Hexan 1 : 1). Diese Lösung wurde im Vakuum eingeengt und 3 mal mit je 300 ml Toluol coevaporiert. Das erhaltene Öl wird in 900 ml Dichlormethan gelöst und unter Eiskühlung mit 38.8 g (171 mmol; 1.1 eq.) 2,3-Dichlor-5,6- dicyanoparachinon versetzt. Nach 15 min. wurde das Eisbad entfernt und 1.5 h bei RT nachgerührt (DC-Kontrolle: EtOAc/iso-Hexan 1 : 1). Der ausgefallene Niedercshlag wurde abgesaugt und mit Dichlormethan gewaschen und verworfen. Das Filtrat wurde mit 600 ml ges. NaHCO3-Lösung gewaschen. Der dabei ausgefallene Niederschlag wurde erneut abgesaugt und mit Dichlormethan gewaschen und verworfen. Die vereinigten organischen
Extrakte wurden über NaSO4 getrocknet und im Vak. eingeengt. Der Rückstand (90.9 g) wurde durch Flashchromatographie an Kieselgel 60 gereinigt (10 x 25 cm; EtOAc/iso- Hexan 2:3).
Man erhielt: 21.5 g reines B und 46.83 g Mischfraktionen, die nach erneuter Chromatographie weitere 20.4 g reines B lieferten. Gesamtausbeute: 41.9 g (76 mmol) B, d. s. 49%.
'H-NMR (CDC13, 300 MHz): 1.64, 1.98, 2.19 (3 s, 3 x 3 H, Ac), 3.06 (t, J = 8.0 Hz, 2 H, CH2CH2NPhth), 3.81-4.00 (m, 4 H, H-5'ax, H-5'eq, CH2NPhth), 5.13 (ddd, J = 2.5, 6.0, 10.5 Hz, 1 H, H-4'), 5.36 (dd, J = 3.5, 9.5 Hz, 1 H, H-2'), 5.71 (d, J = 9.5 Hz, 1 H, H-l'), 5.74 (app t, J = 3.0 Hz, 1 H, H-3'), 7.02 (s, 1 H, H-2), 7.04-7.10, 7.13-7.19 (2 m, 2 x 1 H, H-5, H-6), 7.33 (d, J = 8.0 Hz, 1 H, H-7), 7.58-7.66, 7.72-7.80 (2 m, 5 H, Phth, H-4). I3C-NMR (CDCI3, 75 MHz): 20.23, 20.65, 20.87 (3 q, Ac), 24.41, 38.28 (2 t, CH2CH2), 63.53 (t, C-5'), 66.24, 68.00, 68.64 (3 d, C-2', C-3', C-4'), 80.33 (d, C-l'), 109.79 (d, C-7), 113.95 (s, C-3), 1 19.33, 120.39, 122.04, 122.47 (4 d, C-4, C-5, C-6, C-7), 123.18 (d, Phth), 128.70, 132.17 (2 s, C-3a, Phth), 133.87 (d, Phth), 136.78 (s, C-7a), 168.24, 168.77, 169.44, 169.87 (4 s, C=O).
Ber: C: 63.50, H: 5.15, N: 5.1 1; gef : C: 63.48, H: 5.16, N: 5.05. MS (ES+): 566 (M+NH , 82%), 549 (MIT, 74%), 1 14 (100%).
3-(N-PhthaloyI-2-aminoethyl)-l-ß-D-ribo-pyranosyl-indol
Unter Stickstoffatmosphäre wurden 44.1 g (80 mmol) A in 400 ml wasserfreiem Methanol gelöst. Unter Eiskühlung versetzte man mit 4.0 ml 30%iger Natriummethylatlösung und
ruhrte dann 18 h bei RT Der ausgefallene Niederschlag wurde abgesaugt und mit kaltem Ethanol gewaschen Das Filtrat wurde im Vak eingeengt Der Ruckstand wurde in Dichlormethan aufgenommen Diese Losung wurde mit ges NaHCO^-Losung gewaschen, über NaSO4 getrocknet und im Vak eingeengt Der erhaltene Ruckstand wurde zusammen mit dem aus der Reaktionslosung ausgefallenen Niederschlag aus heißem Ethanol umkristallisiert Man erhielt 22.6 g B, Smp 196-198 °C Die Mutterlauge wurde im Vakuum eingeengt und der Ruckstand erneut aus Ethanol umkπstallisiert Man erhielt weitere 9 2 g B, Smp 188-194 °C Gesamtausbeute 25 8 g B, d s 76%
1H-NMR (MeOD, 300 MHz) 3 09 (app t, J = 7 0 Hz, 2 H, CH2CH2NPhth), 3 64-3 98 (m, 5 H, H-4', H-5'ax, H-5'eq, CH2NPhth), 4 05 (dd, J = 3 5, 9 5 Hz, 1 H, H-2'), 4 22 (app t, J = 3 0 Hz, 1 H, H-3'), 5 65 (d, J = 9 5 Hz, 1 H, H-l'), 6 95-7 05, 7 09-7 16 (2 m, 2 x 1 H, H-5, H-6), 7 25 (s, 1 H, H-2), 7 44 (d, J = 8 0 Hz, 1 H, H-7), 7 60 (d, J = 8 0 Hz, 1 H, H- 4), 7 74-7 84 (m, 4 H, Phth)
13C-NMR (d6-DMSO, 75 MHz) 23 87, 37 79 (2 t, CH2CH2NPhth), 64 82 (t, C-5'), 66 74 (d, C-4'), 68 41 (d, C-2'), 71 42 (d, C-3'), 81 37 (d, C-l'), 110 42 (d, C-7), 111 05 (s, C-3), 118 17, 119 21, 121 36, 122 92, 123 80 (5 d, C-2, C-4, C-5, C-6, NPhth), 127 86, 131 59 (2 s, C-3a, Phth), 134 27 (d, Phth), 136 62 (s, C-7a), 167 72 (s, C=O) MS (ES") 457 (M+OH" +H2O, 49%), 439 (M+OH", 100%), 421 (M-H\ 28%)
l-(2'-O-Benzoyl-ß-D-ribo-pyranosyl)-3-(N-phthaloyl-2-aminoethyI)-indol
Unter Stickstoffatmoshare wurde 10 6 g (25 mmol) A in 250 ml trockenem Dichlormethan aufgenommen. Man versetzt mit 305 mg DMAP (2 5 mmol) und 20 ml Pyridin Es wurde
erwärmt bis alles in Losung war und anschließend auf -78 °C abgekühlt. Jetzt wurde 3.35 ml Benzoylchlorid (28 8 mmol) geloßt in 8 ml Dichlormethan innerhalb von 15 min zugetropft. DC-Kontrolle (EtOAc/Hexan 3 1) nach weiteren 30 min zeigte vollständige Reaktion an. Nach 45 min wurde die kalte Losung über einen Faltenfilter direkt auf 200 ml ges. NHjCl-losung gegeben und der Filterruckstand wurde mit Dichlormethan gewaschen. Die organische Phase wurde einmal mit Wasser gewaschen, über MgSO4 getrochnet und eingeengt. Der Ruckstand wurde 2 mal mit Toluol coevaporiert und durch Flashchromatographie an 10 x 20 cm Kieselgel mit EtOAc/Hexan 3 1 gereinigt Man erhiehlt 8 1 g B (64%)
'H-NMR (CDC13, 300 MHz) 2 45, 2 70 (2 bs, 2 x 1 H, OH), 3 04 (t, J = 8 0 Hz, 2 H, CH2CH2NPhth), 3 80-4 20 (m, 5 H, H-4'. H-5'ax, H-5'eq, CH2NPhth), 4 63 (bs, 1 H, H-3'), 5 46 (dd, J = 3 5, 9 5 Hz, 1 H, H-2'), 6 03 (d, J = 9 5 Hz, 1 H, H-l'), 7 08-7 31 (m, 5 H, H- 2, H-5, H-6, Bz-m-H), 7 41-7 48 (m, 1 H, H-Bz-p-H), 7 50 (d, J = 8 0 Hz, 1 H, H-7), 7 64- 7 79 (m, 7 H, Phth, H-4, Bz-o-H)
13C-NMR (dö-DMSO, 75 MHz) 24 40, 38 22 (2 t, CH2CH2NPhth), 65 95 (t, C-5'), 66 65 (d, C-4'), 69 55 (d, C-3'), 71 87 (d, C-2'), 79 57 (d, C-l'), 109 96 (d, C-7), 1 13 70 (s, C-3), 119.21, 120 21, 122 1 1, 122 41, 123 14 (5 d, C-2, C-4, C-5, C-6, NPhth), 128 28 (d, Bz), 128 58, 128 59 (2 s, C-3a, Bz), 129 62 (d, Phth), 132.05 (s, Phth), 133 81 (Bz), 136 97 (s, C-7a), 165 12, 168 29 (2 s, C=O) MS (ES") 525 (M-H\ 12%), 421 (M-PhCOτ, 23%), 107 (100%)
l-{3,-O-Benzoyl-4'O-[(4,4,-dimethoxytriphenyl)-methyl]-ß-D-ribo-pyranosyI}-3-(N- phthaloyI-2-aminoethyI)-indol

Unter Stickstoffatmoshare wurde 8.9 g (16.9 mmol) A in 135 ml trockenem Dichlormethan suspendiert Man versetzte mit 206 mg DMAP (1 68 mmol), 5 8 ml N-Ethyldiisopropylamin (33.7 mmol) und ca 12 ml Pyridin (bis zur vollständigen Losung) Jetzt wurde mit 34 g Molsieb 4Ä versetzt und 30 min gerührt. Nach Abkühlen auf 0 °C wurde mit 11 4 g DMTCl (33.7 mmol) versetzt und nach Entfernen des Kuhlbads 75 min gerührt. Dann wurden nochmals 1.94 g (0.34 eq) und nach weiteren 40 min 1.14 g (0.2 eq) und nach weiteren 65 min 1 14 g DMTCl (0 2 eq) zugegeben. Nach 4 25 h war die Reaktion beendet. Man versetzte dann mit 25.3 ml n-Propanol (20 eq), rührte noch 30 min nach und engte dann vorsichtig ein (Schaumbildung) Der Rückstand wurde in 100 ml Pyridin geloßt Man versetzte mit 1 85 g DMAP (15 1 mmol, 0 9 eq), 13 05 ml N-Ethyldiisopropylamin (101 mmol, 6 0 eq), 71 ml n-Propanol (940 mmol; 56 eq) und 3 74 g p-Nitrophenol (26 9 mmol, 1 6 eq) Diese Mischung wurde unter Stickstoff 96 h bei 75-80 °C gerührt Nach Abkühlen auf Raumtemperatur wurde die Mischung über Celite filtiert und eingeengt Der Ruckstand wurde durch Flashchromatographie an 9 x 17 cm Kieselgel mit Toluol/Diethylether/Triethylamin 90 10.1 gereinigt. Die produkthaltuigen Fraktionen (9.25 g) wurden zunächst aus EtOAc umkristallisiert und anschließend aus Toluol/Methanol umgefällt. Man erhielt 5 86 g B (42%).
1H-NMR (CDC13, 300 MHz). 2 64 (bs, 1 H, OH), 2 68 (dd, J = 5 0, 1 1 5 Hz, 1 H, H-5'eq), 2 94 (dd. J = 7 5, 16 0 Hz, 1 H, CH2CH2NPhth), 3 03 (dd, J = 8 0, 16 0 Hz. 1 H,
CH2CH2NPhth), 3 67-3 74 (m, 1 H, H-5'ax), 3 69, 3 70 (2 s, 2 x 3 H, OMe), 3 85 (t, J =
7 5 Hz, 2 H, CH2CH2NPhth), 3 94 (ddd, J = 3 0, 5 0, 10 5 Hz, 1 H, H-4'), 4 03 (dd, J = 3 5,
9 0 Hz, 1 H, H-2'), 5 51 (d, J = 9 0 Hz, 1 H, H-l'), 5 86 (bs, 1 H, H-3'), 6 68-7 66 (m, 25
H), 8 19-8 30 (m, 2 H). 13C-NMR (CDC13, 75 MHz). 24 16, 38 80 (2 t, CH2CH2NPhth), 55 25, 55 26 (2 q, Ome),
65.58 (t, C-5'), 68.29, 69 19, 73,83 (3 d, C-2', C-3', C-4'), 83.03 (d, C-l'), 87.31
(CAr3)110 03 (d, C-7), 113.37, 113 47 (2 d), 113.53 (s, C-3), 118.95, 120.20, 122.28,
122.31, 123.10, 12707, 128.02, 128.08, 128.68 (9 d), 12874 (s), 13002, 130.19, 130.22
(3 d), 130.37, 131.95 (2 s), 133.40, 133.83 (2 d), 135.98, 136.14, 136.56, 145.12, 158.82, 166 76, 168.52 (7 s, C-7a, 2 COMe, 2 C=O).
l- 'O^AIlyloxyXdiisopropylamino^hosphino^S'-O-BenzoyMO-^^'- dimethoxytriphenyl)-methyl]-ß-D-ribo-pyranosyl}-3-(N-phthaloyl-2-aminoethyl)- indol (2 Diastereomere)
Unter Argonatmosphäre wurde 1658 mg Alkohol A (2.0 mmol) in 10 ml trockenem Dichlormethan geloßt. Man versetzte mit 1.03 ml N-Ethyldiisopropylamin (6.0 mmol) und 0.63 ml Phosphorigsäuremonoallylesterdiisopropylamidchlorid (2.8 mmol) und rührte 1 h bei Raumtemperatur. Dann wurde das überschüssige Phosphorylierungsreagenz durch Zugabe von 61 μl (0.8 mmol) Isopropanol zerstört. Nach 10 min wurde im Vakuum eingeengt und der Rückstand durch Flashchromatographie an 3.3 x 21 cm Kieselgel mit Hexan/EtOAc/NEt3 (75:25: 1) gereinigt. Die produkthaltigen Fraktionen wurden eingeengt, in CC1 aufgenommen und wieder eingeengt. Man erhielt 2.04 g eines fast farblosen Schaums (quant.), der so direkt zur Oligomerisierung verwendet werden kann und bei -20 °C mehrere Wochen haltbar ist. DC auf Kieselgel (EtOAc/Hexan NEt 33:66: 1): 0.41
Η-NMR (CDC13, 300 MHz): Ausgewählte charakteristische Lagen: 2.42, 2.53 (2 dd, J = 5.0, 11.0 Hz, 2 H, 2 H-5'eq), 3.76, 3.77, 3.78, 3.79 (4 s, 4 x 3 H, OMe), 5.70, 5.73 (2 d, J = 9.0 Hz, 2 H, 2 H-l'), 6.16, 6.29 (2 bs, 2 H, 2 H-3'). 31P-NMR (CDCI3): 150.6, 151.0
5.3 Lysin-basierender Linker
Die Synthese ist im Schema 7 abgebildet und wird im folgenden im Detail beschrieben.
OH
Schema 7 Synthese des Lysinlinkers
6-Amino-2(S)-hydroxyhexansaure (1) wurde nach literaturbekannter Weise durch Diazotierung und anschließebnde Hydrolyse aus L-Lysin hergestellt (K -I Aketa. Chem Pharm Bull 1976, 24, 621)
2-(S)-N-Fmoc-6-amιno- 1 ,2-hexandιol (2)
3 4 g LiBHj (156 mmol, 4 eq) werden unter Argon in 100 ml abs THF gelost (exotherm') Nach Abkühlen auf ca 30 °C werden 39 6 ml TMSC1 (312 mmol, 8 eq) langsam zugetropft (Gasentwicklung!), wobei sich ein Niederschlag bildet Anschließend werden im Argon- Gegenstrom 5 74 g 6-Amino-2(S)-hydroxyhexansaure (1) (39 mmol) portionsweise zugegeben und es wird auf 65 °C erwärmt, bis das DC (Kieselgel, 1-PrOH/konz. NHUOH/Wasser 7 2.1, Anfärben mit Ninhydπn) kein Edukt mehr zeigt (ca 3 h) Unter Eiskuhlung wird vorsichtig mit 120 ml Methanol versetzt (starke Gasentwicklung I) Das Lösungsmittel wird im Vakuum eingeengt, der Ruckstand wird 3 mal mit je 200 ml Methanol coevaporiert und anschließend in 100 ml abs. DMF gelost Nach Zugabe von 16 ml Ethyldiisopropylamin (93 6 mmol, 2 4 eq) wird die Mischung auf 0°C gekühlt und portionsweise mit 12 1 g FmocCl (46 8 mmol, 1 2 eq) versetzt Nach 15 Minuten wird das Kuhlbad entfernt und bei Raumtemperatur gerührt bis das Edukt verbraucht ist (ca 3 h, DC-Kontrolle. Kieselgel, CHCl3/MeOH/HOAc/Wasser 60.30 3 5) Die Reaktionslosung
wird auf 600 ml ges. NaHCO3-Lösung gegeben. Der Niederschlag wird abfiltriert, mit 200 ml Wasser gewaschen und bei 50 °C am HV getrocknet bis zur Gewichtskonstanz (ca. 6 h). Man erhält 13.9 g eines farblosen Feststoffs, der aus Ethylacetat (40 ml)/n-Hexan (35 ml) umkristallisiert wird. Ausbeute: 9.05 g (65%).
Η-NMR (300 MHz, CDC13): 7.68, 7.51 (2 d, J = 8.0 Hz, je 2 H, Ar-H), 7.32 (t, J = 8.0 Hz, 2 H, Ar-H), 7.23 (dt, J = 1.6, 8.0 Hz, 2 H, Ar-H), 4.92 (bs, 1 H. NH), 4.32 (d, J = 7.0 Hz, 2 H, OCOCH2), 4.13 (bt, J = 7.0 Hz, 1 H, OCOCH2CH), 3.64-3.58 (m, 1 H, H-l, H-l ', H-2, H-6, H-6'), 3.54 (dd, J = 3.2, 11.0 Hz, 1 H, H-l, H-l', H-2, H-6, H-6'), 3.35 (dd, J = 7.4, 1 1.0 Hz, 1 H, H-l, H-l ', H-2, H-6, H-6'), 3.16-3.06 (m, 2 H, H-l, H-l ', H-2, H-6, H-6'), 3.0-2.0 (bs, 2 H, OH), 1.52-1.18 (m, 6 H, H-3, H-3', H-4, H-4\ H-5, H-5').
2-(S)-N-Fmoc-θ'-DMT-6-amino-l,2-hexandiol (3) wurde nach WO 89/02439 DM- trityliert.
2-(S)-N-Fmoc-O1-DMT-O2-allyloxydiisopropylaminophosphinyl-6-amino-l,2-hexandiol (4)
Zu einer Lösung von 670 mg des Alkohols (3) (1.02 mmol) in 10 ml abs. Dichlormethan werden unter Argon 0.51 ml Ethyldiisopropylamin (3.0 mmol, 3 eq) und 0.33 ml Chlor- N,N-diisopropylaminoallyloxyphosphin ( 1.5 mmol, 1.5 eq) gegeben. Man rührt 2 h bei Raumtemperatur, zieht das Lösungsmittel im Vakuum ab und reinigt den erhaltenen Rückstand durch Flashchromatographie an 3.2 x 16 cm Kieselgel (EtOAc/iso-Hexan/NEt3 20:80: 1). Man erhält 839 mg (97%) eines leicht gelblichen Öls.
DC: Kieselgel; EtOAc/iso-Hexan/NEt3 50:50: 1; UV; Rf = 0.77.
1H-NMR (300 MHz, CDC13): 7.70-6.68 (m, 21 H, Ar-H), 4.92-4.62 (m, 1 H. NH), 4.31 (d,
J = 7.0 Hz, 2 H, OCOCH2), 4.13 (t, J = 7.0 Hz, 1 H, OCOCH2CH), 3.98-3.40 (m, 5 H),
3.77 (2 s, je 3 H, OMe), 3.16-2.86 (m, 4 H), 2.58 (t, J = 7.0 Hz, 1 H, CHCN), 2.38 (t, 1 H, CHCN), 1.80-1.20 (m, 6 H), 1.20, 1, 18, 1.17, 1.16, 1.15, 1.13, 1.08, 1.06 (8 s, 12 H,
NMe).
31ι -NMR (300 MHz, CDC13). 149 5, 149.0 (2 s)
Beispiel 6
Synthese eines p-RNA-Oligos der Sequenz 4 '-Indollιnker-A8-2 ' unter Verwendung von Benzimidazohumtrißat als Kupplungsreagenz
108 mg Indollinker-Phosphoramidit und 244 mg A-Phosphoramidit werden in Svnthesizerglaschen eingewogen und für 3 h im Exsikkator über KOH zusammen mit dem mit 28, 1 mg CPG-Trager, beladen mit A-Baustein, gefüllten Saulchen am HV belassen Die Phosphoramidite werden in 1 ml (Indollinker) bzw 2,5 ml (A-Phosphoramidit) Acetonitril gelost und einige Kügelchen von dem Molsieb zugesetzt und über KOH geschlossen im Exsikkator belassen. 200 mg Jod werden unter starkem Rühren in 50 ml Acetonitril gelost Nachdem alles gelost ist (Sichtkontrolle) werden 23 ml Wasser und 4,6 ml sym-Collidin zugegeben und die Lösung einmal gut durchmischt Zum Detritylieren wird eine 6 %>ige Losung von Dichloressigsaure in Dichlormethan eingesetzt. Das Cappingreagenz (Acetanhydrid + Base) wird wie für Oligonucleotidsynthese üblich gekauft und verwendet Benzimidazoliumtπflat wird aus heißem Acetonitril umkristallisiert und getrocknet Mit den fast farblosen Kristallen wird eine 0, 1 M Losung in wasserfreiem Acetonitril als Kupplungsreagenz hergestellt Wahrend der Synthese bleibt diese Losung immer klar und es kommt zu keinen Verstopfungen der Synthesizerschläuche Abgeänderter DNA-Kupplungscyclus am Eppendorf Ecosyn 300+ (DMT-on): Detritylierung 7 Minuten
Kupplung 1 Stunde
Capping 1,5 Minuten
Oxidation 1 Minute
20 mg Tetrakis(triphenylphosphin)palladium wird in 1,5 ml Dichlormethan gelost, 20 mg Diethylammoniumhydrogencarbonat, 20 mg Triphenylphosphin und der das Oligonucleotid tragende Glastrager zugesetzt, dicht verschlossen (Parafilm) und das Gläschen 5 h bei RT.
bewegt. Dann wird der Glasträger über eine Analysennutsche abgesaugt, und mit Dichlormethan, mit Aceton und mit Wasser gewaschen.
Der Träger wird mit wäßriger 0, 1 molarer Natriumdiethyldithiocarbamatlösung aufgeschlämmt und 45 min bei RT. belassen. Man saugt ab, wäscht mit Wasser, Aceton,
Ethanol und Dichlormethan. Der Träger wird in 1,5 ml 24 %iger Hydrazinhydratlösung suspendiert, 24-36 h lang bei 4 °C gerüttelt und mit 0, 1 molarem
Triethylammoniumhydrogencarbonatpuffer (TEAB-Puffer) auf 7 ml verdünnt. Über eine
Waters Sep-Pak Cartridge wurde hydrazinfrei gewaschen. Es wird mit 5 ml einer 80%>igen Ameisensäurelösung versetzt, und nach 30 min zur Trockene einrotiert. Der Rückstand wird in 10 ml Wasser aufgenommen, mit Dichlormethan extrahiert, die wäßrige Phase eingeengt und nun HPL-chromatographiert (tR = 33 min, Gradient von Acetonitril in 0, 1M
Triethylammoniumacetat-Puffer). Übliche Entsalzung (Waters Sep-Pak Cartridge) liefert das Oligonucleotid. Ausbeute: 17, 6 OD.
Substanzidentität nachgewiesen durch ESI-Massenspektroskopie: M(ber) = 3082 D, (M+2H) +(gef) = 1541,9 D.
Beispiel 7 Herstellung von Konjugaten
1. Sequentielles Verfahren
Zuerst wird, wie in Beispiel 2 beschrieben, ein p-RNA-Oligomeres der Sequenz A8, d. h. ein Octamer, auf dem Eppendorf Ecosyn D 300+ hergestellt und dann die folgenden Reagenzien ausgetauscht: 6 %ige Dichloressigsäure gegen 2 %>ige Trichloressigsäure, Jod in Collidin gegen Jod in Pyridin, Benzimidazoliumtriflatlösung gegen Tetrazollösung. Nach Änderung des Syntheseprogramms wird ein DNA-Oligomeres der Sequenz GATTC nach bekannten Methoden (M. J. Gait, Oligonucleotide Synthesis, IRL Press, Oxford, UK 1984) weiter synthetisiert. Die Deallylierung, Hydrazinolyse, HPL-Chromatographie und Entsalzung erfolgt wie für das p-RNA-Oligomere beschrieben (siehe oben) und liefert das gewünschte Konjugat.
2. Konvergentes Verfahren
Wie in Beispiel 2 beschrieben, wird ein p-RNA-Oligomeres mit der Sequenz 4'-Indollinker- Ag-2' hergestellt, aufgereinigt, und jodacetyliert. Ein DNA-Oligomeres der Sequenz GATTC-Thiol-Linker wird nach bekannten Methoden (M. J. Gait, Oligonucleotide Synthesis, ERL Press, Oxford, UK 1984) synthetisiert und aufgereinigt (3'-Thiol-Linker von Glen Research: Nr. 20-2933). Beim Stehenlassen der beiden Fragmente (T. Zhu et al., Bioconjug. Chem. 1994, 5, 312) in gepufferter Lösung entsteht das Konjugat, das abschließend über HPLC aufgereinigt wird.
Beispiel 8
Konjugation eines Biotinrestes an eine aminomodifizierie p-RNA:
Zuert wurde analog wie in Beispiel 6 beschrieben, ein p-RNA Oligomer der Sequenz TAGGCAAT, welches am 4' -Ende mittels des 5'-Aminomodifier 5 von Eurogentec (2-(2- (4-Monomethoxytrityl)aminoethoxy)ethyl-(2-cyanoethyl)-(N,N-diisopropyl)-phosphor- amidit) mit einer Aminogruppe versehen ist, synthetisiert und aufgearbeitet. Das Oligonucleotid (17,4 OD, 0, 175 μmol) wurde in 0,5 ml basischem Puffer aufgenommen, 1, 14 mg (2,5 μmol) Biotin-N-hydroxysuccinimidester in 1 14 μl DMF (abs.) gelöst und lh bei RT stehengelassen. Das entstandene Konjugat wurde mittels präparativer HPLC gereinigt und das reine Produkt mit einer Sepak entsalzt.
Ausbeute: 8.6 OD (49%)
M (ber.) = 3080 D, M (fef) = 3080,4 D
Beispiel 9 Herstellung Cyanin- bzw. Biotin-markierter p-RNA online
Die verschiedenen AT,G,C und Ind (Ind = Aminoethylindol als Nucleobase) Phosphoramidite wurden zuerst nach bekannten Verfahren hergestellt. Cyanin (Cy3-CE) und Biotin Phosphoramidite wurden bei Glen Research erhalten.
vollautomatische Festphasensynthese wurde mit jeweils 15 μmol durchgeführt. Ein Synthesezyklus besteht aus den folgenden Schritten
(a) Detritylierung: 5 Minuten mit 6%> DCA (Dichloressigsäure) in CH2C12 (79 ml);
(b) Waschen mit CH2C1 (20 ml), Acetonitril (20 ml) und danach spülen mit Argon; (c) Kupplung: Waschen des Harz mit dem Aktivator (0,5 M Pyridin.HCl in CH2C12, 0,2 ml;
30-minütiges Behandeln mit Aktivator (0,76 ml) und entsprechendes Phosphoramidit (0,76 ml : 8 eq; 0, 1 M in Acetonitril) im Verhältnis 1 : 1;
(d) Capping: 2 Minuten mit 50% Cap A (10,5 ml) und 50% Cap B (10,5 ml) von Perseptive (Cap A: THF, Lutidine, Acetanhydrid; Cap B: 1-Methylimidazol, THF,
Pyridin).
(e) Oxidation: 1 Minute mit 120 ml Iodlösung (400 mg Jod in 100 ml Acetonitril, 46 ml H2O und 9,2 ml sym-Collidine).
(f) Waschen mit Acetonitril (22 ml).
Zur Erleichterung der nachfolgenden HPLC-Reinigung der Oligonucleotide wurde die letzte DMT(Dimethoxytrityl)- bzw. MMT (Monomethoxytrityl)-Schutzgruppe von Biotin- bzw. Cyanin-Monomeren nicht abgespalten. Der Nachweis der letzten Kupplung mit den modifizierten Phorphoramiditen erfolgt nach der Synthese mit 1% des Harzes mittels Tritylkationabsorption in UV (503 nm).
Aufarbeitung des Oligonucleotids:
Die Abspaltung der Allyletherschutzgruppen erfolgte mit einer Lösung von Tetrakis(triphenylphosphin)palladium (272mg), Triphenylphosphin (272 mg) und
Diethylammoniumhydrogencarbonat in CH2C12 (15ml) nach 5 Stunden bei RT. Die
Glasträger werden danach mit CH2CL2 (30ml), Aceton (30ml) und Wasser (30ml)
gewaschen. Um Palladiumkomplexreste zu entfernen, wurde das Harz mit einer wäßrigen 0, 1 M Natriumdiethyldithiocarbamathydratlosung gespult Die oben erwähnte Waschoperation wurde in einer umgekehrten Reihe noch einmal durchgeführt. Anschließend wurde das Harz am Hochvakuum 10 Minuten getrocknet. Der Abspaltungsschritt vom Glastrager bei gleichzeitiger Debenzoylierung wurde in 24% Hydrazinhydratlosung (6ml) bei 4°C durchgeführt Nach HPLC-Kontrolle an RP 18 (18-25 Stunden) wurde das Oligonucleotid „Trityl ON" mittels einer aktiviert (Acetonitril, 20 ml) Waters Sep-Pak Cartridge vom Hydrazin befreit. Das Hydrazin wurde mit TEAB 0, 1M (30ml) gewaschen Das Oligonucleotid wurde dann mit Acetonitril/TEAB 0, 1M (10ml) eluiert Man reinigte mittels HPLC (zur Abtrennung von Abbruchsequenzen) und führte die DMT-Entschutzung (30 ml 80%ig wäßrige Ameisensaure) durch Abschließende Entsalzung (über Sep-Pak Kartuche, mit TEAB Puffer 0, 1 M/ Acetonitril 1/1) lieferte die reinen Cyanin- bzw Biotin- markierten Oligomeren.
Ein Aliquot dieser Oligolosung wurde für die Durchführung einer ESI-MS verwendet. 4' Cy-AIndTTCCTA 2' berechnet M = 3026, gefunden (M+HT = 3027.
4' Biotin-TAGGAAIndT 2' berechnet M = 3014, gefunden (M+2H) + m/z 1508 und (m+H)~ m/z 3015
Die Oligos wurden zur Lagerung gefriergetrocknet
Beispiel 10
Jodacetylierung von p-RNA mit N-(]odacetyloxy)-succιmmιd
/7-RNA-Sequenz . 4' AGGCAIndT 2' Mw = 2266,56 g/mol (Ind = Indol-CH2-CH2-NH2- Linker)
1 eq. der p-RNA wurde in einer 0, 1 molaren Natriumhydrogencarbonatlosung (pH 8,4) gelost (1 ml pro 350 nmol) und mit einer Losung von N-(jodacetyloxy)-succinimid in DMSO versetzt (40 μl pro mg) Man dunkelte den Ansatz mit Aluminiumfolie ab und beließ ihn bei Raumtemperatur für 30-90 Minuten.
Der Fortgang der Reaktion wurde mittels analytischer HPLC verfolgt Die
Standardbedingungen sind
Puffer A 0, 1 molarer Tπethylammoniumacetat-Puffer in Wasser Puffer B 0, 1 molarer Tπethylammoniumacetat-Puffer in Wasser Acetomtπl 1 4
Gradient von 10% B startend auf 50% B in 40 Minuten
Saulenmateπal 10 μM LiChrosphere ® 100 RP-18 von Merck Darmstadt GmbH, 250 x 4 mm
Retentionszeit der Edukte 18,4 Minuten Retentionszeit der Produkte in diesem Falle 23, 1 Minuten
Nach beendeter Reaktion wurde der Ansatz mit Wasser auf das vierfache Volumen verdünnt Man aktivierte eine Waters Sep-Pak-Kartusche RP-18 (ab 15 OD 2 g Füllung) mit 2 x 10 ml Acetonitril und 2 x 10 ml Wasser, trug das Oligo auf, ließ es einsinken, wusch das Reaktionsgefaß mit 2 x 10 ml Wasser, wusch mit 3 x 10 ml Wasser nach, um Salz und Reagenz zu entfernen, und eluierte zuerst mit 5 x 1 ml 50 1 Wasser Acetonitril und anschließend mit 1 1 Das Produkt eluierte in den 1 1 -Fraktionen in sehr guter Reinheit Die Fraktionen wurden in der Kalte und im Dunkeln eingeengt, vereinigt, und wieder eingeengt
Die Ausbeuten wurden mittels UV-Absorptionspektrometπe bei 260 nm bestimmt Massenspektrometπe
Sequenz 4' AGGCAInd(CH2CH2NHCOCH2-I)T 2' berechnete Masse 2434,50 g/mol gefundene Masse MH2 2+ 1217,9 g/mol = 2433 g/mol
Beispiel 1 1
Konjugation von p-RNA an ein Peptid der Sequenz CYSKVG
Die jodacetylierte p-RNA (Mw = 2434,50 g/mol) wurde in einem Puffersystem gelost (lOOOμl pro 114 nmol) und dann mit einer Losung des Peptides in Puffer versetzt (2 mol CYSKVG-Peptid, Mw = 655, 773 g/mol, 228 nmol in 20 μl Puffer)
Wasser Acetonitril 1 1. Die Produkt-Fraktionen wurden eingeengt, vereinigt und wieder eingeengt.
Die Ausbeuten wurden mittels UV-Absorptionspektrometrie bei 260 nm bestimmt. Sie erreichten 70-95% der Theoπe.
Massenspektrometrie
Sequenz . 4' AGGCAInd(CH2CH2NHCOCH2-CYSKVG)T 2' berechnete Masse 2962,36 g/mol gefundene Masse MH2 2+ 1482,0 g/mol = 2962 g/mol
Beispiel 12
Konjugation von p-RNA an eine Pepüdbibhothek
Die jodacetyherte p-RNA (Mw = 2434,50 g/mol wurde in einem Puffersystem gelost (1300 μl pro 832 nmol) und dann mit einer Losung der Peptidbibliothek (CKR-XX-OH), X = Arg, Asn, Glu, His, Leu, Lys, Phe, Ser, Trp, Tyr) in Puffer versetzt (8 mol, mittlere Molekulmasse Mm = 677,82 g/mol, 4,5 mg = 6,66 μmol in 200 μmol Puffer)
Puffersystem Borax/HCl-Puffer der Firma Riedel-de Haen, pH 8,0, wurde im Verhältnis 1 1 mit einer 10 millimolaren Losung von EDTA-Dinatπumsalz in Wasser gemischt und auf pH 6,6 mit HC1 eingestellt Man erhielt dadurch eine Losung, die 5 mM Na2EDTA enthalt
Man beließ den Ansatz bis zum voUstandien Umsatz bei Raumtermperatur im Dunkeln. Die Reaktion wurde mittels HPLC-Analytik verfolgt In diesem Fall war das Edukt nach 70 Stunden verschwunden.
Die Standardbedingungen der analytischen HPLC sind: Puffer A 0, 1 molarer Triethylarnmoniumacetat-Puffer in Wasser Puffer B 0, 1 molarer Triethylarnmoniumacetat-Puffer in Wasser.Acetonitril 1 4 Gradient ■ von 10% B startend auf 50% B in 40 Minuten Säulenmaterial . 10 μM LiChrosphere® 100 RP-18 von Merck Darmstadt GmbH, 250 x 4
Retentionszeit des Eduktes : 18,8 Minuten
Retentionszeit des Produktes: mehrere Peaks von 13,9-36,2 Minuten
Nach beendeter Reaktion wurde der Ansatz mit Wasser auf das vierfache Volumen verdünnt. Man aktivierte eine Waters Sep-Pak-Kartusche RP-18 (ab 15 OD 2g Füllung) mit 3 x 10 ml Acetoniril und 3 x 10 ml Wasser, trug das Oligo auf, ließ es einsinken, wusch das Reaktionsgefäß mit 2 x 10 ml Wasser nach, wusch die Kartusche mit 3 x 10 ml Wasser nach, um Salz und überschüssiges Peptid zu entfernen, und eluierte mit 1 : 1 Wasser : Acetonitril, bis UV-spektroskopisch kein Prodikt mehr eluierte. Die Franktionen wurden in Kälte und im Dunkeln eingeengt, vereinigt und wieder eingeengt.