WO2005019373A2 - Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) - Google Patents
Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) Download PDFInfo
- Publication number
- WO2005019373A2 WO2005019373A2 PCT/EP2004/009269 EP2004009269W WO2005019373A2 WO 2005019373 A2 WO2005019373 A2 WO 2005019373A2 EP 2004009269 W EP2004009269 W EP 2004009269W WO 2005019373 A2 WO2005019373 A2 WO 2005019373A2
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- aryl
- alkyl
- ligands
- transition metal
- carbene
- Prior art date
Links
- 239000003446 ligand Substances 0.000 title claims abstract description 167
- 150000003624 transition metals Chemical class 0.000 title claims abstract description 121
- 229910052723 transition metal Inorganic materials 0.000 title claims abstract description 115
- HZVOZRGWRWCICA-UHFFFAOYSA-N methanediyl Chemical compound [CH2] HZVOZRGWRWCICA-UHFFFAOYSA-N 0.000 title claims abstract description 88
- 229910052751 metal Inorganic materials 0.000 claims abstract description 67
- 239000002184 metal Substances 0.000 claims abstract description 67
- 230000007935 neutral effect Effects 0.000 claims abstract description 27
- 230000003647 oxidation Effects 0.000 claims abstract description 10
- 238000007254 oxidation reaction Methods 0.000 claims abstract description 10
- 150000002825 nitriles Chemical class 0.000 claims abstract description 4
- 150000003222 pyridines Chemical class 0.000 claims abstract description 4
- 150000001993 dienes Chemical class 0.000 claims abstract description 3
- 150000003003 phosphines Chemical class 0.000 claims abstract description 3
- 125000003118 aryl group Chemical group 0.000 claims description 123
- -1 alkenyl radical Chemical class 0.000 claims description 97
- 125000000217 alkyl group Chemical group 0.000 claims description 80
- 125000004429 atom Chemical group 0.000 claims description 70
- 150000003254 radicals Chemical class 0.000 claims description 66
- 125000001072 heteroaryl group Chemical group 0.000 claims description 63
- 229910052739 hydrogen Inorganic materials 0.000 claims description 56
- 229910052757 nitrogen Inorganic materials 0.000 claims description 54
- 125000004435 hydrogen atom Chemical class [H]* 0.000 claims description 51
- 239000001257 hydrogen Substances 0.000 claims description 49
- 125000004432 carbon atom Chemical group C* 0.000 claims description 37
- 125000005842 heteroatom Chemical group 0.000 claims description 35
- 239000000463 material Substances 0.000 claims description 35
- 150000005840 aryl radicals Chemical class 0.000 claims description 33
- 230000009471 action Effects 0.000 claims description 28
- 229910052799 carbon Inorganic materials 0.000 claims description 26
- 229910052760 oxygen Inorganic materials 0.000 claims description 26
- 125000003342 alkenyl group Chemical group 0.000 claims description 24
- 229910052717 sulfur Inorganic materials 0.000 claims description 20
- 229910052698 phosphorus Inorganic materials 0.000 claims description 17
- 239000002243 precursor Substances 0.000 claims description 16
- 125000001424 substituent group Chemical group 0.000 claims description 16
- 238000000034 method Methods 0.000 claims description 13
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 13
- 238000006243 chemical reaction Methods 0.000 claims description 11
- 238000002360 preparation method Methods 0.000 claims description 11
- 229910052697 platinum Inorganic materials 0.000 claims description 10
- 229920006395 saturated elastomer Polymers 0.000 claims description 10
- 150000001721 carbon Chemical group 0.000 claims description 9
- 229910052741 iridium Inorganic materials 0.000 claims description 9
- 125000006850 spacer group Chemical group 0.000 claims description 7
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 6
- 125000002947 alkylene group Chemical group 0.000 claims description 6
- 125000000732 arylene group Chemical group 0.000 claims description 6
- 230000008569 process Effects 0.000 claims description 6
- 229910052703 rhodium Inorganic materials 0.000 claims description 6
- 229910052707 ruthenium Inorganic materials 0.000 claims description 6
- 238000004040 coloring Methods 0.000 claims description 5
- 230000005595 deprotonation Effects 0.000 claims description 5
- 238000010537 deprotonation reaction Methods 0.000 claims description 5
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical group [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 claims description 4
- 125000004450 alkenylene group Chemical group 0.000 claims description 4
- 229910052802 copper Inorganic materials 0.000 claims description 4
- 230000001419 dependent effect Effects 0.000 claims description 4
- 125000005549 heteroarylene group Chemical group 0.000 claims description 4
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 3
- 229910052763 palladium Inorganic materials 0.000 claims description 3
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical class OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 claims description 2
- 229910052737 gold Inorganic materials 0.000 claims description 2
- 229910052742 iron Inorganic materials 0.000 claims description 2
- 229910052748 manganese Inorganic materials 0.000 claims description 2
- 229910052750 molybdenum Inorganic materials 0.000 claims description 2
- 229910052758 niobium Inorganic materials 0.000 claims description 2
- AQSJGOWTSHOLKH-UHFFFAOYSA-N phosphite(3-) Chemical class [O-]P([O-])[O-] AQSJGOWTSHOLKH-UHFFFAOYSA-N 0.000 claims description 2
- 229910052702 rhenium Inorganic materials 0.000 claims description 2
- 229910052709 silver Inorganic materials 0.000 claims description 2
- 229910052713 technetium Inorganic materials 0.000 claims description 2
- 229910052721 tungsten Inorganic materials 0.000 claims description 2
- 239000010410 layer Substances 0.000 description 130
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 111
- 239000000203 mixture Substances 0.000 description 52
- 239000000975 dye Substances 0.000 description 37
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 24
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 24
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 24
- 239000004926 polymethyl methacrylate Substances 0.000 description 24
- 239000000523 sample Substances 0.000 description 24
- 239000000243 solution Substances 0.000 description 24
- 150000001875 compounds Chemical class 0.000 description 23
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Substances [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 21
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 20
- 239000000370 acceptor Substances 0.000 description 20
- 238000001228 spectrum Methods 0.000 description 19
- 230000007704 transition Effects 0.000 description 19
- 239000000126 substance Substances 0.000 description 18
- 150000001408 amides Chemical group 0.000 description 17
- 230000001815 facial effect Effects 0.000 description 17
- 238000006862 quantum yield reaction Methods 0.000 description 17
- 125000004149 thio group Chemical group *S* 0.000 description 17
- 150000002148 esters Chemical group 0.000 description 16
- 229910052736 halogen Inorganic materials 0.000 description 16
- 125000003545 alkoxy group Chemical group 0.000 description 15
- 125000004104 aryloxy group Chemical group 0.000 description 15
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 15
- 238000005259 measurement Methods 0.000 description 15
- 229910052731 fluorine Inorganic materials 0.000 description 14
- 230000032258 transport Effects 0.000 description 14
- 230000003287 optical effect Effects 0.000 description 13
- 239000002904 solvent Substances 0.000 description 13
- 238000005160 1H NMR spectroscopy Methods 0.000 description 12
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 12
- 125000003277 amino group Chemical group 0.000 description 11
- 239000003086 colorant Substances 0.000 description 11
- 238000005401 electroluminescence Methods 0.000 description 11
- YUCFVHQCAFKDQG-UHFFFAOYSA-N fluoromethane Chemical compound F[CH] YUCFVHQCAFKDQG-UHFFFAOYSA-N 0.000 description 11
- 238000010521 absorption reaction Methods 0.000 description 10
- 238000000295 emission spectrum Methods 0.000 description 10
- 239000000843 powder Substances 0.000 description 10
- 239000000758 substrate Substances 0.000 description 10
- 230000006870 function Effects 0.000 description 9
- 238000010992 reflux Methods 0.000 description 9
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 8
- 238000004519 manufacturing process Methods 0.000 description 8
- 238000005424 photoluminescence Methods 0.000 description 8
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 7
- 238000000862 absorption spectrum Methods 0.000 description 7
- 239000002585 base Substances 0.000 description 7
- 230000000694 effects Effects 0.000 description 7
- 238000004020 luminiscence type Methods 0.000 description 7
- 239000000725 suspension Substances 0.000 description 7
- 150000001336 alkenes Chemical class 0.000 description 6
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 230000005284 excitation Effects 0.000 description 6
- 150000002739 metals Chemical class 0.000 description 6
- 239000001301 oxygen Substances 0.000 description 6
- 238000003786 synthesis reaction Methods 0.000 description 6
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 5
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 5
- 150000001412 amines Chemical group 0.000 description 5
- 238000010438 heat treatment Methods 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 239000000976 ink Substances 0.000 description 5
- 229920000642 polymer Polymers 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 238000004611 spectroscopical analysis Methods 0.000 description 5
- ADLVDYMTBOSDFE-UHFFFAOYSA-N 5-chloro-6-nitroisoindole-1,3-dione Chemical compound C1=C(Cl)C([N+](=O)[O-])=CC2=C1C(=O)NC2=O ADLVDYMTBOSDFE-UHFFFAOYSA-N 0.000 description 4
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 150000004703 alkoxides Chemical class 0.000 description 4
- 229910052786 argon Inorganic materials 0.000 description 4
- 230000008033 biological extinction Effects 0.000 description 4
- 239000002800 charge carrier Substances 0.000 description 4
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 4
- 238000004587 chromatography analysis Methods 0.000 description 4
- 238000004440 column chromatography Methods 0.000 description 4
- 150000004696 coordination complex Chemical class 0.000 description 4
- 238000004770 highest occupied molecular orbital Methods 0.000 description 4
- 230000005525 hole transport Effects 0.000 description 4
- 150000004693 imidazolium salts Chemical class 0.000 description 4
- 239000011261 inert gas Substances 0.000 description 4
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 4
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 4
- 239000012044 organic layer Substances 0.000 description 4
- 239000003973 paint Substances 0.000 description 4
- 239000000123 paper Substances 0.000 description 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 4
- 229920001467 poly(styrenesulfonates) Polymers 0.000 description 4
- IUBQJLUDMLPAGT-UHFFFAOYSA-N potassium bis(trimethylsilyl)amide Chemical compound C[Si](C)(C)N([K])[Si](C)(C)C IUBQJLUDMLPAGT-UHFFFAOYSA-N 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 239000004065 semiconductor Substances 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- 238000000859 sublimation Methods 0.000 description 4
- 230000008022 sublimation Effects 0.000 description 4
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 4
- DYLIWHYUXAJDOJ-OWOJBTEDSA-N (e)-4-(6-aminopurin-9-yl)but-2-en-1-ol Chemical compound NC1=NC=NC2=C1N=CN2C\C=C\CO DYLIWHYUXAJDOJ-OWOJBTEDSA-N 0.000 description 3
- POILWHVDKZOXJZ-ARJAWSKDSA-M (z)-4-oxopent-2-en-2-olate Chemical compound C\C([O-])=C\C(C)=O POILWHVDKZOXJZ-ARJAWSKDSA-M 0.000 description 3
- DHDHJYNTEFLIHY-UHFFFAOYSA-N 4,7-diphenyl-1,10-phenanthroline Chemical compound C1=CC=CC=C1C1=CC=NC2=C1C=CC1=C(C=3C=CC=CC=3)C=CN=C21 DHDHJYNTEFLIHY-UHFFFAOYSA-N 0.000 description 3
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 3
- WRYCSMQKUKOKBP-UHFFFAOYSA-N Imidazolidine Chemical class C1CNCN1 WRYCSMQKUKOKBP-UHFFFAOYSA-N 0.000 description 3
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 3
- 229920000297 Rayon Polymers 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 150000001298 alcohols Chemical class 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 3
- 238000010719 annulation reaction Methods 0.000 description 3
- 239000012682 cationic precursor Substances 0.000 description 3
- 239000004020 conductor Substances 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 239000010949 copper Substances 0.000 description 3
- 239000013078 crystal Substances 0.000 description 3
- 238000002425 crystallisation Methods 0.000 description 3
- 230000008025 crystallization Effects 0.000 description 3
- 238000000354 decomposition reaction Methods 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 238000001914 filtration Methods 0.000 description 3
- 239000000543 intermediate Substances 0.000 description 3
- MILUBEOXRNEUHS-UHFFFAOYSA-N iridium(3+) Chemical class [Ir+3] MILUBEOXRNEUHS-UHFFFAOYSA-N 0.000 description 3
- 125000002524 organometallic group Chemical group 0.000 description 3
- 230000000737 periodic effect Effects 0.000 description 3
- SIOXPEMLGUPBBT-UHFFFAOYSA-M picolinate Chemical compound [O-]C(=O)C1=CC=CC=N1 SIOXPEMLGUPBBT-UHFFFAOYSA-M 0.000 description 3
- 229960002796 polystyrene sulfonate Drugs 0.000 description 3
- 239000011970 polystyrene sulfonate Substances 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 239000011833 salt mixture Substances 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- FZHAPNGMFPVSLP-UHFFFAOYSA-N silanamine Chemical class [SiH3]N FZHAPNGMFPVSLP-UHFFFAOYSA-N 0.000 description 3
- CXNIUSPIQKWYAI-UHFFFAOYSA-N xantphos Chemical compound C=12OC3=C(P(C=4C=CC=CC=4)C=4C=CC=CC=4)C=CC=C3C(C)(C)C2=CC=CC=1P(C=1C=CC=CC=1)C1=CC=CC=C1 CXNIUSPIQKWYAI-UHFFFAOYSA-N 0.000 description 3
- APPOKADJQUIAHP-GGWOSOGESA-N (2e,4e)-hexa-2,4-diene Chemical compound C\C=C\C=C\C APPOKADJQUIAHP-GGWOSOGESA-N 0.000 description 2
- 125000001140 1,4-phenylene group Chemical group [H]C1=C([H])C([*:2])=C([H])C([H])=C1[*:1] 0.000 description 2
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical class C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 2
- IXHWGNYCZPISET-UHFFFAOYSA-N 2-[4-(dicyanomethylidene)-2,3,5,6-tetrafluorocyclohexa-2,5-dien-1-ylidene]propanedinitrile Chemical compound FC1=C(F)C(=C(C#N)C#N)C(F)=C(F)C1=C(C#N)C#N IXHWGNYCZPISET-UHFFFAOYSA-N 0.000 description 2
- VQGHOUODWALEFC-UHFFFAOYSA-N 2-phenylpyridine Chemical compound C1=CC=CC=C1C1=CC=CC=N1 VQGHOUODWALEFC-UHFFFAOYSA-N 0.000 description 2
- VFUDMQLBKNMONU-UHFFFAOYSA-N 9-[4-(4-carbazol-9-ylphenyl)phenyl]carbazole Chemical group C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 VFUDMQLBKNMONU-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical compound C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 239000002262 Schiff base Substances 0.000 description 2
- 150000004753 Schiff bases Chemical class 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- BCRJHHFLBOQAMG-YNRRLODASA-N [(1e,3e)-penta-1,3-dienyl]benzene Chemical compound C\C=C\C=C\C1=CC=CC=C1 BCRJHHFLBOQAMG-YNRRLODASA-N 0.000 description 2
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 2
- CUJRVFIICFDLGR-UHFFFAOYSA-N acetylacetonate Chemical compound CC(=O)[CH-]C(C)=O CUJRVFIICFDLGR-UHFFFAOYSA-N 0.000 description 2
- 125000005595 acetylacetonate group Chemical group 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- IYABWNGZIDDRAK-UHFFFAOYSA-N allene Chemical group C=C=C IYABWNGZIDDRAK-UHFFFAOYSA-N 0.000 description 2
- 150000001450 anions Chemical class 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 229910052788 barium Inorganic materials 0.000 description 2
- WZJYKHNJTSNBHV-UHFFFAOYSA-N benzo[h]quinoline Chemical compound C1=CN=C2C3=CC=CC=C3C=CC2=C1 WZJYKHNJTSNBHV-UHFFFAOYSA-N 0.000 description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- QARVLSVVCXYDNA-UHFFFAOYSA-N bromobenzene Chemical compound BrC1=CC=CC=C1 QARVLSVVCXYDNA-UHFFFAOYSA-N 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 238000011097 chromatography purification Methods 0.000 description 2
- URYYVOIYTNXXBN-UPHRSURJSA-N cyclooctene Chemical compound C1CCC\C=C/CC1 URYYVOIYTNXXBN-UPHRSURJSA-N 0.000 description 2
- 239000004913 cyclooctene Substances 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- 239000002019 doping agent Substances 0.000 description 2
- 238000000921 elemental analysis Methods 0.000 description 2
- 239000003480 eluent Substances 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- LEQAOMBKQFMDFZ-UHFFFAOYSA-N glyoxal Chemical compound O=CC=O LEQAOMBKQFMDFZ-UHFFFAOYSA-N 0.000 description 2
- 150000004820 halides Chemical class 0.000 description 2
- 150000008282 halocarbons Chemical class 0.000 description 2
- 238000011835 investigation Methods 0.000 description 2
- 239000004922 lacquer Substances 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 229910052744 lithium Inorganic materials 0.000 description 2
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 2
- 229910044991 metal oxide Inorganic materials 0.000 description 2
- 150000004706 metal oxides Chemical class 0.000 description 2
- IBHBKWKFFTZAHE-UHFFFAOYSA-N n-[4-[4-(n-naphthalen-1-ylanilino)phenyl]phenyl]-n-phenylnaphthalen-1-amine Chemical group C1=CC=CC=C1N(C=1C2=CC=CC=C2C=CC=1)C1=CC=C(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1 IBHBKWKFFTZAHE-UHFFFAOYSA-N 0.000 description 2
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 238000010606 normalization Methods 0.000 description 2
- 239000011368 organic material Substances 0.000 description 2
- RZXMPPFPUUCRFN-UHFFFAOYSA-N p-toluidine Chemical compound CC1=CC=C(N)C=C1 RZXMPPFPUUCRFN-UHFFFAOYSA-N 0.000 description 2
- 238000010422 painting Methods 0.000 description 2
- 239000000049 pigment Substances 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 229920003227 poly(N-vinyl carbazole) Polymers 0.000 description 2
- 229920000548 poly(silane) polymer Polymers 0.000 description 2
- 229920000767 polyaniline Polymers 0.000 description 2
- 229920002857 polybutadiene Polymers 0.000 description 2
- 229920000515 polycarbonate Polymers 0.000 description 2
- 239000004417 polycarbonate Substances 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 238000007639 printing Methods 0.000 description 2
- 239000011241 protective layer Substances 0.000 description 2
- 125000002577 pseudohalo group Chemical group 0.000 description 2
- 125000004076 pyridyl group Chemical group 0.000 description 2
- 238000010791 quenching Methods 0.000 description 2
- 230000000171 quenching effect Effects 0.000 description 2
- 239000002964 rayon Substances 0.000 description 2
- 230000009257 reactivity Effects 0.000 description 2
- 230000006798 recombination Effects 0.000 description 2
- 238000005215 recombination Methods 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 239000012047 saturated solution Substances 0.000 description 2
- 230000035939 shock Effects 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- ORFSSYGWXNGVFB-UHFFFAOYSA-N sodium 4-amino-6-[[4-[4-[(8-amino-1-hydroxy-5,7-disulfonaphthalen-2-yl)diazenyl]-3-methoxyphenyl]-2-methoxyphenyl]diazenyl]-5-hydroxynaphthalene-1,3-disulfonic acid Chemical compound COC1=C(C=CC(=C1)C2=CC(=C(C=C2)N=NC3=C(C4=C(C=C3)C(=CC(=C4N)S(=O)(=O)O)S(=O)(=O)O)O)OC)N=NC5=C(C6=C(C=C5)C(=CC(=C6N)S(=O)(=O)O)S(=O)(=O)O)O.[Na+] ORFSSYGWXNGVFB-UHFFFAOYSA-N 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 230000008646 thermal stress Effects 0.000 description 2
- JFLKFZNIIQFQBS-FNCQTZNRSA-N trans,trans-1,4-Diphenyl-1,3-butadiene Chemical compound C=1C=CC=CC=1\C=C\C=C\C1=CC=CC=C1 JFLKFZNIIQFQBS-FNCQTZNRSA-N 0.000 description 2
- 150000003623 transition metal compounds Chemical class 0.000 description 2
- ODHXBMXNKOYIBV-UHFFFAOYSA-N triphenylamine Chemical compound C1=CC=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-N 0.000 description 2
- 238000001291 vacuum drying Methods 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- RRKODOZNUZCUBN-CCAGOZQPSA-N (1z,3z)-cycloocta-1,3-diene Chemical compound C1CC\C=C/C=C\C1 RRKODOZNUZCUBN-CCAGOZQPSA-N 0.000 description 1
- VIMMECPCYZXUCI-MIMFYIINSA-N (4s,6r)-6-[(1e)-4,4-bis(4-fluorophenyl)-3-(1-methyltetrazol-5-yl)buta-1,3-dienyl]-4-hydroxyoxan-2-one Chemical compound CN1N=NN=C1C(\C=C\[C@@H]1OC(=O)C[C@@H](O)C1)=C(C=1C=CC(F)=CC=1)C1=CC=C(F)C=C1 VIMMECPCYZXUCI-MIMFYIINSA-N 0.000 description 1
- GEYOCULIXLDCMW-UHFFFAOYSA-N 1,2-phenylenediamine Chemical compound NC1=CC=CC=C1N GEYOCULIXLDCMW-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- 239000004912 1,5-cyclooctadiene Substances 0.000 description 1
- ZVJHJDDKYZXRJI-UHFFFAOYSA-N 1-Pyrroline Chemical class C1CC=NC1 ZVJHJDDKYZXRJI-UHFFFAOYSA-N 0.000 description 1
- KGLYHHCCIBZMLN-UHFFFAOYSA-N 1-methyl-4-[4-(4-methylphenyl)buta-1,3-dienyl]benzene Chemical compound C1=CC(C)=CC=C1C=CC=CC1=CC=C(C)C=C1 KGLYHHCCIBZMLN-UHFFFAOYSA-N 0.000 description 1
- IYZMXHQDXZKNCY-UHFFFAOYSA-N 1-n,1-n-diphenyl-4-n,4-n-bis[4-(n-phenylanilino)phenyl]benzene-1,4-diamine Chemical compound C1=CC=CC=C1N(C=1C=CC(=CC=1)N(C=1C=CC(=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C=1C=CC(=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 IYZMXHQDXZKNCY-UHFFFAOYSA-N 0.000 description 1
- ZNZCBZJTANSNGL-UHFFFAOYSA-N 1-n,2-n-diphenylbenzene-1,2-diamine Chemical compound C=1C=CC=C(NC=2C=CC=CC=2)C=1NC1=CC=CC=C1 ZNZCBZJTANSNGL-UHFFFAOYSA-N 0.000 description 1
- STTGYIUESPWXOW-UHFFFAOYSA-N 2,9-dimethyl-4,7-diphenyl-1,10-phenanthroline Chemical compound C=12C=CC3=C(C=4C=CC=CC=4)C=C(C)N=C3C2=NC(C)=CC=1C1=CC=CC=C1 STTGYIUESPWXOW-UHFFFAOYSA-N 0.000 description 1
- NRSBAUDUBWMTGL-UHFFFAOYSA-N 2-(1-benzothiophen-2-yl)pyridine Chemical compound S1C2=CC=CC=C2C=C1C1=CC=CC=N1 NRSBAUDUBWMTGL-UHFFFAOYSA-N 0.000 description 1
- BWLBGMIXKSTLSX-UHFFFAOYSA-N 2-hydroxyisobutyric acid Chemical compound CC(C)(O)C(O)=O BWLBGMIXKSTLSX-UHFFFAOYSA-N 0.000 description 1
- KAJMDIRNTNSOLE-UHFFFAOYSA-N 2-naphthalen-1-yl-1,3-benzoxazole Chemical compound C1=CC=C2C(C=3OC4=CC=CC=C4N=3)=CC=CC2=C1 KAJMDIRNTNSOLE-UHFFFAOYSA-N 0.000 description 1
- XBHOUXSGHYZCNH-UHFFFAOYSA-N 2-phenyl-1,3-benzothiazole Chemical compound C1=CC=CC=C1C1=NC2=CC=CC=C2S1 XBHOUXSGHYZCNH-UHFFFAOYSA-N 0.000 description 1
- FIISKTXZUZBTRC-UHFFFAOYSA-N 2-phenyl-1,3-benzoxazole Chemical compound C1=CC=CC=C1C1=NC2=CC=CC=C2O1 FIISKTXZUZBTRC-UHFFFAOYSA-N 0.000 description 1
- QLPKTAFPRRIFQX-UHFFFAOYSA-N 2-thiophen-2-ylpyridine Chemical compound C1=CSC(C=2N=CC=CC=2)=C1 QLPKTAFPRRIFQX-UHFFFAOYSA-N 0.000 description 1
- VJHVLELNDFVKMS-UHFFFAOYSA-N 3-methoxy-2-phenylpyridine Chemical compound COC1=CC=CN=C1C1=CC=CC=C1 VJHVLELNDFVKMS-UHFFFAOYSA-N 0.000 description 1
- OGGKVJMNFFSDEV-UHFFFAOYSA-N 3-methyl-n-[4-[4-(n-(3-methylphenyl)anilino)phenyl]phenyl]-n-phenylaniline Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 OGGKVJMNFFSDEV-UHFFFAOYSA-N 0.000 description 1
- IBOFVQJTBBUKMU-UHFFFAOYSA-N 4,4'-methylene-bis-(2-chloroaniline) Chemical compound C1=C(Cl)C(N)=CC=C1CC1=CC=C(N)C(Cl)=C1 IBOFVQJTBBUKMU-UHFFFAOYSA-N 0.000 description 1
- YGBCLRRWZQSURU-UHFFFAOYSA-N 4-[(diphenylhydrazinylidene)methyl]-n,n-diethylaniline Chemical compound C1=CC(N(CC)CC)=CC=C1C=NN(C=1C=CC=CC=1)C1=CC=CC=C1 YGBCLRRWZQSURU-UHFFFAOYSA-N 0.000 description 1
- KBXXZTIBAVBLPP-UHFFFAOYSA-N 4-[[4-(diethylamino)-2-methylphenyl]-(4-methylphenyl)methyl]-n,n-diethyl-3-methylaniline Chemical compound CC1=CC(N(CC)CC)=CC=C1C(C=1C(=CC(=CC=1)N(CC)CC)C)C1=CC=C(C)C=C1 KBXXZTIBAVBLPP-UHFFFAOYSA-N 0.000 description 1
- 125000004860 4-ethylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])C([H])([H])[H] 0.000 description 1
- ZOKIJILZFXPFTO-UHFFFAOYSA-N 4-methyl-n-[4-[1-[4-(4-methyl-n-(4-methylphenyl)anilino)phenyl]cyclohexyl]phenyl]-n-(4-methylphenyl)aniline Chemical compound C1=CC(C)=CC=C1N(C=1C=CC(=CC=1)C1(CCCCC1)C=1C=CC(=CC=1)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)C1=CC=C(C)C=C1 ZOKIJILZFXPFTO-UHFFFAOYSA-N 0.000 description 1
- UHBIKXOBLZWFKM-UHFFFAOYSA-N 8-hydroxy-2-quinolinecarboxylic acid Chemical compound C1=CC=C(O)C2=NC(C(=O)O)=CC=C21 UHBIKXOBLZWFKM-UHFFFAOYSA-N 0.000 description 1
- SFBHJDZYFDQEEY-UHFFFAOYSA-N 9-cyclobutylcarbazole Chemical compound C1CCC1N1C2=CC=CC=C2C2=CC=CC=C21 SFBHJDZYFDQEEY-UHFFFAOYSA-N 0.000 description 1
- 244000198134 Agave sisalana Species 0.000 description 1
- 101150019028 Antp gene Proteins 0.000 description 1
- DJHGAFSJWGLOIV-UHFFFAOYSA-K Arsenate3- Chemical class [O-][As]([O-])([O-])=O DJHGAFSJWGLOIV-UHFFFAOYSA-K 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 244000025254 Cannabis sativa Species 0.000 description 1
- 235000012766 Cannabis sativa ssp. sativa var. sativa Nutrition 0.000 description 1
- 235000012765 Cannabis sativa ssp. sativa var. spontanea Nutrition 0.000 description 1
- 102100024133 Coiled-coil domain-containing protein 50 Human genes 0.000 description 1
- 240000000491 Corchorus aestuans Species 0.000 description 1
- 235000011777 Corchorus aestuans Nutrition 0.000 description 1
- 235000010862 Corchorus capsularis Nutrition 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 1
- BDAGIHXWWSANSR-UHFFFAOYSA-M Formate Chemical compound [O-]C=O BDAGIHXWWSANSR-UHFFFAOYSA-M 0.000 description 1
- 101000910772 Homo sapiens Coiled-coil domain-containing protein 50 Proteins 0.000 description 1
- RAXXELZNTBOGNW-UHFFFAOYSA-O Imidazolium Chemical compound C1=C[NH+]=CN1 RAXXELZNTBOGNW-UHFFFAOYSA-O 0.000 description 1
- 240000006240 Linum usitatissimum Species 0.000 description 1
- 235000004431 Linum usitatissimum Nutrition 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229920000877 Melamine resin Polymers 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 101100518501 Mus musculus Spp1 gene Proteins 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- 229910020808 NaBF Inorganic materials 0.000 description 1
- 101100326803 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) fac-2 gene Proteins 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- CBENFWSGALASAD-UHFFFAOYSA-N Ozone Chemical compound [O-][O+]=O CBENFWSGALASAD-UHFFFAOYSA-N 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- YNPNZTXNASCQKK-UHFFFAOYSA-N Phenanthrene Natural products C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 1
- 229920002845 Poly(methacrylic acid) Polymers 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 239000005062 Polybutadiene Substances 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004642 Polyimide Substances 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 229910052772 Samarium Inorganic materials 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 229910052768 actinide Inorganic materials 0.000 description 1
- 150000001255 actinides Chemical class 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 239000012491 analyte Substances 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- 150000003851 azoles Chemical class 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- QJXVCEINEQQSPK-UHFFFAOYSA-N bis(2-methylphenyl)-diphenylsilane Chemical compound CC1=CC=CC=C1[Si](C=1C(=CC=CC=1)C)(C=1C=CC=CC=1)C1=CC=CC=C1 QJXVCEINEQQSPK-UHFFFAOYSA-N 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- XZCJVWCMJYNSQO-UHFFFAOYSA-N butyl pbd Chemical compound C1=CC(C(C)(C)C)=CC=C1C1=NN=C(C=2C=CC(=CC=2)C=2C=CC=CC=2)O1 XZCJVWCMJYNSQO-UHFFFAOYSA-N 0.000 description 1
- 235000009120 camo Nutrition 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 235000005607 chanvre indien Nutrition 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- PBAYDYUZOSNJGU-UHFFFAOYSA-N chelidonic acid Natural products OC(=O)C1=CC(=O)C=C(C(O)=O)O1 PBAYDYUZOSNJGU-UHFFFAOYSA-N 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 150000008280 chlorinated hydrocarbons Chemical class 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 239000012459 cleaning agent Substances 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 229920001940 conductive polymer Polymers 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000012084 conversion product Substances 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 125000000058 cyclopentadienyl group Chemical group C1(=CC=CC1)* 0.000 description 1
- 229940043397 deconex Drugs 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 125000001664 diethylamino group Chemical group [H]C([H])([H])C([H])([H])N(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 238000000840 electrochemical analysis Methods 0.000 description 1
- 238000001194 electroluminescence spectrum Methods 0.000 description 1
- 230000005670 electromagnetic radiation Effects 0.000 description 1
- ZSWFCLXCOIISFI-UHFFFAOYSA-N endo-cyclopentadiene Natural products C1C=CC=C1 ZSWFCLXCOIISFI-UHFFFAOYSA-N 0.000 description 1
- 238000000407 epitaxy Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 239000002657 fibrous material Substances 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 238000005194 fractionation Methods 0.000 description 1
- 150000002240 furans Chemical class 0.000 description 1
- JVZRCNQLWOELDU-UHFFFAOYSA-N gamma-Phenylpyridine Natural products C1=CC=CC=C1C1=CC=NC=C1 JVZRCNQLWOELDU-UHFFFAOYSA-N 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229940015043 glyoxal Drugs 0.000 description 1
- 210000004209 hair Anatomy 0.000 description 1
- 150000002367 halogens Chemical group 0.000 description 1
- 239000011487 hemp Substances 0.000 description 1
- 150000002390 heteroarenes Chemical class 0.000 description 1
- 125000004447 heteroarylalkenyl group Chemical group 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 239000012456 homogeneous solution Substances 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 238000003018 immunoassay Methods 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 239000013067 intermediate product Substances 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 150000002503 iridium Chemical class 0.000 description 1
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 1
- UEEXRMUCXBPYOV-UHFFFAOYSA-N iridium;2-phenylpyridine Chemical compound [Ir].C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1 UEEXRMUCXBPYOV-UHFFFAOYSA-N 0.000 description 1
- 229910052747 lanthanoid Inorganic materials 0.000 description 1
- 150000002602 lanthanoids Chemical class 0.000 description 1
- 239000010985 leather Substances 0.000 description 1
- 238000012698 light-induced step-growth polymerization Methods 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- 238000000504 luminescence detection Methods 0.000 description 1
- 125000000040 m-tolyl group Chemical group [H]C1=C([H])C(*)=C([H])C(=C1[H])C([H])([H])[H] 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 229910001092 metal group alloy Inorganic materials 0.000 description 1
- 150000004702 methyl esters Chemical class 0.000 description 1
- 229910003455 mixed metal oxide Inorganic materials 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 239000012452 mother liquor Substances 0.000 description 1
- PADPKJACPLYMPK-UHFFFAOYSA-N n',n'-diphenylethane-1,2-diamine Chemical compound C=1C=CC=CC=1N(CCN)C1=CC=CC=C1 PADPKJACPLYMPK-UHFFFAOYSA-N 0.000 description 1
- JGOAZQAXRONCCI-SDNWHVSQSA-N n-[(e)-benzylideneamino]aniline Chemical compound C=1C=CC=CC=1N\N=C\C1=CC=CC=C1 JGOAZQAXRONCCI-SDNWHVSQSA-N 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- GKTNLYAAZKKMTQ-UHFFFAOYSA-N n-[bis(dimethylamino)phosphinimyl]-n-methylmethanamine Chemical compound CN(C)P(=N)(N(C)C)N(C)C GKTNLYAAZKKMTQ-UHFFFAOYSA-N 0.000 description 1
- XTBLDMQMUSHDEN-UHFFFAOYSA-N naphthalene-2,3-diamine Chemical compound C1=CC=C2C=C(N)C(N)=CC2=C1 XTBLDMQMUSHDEN-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 230000003472 neutralizing effect Effects 0.000 description 1
- 229910052755 nonmetal Inorganic materials 0.000 description 1
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 1
- 150000002902 organometallic compounds Chemical class 0.000 description 1
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 description 1
- 150000002905 orthoesters Chemical class 0.000 description 1
- 150000002908 osmium compounds Chemical class 0.000 description 1
- 125000001037 p-tolyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 1
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 1
- 125000001792 phenanthrenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C=CC12)* 0.000 description 1
- 229920002239 polyacrylonitrile Polymers 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920002480 polybenzimidazole Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920000570 polyether Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920001721 polyimide Polymers 0.000 description 1
- 229920006254 polymer film Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 229920002689 polyvinyl acetate Polymers 0.000 description 1
- 239000011118 polyvinyl acetate Substances 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 239000000700 radioactive tracer Substances 0.000 description 1
- 229910052761 rare earth metal Inorganic materials 0.000 description 1
- 150000002910 rare earth metals Chemical class 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 238000004064 recycling Methods 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 238000000518 rheometry Methods 0.000 description 1
- 150000003303 ruthenium Chemical class 0.000 description 1
- KZUNJOHGWZRPMI-UHFFFAOYSA-N samarium atom Chemical compound [Sm] KZUNJOHGWZRPMI-UHFFFAOYSA-N 0.000 description 1
- 238000011896 sensitive detection Methods 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 1
- 238000010129 solution processing Methods 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- 238000009987 spinning Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000010902 straw Substances 0.000 description 1
- 125000005504 styryl group Chemical group 0.000 description 1
- 150000003513 tertiary aromatic amines Chemical class 0.000 description 1
- 238000004154 testing of material Methods 0.000 description 1
- RAOIDOHSFRTOEL-UHFFFAOYSA-N tetrahydrothiophene Chemical compound C1CCSC1 RAOIDOHSFRTOEL-UHFFFAOYSA-N 0.000 description 1
- 238000002230 thermal chemical vapour deposition Methods 0.000 description 1
- 238000002207 thermal evaporation Methods 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- 239000010981 turquoise Substances 0.000 description 1
- 238000002604 ultrasonography Methods 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- 239000000984 vat dye Substances 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 239000002023 wood Substances 0.000 description 1
- 210000002268 wool Anatomy 0.000 description 1
- 238000012982 x-ray structure analysis Methods 0.000 description 1
- 229910052727 yttrium Inorganic materials 0.000 description 1
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/22—Organic complexes
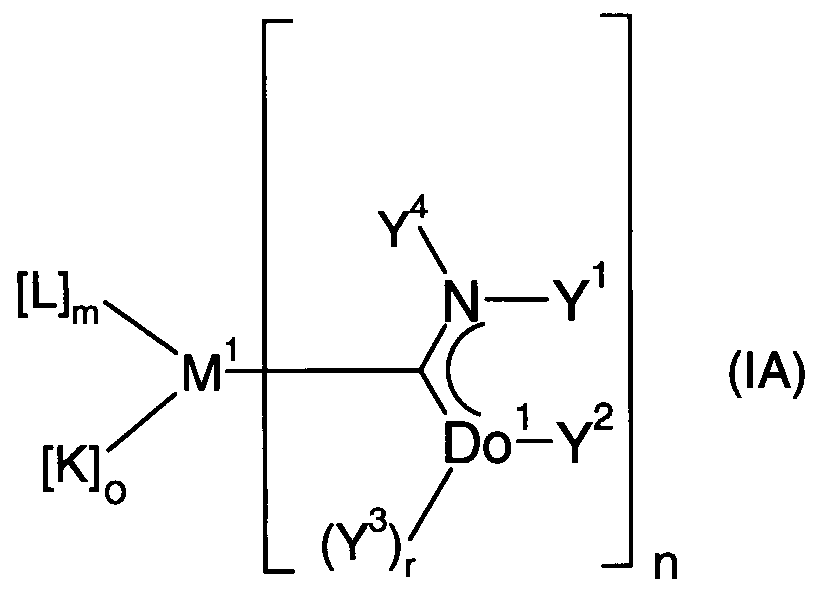
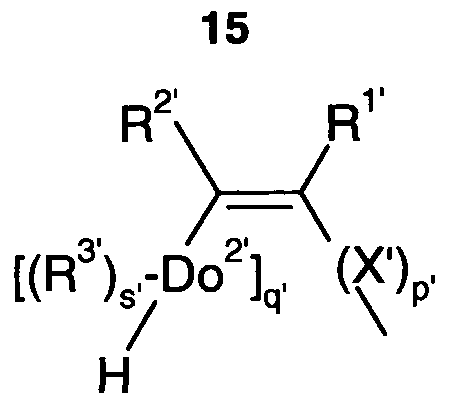
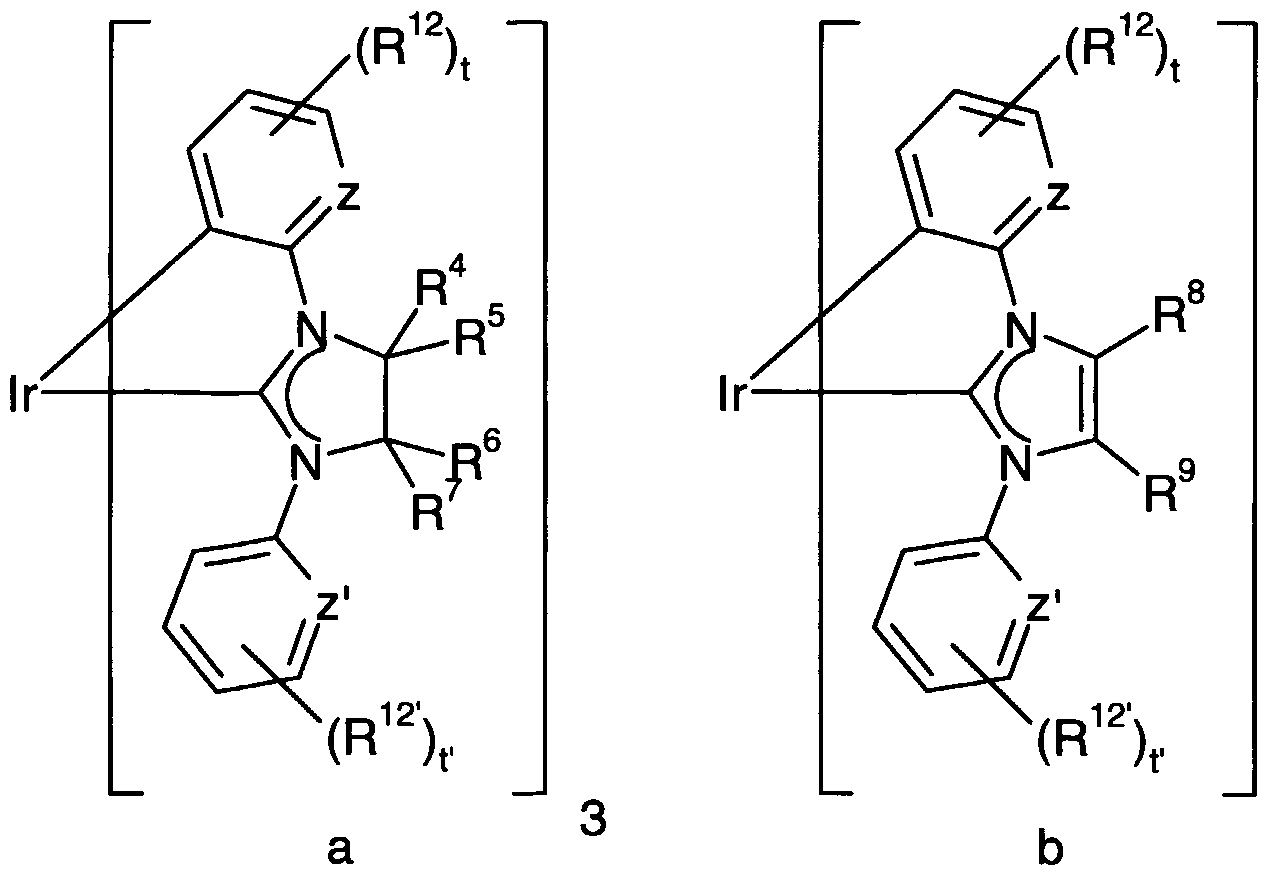
- B01J31/2265—Carbenes or carbynes, i.e.(image)
- B01J31/2269—Heterocyclic carbenes
- B01J31/2273—Heterocyclic carbenes with only nitrogen as heteroatomic ring members, e.g. 1,3-diarylimidazoline-2-ylidenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System compounds of the platinum group
- C07F15/0033—Iridium compounds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
- C09B57/10—Metal complexes of organic compounds not being dyes in uncomplexed form
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/10—Complexes comprising metals of Group I (IA or IB) as the central metal
- B01J2531/16—Copper
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/10—Complexes comprising metals of Group I (IA or IB) as the central metal
- B01J2531/17—Silver
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/10—Complexes comprising metals of Group I (IA or IB) as the central metal
- B01J2531/18—Gold
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/50—Complexes comprising metals of Group V (VA or VB) as the central metal
- B01J2531/57—Niobium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/60—Complexes comprising metals of Group VI (VIA or VIB) as the central metal
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/70—Complexes comprising metals of Group VII (VIIB) as the central metal
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/80—Complexes comprising metals of Group VIII as the central metal
- B01J2531/82—Metals of the platinum group
- B01J2531/821—Ruthenium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/80—Complexes comprising metals of Group VIII as the central metal
- B01J2531/82—Metals of the platinum group
- B01J2531/822—Rhodium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/80—Complexes comprising metals of Group VIII as the central metal
- B01J2531/82—Metals of the platinum group
- B01J2531/827—Iridium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/80—Complexes comprising metals of Group VIII as the central metal
- B01J2531/82—Metals of the platinum group
- B01J2531/828—Platinum
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/22—Organic complexes
- B01J31/2265—Carbenes or carbynes, i.e.(image)
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1059—Heterocyclic compounds characterised by ligands containing three nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/18—Metal complexes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/18—Metal complexes
- C09K2211/185—Metal complexes of the platinum group, i.e. Os, Ir, Pt, Ru, Rh or Pd
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/18—Carrier blocking layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/18—Carrier blocking layers
- H10K50/181—Electron blocking layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/321—Metal complexes comprising a group IIIA element, e.g. Tris (8-hydroxyquinoline) gallium [Gaq3]
- H10K85/324—Metal complexes comprising a group IIIA element, e.g. Tris (8-hydroxyquinoline) gallium [Gaq3] comprising aluminium, e.g. Alq3
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/582—Recycling of unreacted starting or intermediate materials
Abstract
Description
Claims
Priority Applications (13)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10/568,344 US7846763B2 (en) | 2003-08-19 | 2004-08-18 | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (OLED's) |
| KR1020067003352A KR101186706B1 (ko) | 2003-08-19 | 2004-08-18 | 유기 발광 다이오드용 이미터로서 작용하는 카르빈리간드를 함유하는 전이 금속 착체 |
| JP2006523602A JP4351702B2 (ja) | 2003-08-19 | 2004-08-18 | 有機発光ダイオード用の発光体としてカルベンリガンドを有する遷移金属錯体 |
| EP17191410.4A EP3299437B1 (de) | 2003-08-19 | 2004-08-18 | Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) |
| EP20191338.1A EP3805338A1 (de) | 2003-08-19 | 2004-08-18 | Übergangsmetallkomplexe mit carbenliganden als emitter für organische lichtemittierende dioden (oleds) |
| EP04764255.8A EP1658349B1 (de) | 2003-08-19 | 2004-08-18 | VERWENDUNG VON ÜBERGANGSMETALLKOMPLEXEN MIT CARBENLIGANDEN ALS EMITTER FÜR ORGANISCHE LICHT-EMITTIERENDE DIODEN (OLEDs) UND OLEDs |
| US12/901,610 US9748498B2 (en) | 2003-08-19 | 2010-10-11 | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (OLED's) |
| US12/904,290 US8377740B2 (en) | 2003-08-19 | 2010-10-14 | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (OLED's) |
| US12/905,112 US8916853B2 (en) | 2003-08-19 | 2010-10-15 | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (OLED's) |
| US14/540,838 US9024308B2 (en) | 2003-08-19 | 2014-11-13 | Transition metal complexes with carbene ligands as emitters for organic light-emitting diodes (OLEDs) |
| US15/663,900 US10573828B2 (en) | 2003-08-19 | 2017-07-31 | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (OLED's) |
| US16/798,526 US11539005B2 (en) | 2003-08-19 | 2020-02-24 | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (OLED's) |
| US18/061,111 US20230108701A1 (en) | 2003-08-19 | 2022-12-02 | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (oled's) |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10338550A DE10338550A1 (de) | 2003-08-19 | 2003-08-19 | Übergangsmetallkomplexe mit Carbenliganden als Emitter für organische Licht-emittierende Dioden (OLEDs) |
| DE10338550.9 | 2003-08-19 |
Related Child Applications (5)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US10/568,344 A-371-Of-International US7846763B2 (en) | 2003-08-19 | 2004-08-18 | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (OLED's) |
| US10568344 A-371-Of-International | 2004-08-18 | ||
| US12/901,610 Division US9748498B2 (en) | 2003-08-19 | 2010-10-11 | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (OLED's) |
| US12/904,290 Division US8377740B2 (en) | 2003-08-19 | 2010-10-14 | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (OLED's) |
| US12/905,112 Division US8916853B2 (en) | 2003-08-19 | 2010-10-15 | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (OLED's) |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| WO2005019373A2 true WO2005019373A2 (de) | 2005-03-03 |
| WO2005019373A3 WO2005019373A3 (de) | 2005-05-19 |
Family
ID=34201819
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2004/009269 WO2005019373A2 (de) | 2003-08-19 | 2004-08-18 | Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) |
Country Status (7)
| Country | Link |
|---|---|
| US (8) | US7846763B2 (de) |
| EP (3) | EP3805338A1 (de) |
| JP (1) | JP4351702B2 (de) |
| KR (1) | KR101186706B1 (de) |
| CN (2) | CN100573961C (de) |
| DE (1) | DE10338550A1 (de) |
| WO (1) | WO2005019373A2 (de) |
Cited By (963)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006018292A2 (de) * | 2004-08-18 | 2006-02-23 | Basf Aktiengesellschaft | In polymermatrices eingebettete übergansmetallcarbenkomplexe zur verwendung in oleds |
| WO2006056418A2 (de) * | 2004-11-25 | 2006-06-01 | Basf Aktiengesellschaft | Verwendung von übergangsmetall-carbenkomplexen in organischen licht-emittierenden dioden (oleds) |
| WO2006067074A1 (en) * | 2004-12-23 | 2006-06-29 | Ciba Specialty Chemicals Holding Inc. | Electroluminescent metal complexes with nucleophilic carbene ligands |
| WO2006106842A1 (ja) * | 2005-03-31 | 2006-10-12 | Idemitsu Kosan Co., Ltd. | 遷移金属錯体化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2006134113A1 (de) * | 2005-06-14 | 2006-12-21 | Basf Aktiengesellschaft | Verfahren zur isomerisierung cyclometallierter, carbenliganden enthaltender übergangsmetallkomplexe |
| WO2007018067A1 (ja) * | 2005-08-05 | 2007-02-15 | Idemitsu Kosan Co., Ltd. | 遷移金属錯体化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP2007045742A (ja) * | 2005-08-10 | 2007-02-22 | Mitsubishi Chemicals Corp | 遷移金属錯体の製造方法及び遷移金属錯体 |
| WO2007029426A1 (ja) | 2005-09-05 | 2007-03-15 | Idemitsu Kosan Co., Ltd. | 青色発光有機エレクトロルミネッセンス素子 |
| JP2007096259A (ja) * | 2005-04-25 | 2007-04-12 | Fujifilm Corp | 有機電界発光素子 |
| WO2007058104A1 (ja) * | 2005-11-17 | 2007-05-24 | Idemitsu Kosan Co., Ltd. | 金属錯体化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2007058255A1 (ja) * | 2005-11-17 | 2007-05-24 | Idemitsu Kosan Co., Ltd. | 遷移金属錯体化合物 |
| WO2007069539A1 (ja) * | 2005-12-15 | 2007-06-21 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子、表示装置および照明装置 |
| WO2008000727A1 (de) * | 2006-06-26 | 2008-01-03 | Basf Se | Verwendung von übergangsmetallcarbenkomplexen, die keine cyclometallierung über nicht-carbene enthalten, in oleds |
| WO2008031743A1 (en) | 2006-09-14 | 2008-03-20 | Ciba Holding Inc. | Heterocyclic bridged biphenyls and their use in oleds |
| WO2008034758A2 (de) * | 2006-09-21 | 2008-03-27 | Basf Se | Oled-anzeige mit verlängerter lebensdauer |
| CN100390185C (zh) * | 2005-05-11 | 2008-05-28 | 友达光电股份有限公司 | 发光材料及应用其的有机电激发光器件 |
| WO2008096609A1 (ja) * | 2007-02-05 | 2008-08-14 | Idemitsu Kosan Co., Ltd. | 遷移金属錯体化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2008108430A1 (ja) | 2007-03-07 | 2008-09-12 | Mitsubishi Chemical Corporation | 有機デバイス用組成物、高分子膜および有機電界発光素子 |
| EP1995292A1 (de) | 2007-05-18 | 2008-11-26 | FUJIFILM Corporation | Organische elektrolumineszente Vorrichtung |
| WO2009003898A1 (de) * | 2007-07-05 | 2009-01-08 | Basf Se | Organische leuchtdioden enthaltend carben-übergangsmetall-komplex-emitter und mindestens eine verbindung ausgewählt aus disilylcarbazolen; disilyldibenzofuranen, disilyldibenzothiophenen, disilyldibenzophospholen, disilyldibenzothiophen-s-oxiden und disilyldibenzothiophen-s,s-dioxiden |
| CN100465168C (zh) * | 2006-09-15 | 2009-03-04 | 华东理工大学 | 噁二唑衍生物及其在电致发光材料中应用 |
| EP2031037A1 (de) | 2007-08-29 | 2009-03-04 | Fujifilm Corporation | Organische Elektrolumineszenzvorrichtung |
| EP2036907A1 (de) | 2007-09-14 | 2009-03-18 | FUJIFILM Corporation | Organische Elektrolumineszenzvorrichtung |
| JP2009057505A (ja) * | 2007-09-03 | 2009-03-19 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| WO2009037155A1 (en) | 2007-09-20 | 2009-03-26 | Basf Se | Electroluminescent device |
| EP2042508A1 (de) | 2007-09-25 | 2009-04-01 | FUJIFILM Corporation | Organische Elektrolumineszenzvorrichtung |
| DE102007046445A1 (de) | 2007-09-28 | 2009-04-16 | Osram Opto Semiconductors Gmbh | Organisches selbstemittierendes Bauteil |
| JPWO2007060826A1 (ja) * | 2005-11-24 | 2009-05-07 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| EP2061087A2 (de) | 2007-11-15 | 2009-05-20 | FUJIFILM Corporation | Dünnschicht-Feldeffekttransistor und Anzeige unter Benutzung desselben |
| EP2061086A2 (de) | 2007-11-15 | 2009-05-20 | FUJIFILM Corporation | Dünnschicht-Feldeffekttransistor und Anzeige unter Benutzung desselben |
| EP2070936A1 (de) | 2007-12-14 | 2009-06-17 | Fujifilm Corporation | Platinkomplexverbindungen und organische Elektrolumineszenzvorrichtung dafür |
| WO2009100991A1 (en) | 2008-02-12 | 2009-08-20 | Basf Se | Electroluminescent metal complexes with dibenzo[f,h]quinoxalines |
| EP2096690A2 (de) | 2008-02-28 | 2009-09-02 | FUJIFILM Corporation | Organische Elektrolumineszenzvorrichtung |
| JP2009532431A (ja) * | 2006-04-05 | 2009-09-10 | ビーエーエスエフ ソシエタス・ヨーロピア | ヘテロレプティックな遷移金属−カルベン錯体及びそれを有機発光ダイオード(oled)において用いる使用 |
| EP2105967A1 (de) | 2008-03-24 | 2009-09-30 | FUJIFILM Corporation | Dünnschicht-Feldeffekttransistor und Anzeige |
| EP2112213A2 (de) | 2008-04-22 | 2009-10-28 | FUJIFILM Corporation | Organische Elektrolumineszenzvorrichtung, neue Platinkomplexverbindung und neue Verbindung, die als Ligand dafür geeignet ist |
| EP2113548A1 (de) | 2008-04-24 | 2009-11-04 | FUJIFILM Corporation | Organische Elektrolumineszenzvorrichtung |
| JP2009542026A (ja) * | 2006-06-26 | 2009-11-26 | ビーエーエスエフ ソシエタス・ヨーロピア | 架橋カルベン配位子を有するPtとPdのビスカルベン錯体及びテトラカルベン錯体のOLED内での利用 |
| WO2009147237A1 (en) | 2008-06-06 | 2009-12-10 | Basf Se | Chlorinated naphthalenetetracarboxylic acid derivatives, preparation thereof and use thereof in organic electronics |
| DE102008033929A1 (de) | 2008-07-18 | 2010-01-21 | Siemens Aktiengesellschaft | Phosphoreszente Metallkomplexverbindung, Verfahren zur Herstellung dazu und strahlungsemittierendes Bauelement |
| DE102008056688A1 (de) | 2008-11-11 | 2010-05-12 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2010083871A1 (de) | 2009-01-20 | 2010-07-29 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| EP2214223A2 (de) | 2009-02-03 | 2010-08-04 | Fujifilm Corporation | Organische Elektrolumineszenzanzeigevorrichtung |
| WO2010093062A1 (en) | 2009-02-13 | 2010-08-19 | Fujifilm Corporation | Organic electroluminescence device, and method for producing the same |
| WO2010097433A1 (de) | 2009-02-26 | 2010-09-02 | Basf Se | Chinonverbindungen als dotierstoff in der organischen elektronik |
| EP2226867A2 (de) | 2009-03-05 | 2010-09-08 | Fujifilm Corporation | Organische Elektrolumineszenzvorrichtung |
| WO2010101011A1 (en) | 2009-03-03 | 2010-09-10 | Fujifilm Corporation | Method for producing light-emitting display device, light-emitting display device and light-emitting display |
| DE102009031021A1 (de) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011006574A1 (de) | 2009-07-14 | 2011-01-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2011013626A1 (ja) | 2009-07-31 | 2011-02-03 | 富士フイルム株式会社 | 有機デバイス用蒸着材料及び有機デバイスの製造方法 |
| WO2011024922A1 (ja) | 2009-08-27 | 2011-03-03 | 三菱化学株式会社 | モノアミン化合物、電荷輸送材料、電荷輸送膜用組成物、有機電界発光素子、有機el表示装置及び有機el照明 |
| WO2011024976A1 (ja) | 2009-08-31 | 2011-03-03 | 富士フイルム株式会社 | 有機電界発光素子 |
| WO2011030882A1 (en) | 2009-09-14 | 2011-03-17 | Fujifilm Corporation | Color filter and light-emitting display element |
| WO2011030620A1 (en) | 2009-09-09 | 2011-03-17 | Fujifilm Corporation | Organic el device optical member and organic el device |
| WO2011030883A1 (en) | 2009-09-14 | 2011-03-17 | Fujifilm Corporation | Color filter and light-emitting display element |
| DE102009031683A1 (de) | 2009-07-03 | 2011-03-24 | Siemens Aktiengesellschaft | Phophoreszente Metallkomplexverbindung, Verfahren zur Herstellung dazu und strahlungsemittierendes Bauelement |
| WO2011042107A2 (de) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2011051404A1 (de) | 2009-10-28 | 2011-05-05 | Basf Se | Heteroleptische carben-komplexe und deren verwendung in der organischen elektronik |
| DE102009052428A1 (de) | 2009-11-10 | 2011-05-12 | Merck Patent Gmbh | Verbindung für elektronische Vorrichtungen |
| DE102009053382A1 (de) | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009053644A1 (de) | 2009-11-17 | 2011-05-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011063083A1 (en) | 2009-11-19 | 2011-05-26 | The University Of Southern California | 3-coordinate copper (i) - carbene complexes |
| WO2011060867A1 (de) | 2009-11-18 | 2011-05-26 | Merck Patent Gmbh | Stickstoffhaltige kondensierte heterozyklen für oleds |
| WO2011073149A1 (de) | 2009-12-14 | 2011-06-23 | Basf Se | Metallkomplexe, enthaltend diazabenzimidazolcarben-liganden und deren verwendung in oleds |
| EP2338593A1 (de) | 2006-01-31 | 2011-06-29 | Basf Se | Verfahren zur Herstellung von Übergangsmetall-Carbenkomplexen |
| DE102010004803A1 (de) | 2010-01-16 | 2011-07-21 | Merck Patent GmbH, 64293 | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011088877A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2011088918A1 (de) | 2010-01-25 | 2011-07-28 | Siemens Aktiengesellschaft | Verwendung des guanidinium-kations in einem lichtemittierenden bauelement |
| DE102010005632A1 (de) | 2010-01-25 | 2011-07-28 | Siemens Aktiengesellschaft, 80333 | Phosphoreszente Metallkomplexverbindung, Verfahren zur Herstellung und lichtemittierendes Bauelement |
| DE102010009903A1 (de) | 2010-03-02 | 2011-09-08 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| WO2011115075A1 (ja) | 2010-03-15 | 2011-09-22 | 三菱化学株式会社 | 有機電界発光素子及びその製造方法、有機el表示装置、有機el照明、並びに有機電界発光素子の製造装置 |
| WO2011116865A1 (de) | 2010-03-25 | 2011-09-29 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102010013068A1 (de) | 2010-03-26 | 2011-09-29 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| WO2011126095A1 (ja) | 2010-04-09 | 2011-10-13 | 三菱化学株式会社 | 有機電界発光素子用組成物の製造方法、有機電界発光素子用組成物、有機電界発光素子の製造方法、有機電界発光素子、有機el表示装置および有機el照明 |
| DE102010014933A1 (de) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102010018321A1 (de) | 2010-04-27 | 2011-10-27 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| US8048538B2 (en) * | 2005-04-25 | 2011-11-01 | Fujifilm Corporation | Organic electroluminescent device |
| DE102010019306A1 (de) | 2010-05-04 | 2011-11-10 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| US8067100B2 (en) * | 2007-10-04 | 2011-11-29 | Universal Display Corporation | Complexes with tridentate ligands |
| DE102009022858A1 (de) | 2009-05-27 | 2011-12-15 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| JP2011256191A (ja) * | 2005-08-01 | 2011-12-22 | Mitsubishi Chemicals Corp | 遷移金属錯体の製造方法 |
| WO2011157346A1 (de) | 2010-06-18 | 2011-12-22 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2011157779A1 (en) | 2010-06-18 | 2011-12-22 | Basf Se | Organic electronic devices comprising a layer of a pyridine compound and a 8-hydroxyquinolinolato earth alkaline metal, or alkali metal complex |
| DE102010024542A1 (de) | 2010-06-22 | 2011-12-22 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| WO2011157790A1 (en) | 2010-06-18 | 2011-12-22 | Basf Se | Organic electronic devices comprising a layer of a dibenzofurane compound and a 8-hydroxyquinolinolato earth alkaline metal, or alkali metal complex |
| DE102010024897A1 (de) | 2010-06-24 | 2011-12-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2012005329A1 (ja) | 2010-07-08 | 2012-01-12 | 三菱化学株式会社 | 有機電界発光素子、有機電界発光デバイス、有機el表示装置及び有機el照明 |
| WO2012016630A1 (de) | 2010-08-05 | 2012-02-09 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| DE102010045405A1 (de) | 2010-09-15 | 2012-03-15 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2012041851A1 (en) | 2010-09-29 | 2012-04-05 | Basf Se | Security element |
| DE102010048074A1 (de) | 2010-10-09 | 2012-04-12 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| WO2012045710A1 (en) | 2010-10-07 | 2012-04-12 | Basf Se | Phenanthro[9,10-b]furans for electronic applications |
| WO2012048780A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102010048608A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| CN102482574A (zh) * | 2009-06-18 | 2012-05-30 | 巴斯夫欧洲公司 | 用作场致发光器件的空穴传输材料的菲并唑化合物 |
| WO2012069121A1 (de) | 2010-11-24 | 2012-05-31 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2012074111A1 (ja) | 2010-12-02 | 2012-06-07 | 宇部興産株式会社 | 二核金属錯体、及びそれを用いた有機エレクトロルミネッセンス素子 |
| DE102010054316A1 (de) | 2010-12-13 | 2012-06-14 | Merck Patent Gmbh | Substituierte Tetraarylbenzole |
| WO2012080052A1 (en) | 2010-12-13 | 2012-06-21 | Basf Se | Bispyrimidines for electronic applications |
| WO2012096352A1 (ja) | 2011-01-14 | 2012-07-19 | 三菱化学株式会社 | 有機電界発光素子、有機電界発光素子用組成物、及び有機電界発光装置 |
| DE102012000064A1 (de) | 2011-01-21 | 2012-07-26 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| EP2482159A2 (de) | 2011-01-28 | 2012-08-01 | Honeywell International, Inc. | Verfahren und umkonfigurierbare System zur Optimierung der Leistung eines zustandsabhängigen Wartungssystems |
| WO2012107163A1 (de) | 2011-02-12 | 2012-08-16 | Merck Patent Gmbh | Substituierte dibenzonaphtacene |
| WO2012107158A1 (de) | 2011-02-10 | 2012-08-16 | Merck Patent Gmbh | 1,3 - dioxan-5-on-verbindungen |
| DE102011011539A1 (de) | 2011-02-17 | 2012-08-23 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| WO2012116240A1 (en) * | 2011-02-23 | 2012-08-30 | Universal Display Corporation | Ruthenium carbene complexes for oled material |
| US8258297B2 (en) | 2007-10-17 | 2012-09-04 | Basf Se | Transition metal complexes with bridged carbene ligands and use thereof in OLEDs |
| US8269317B2 (en) | 2010-11-11 | 2012-09-18 | Universal Display Corporation | Phosphorescent materials |
| WO2012130709A1 (en) | 2011-03-25 | 2012-10-04 | Basf Se | 4h-imidazo[1,2-a]imidazoles for electronic applications |
| WO2012139692A1 (de) | 2011-04-13 | 2012-10-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2012139693A1 (de) | 2011-04-13 | 2012-10-18 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012143079A1 (de) | 2011-04-18 | 2012-10-26 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012143080A2 (de) | 2011-04-18 | 2012-10-26 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2012149992A1 (de) | 2011-05-04 | 2012-11-08 | Merck Patent Gmbh | Vorrichtung zur aufbewahrung von frischwaren |
| WO2012150001A1 (de) | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012149999A1 (de) | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012163465A1 (de) | 2011-06-03 | 2012-12-06 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| US8362246B2 (en) | 2010-12-13 | 2013-01-29 | Basf Se | Bispyrimidines for electronic applications |
| US8367223B2 (en) | 2008-11-11 | 2013-02-05 | Universal Display Corporation | Heteroleptic phosphorescent emitters |
| WO2013017192A1 (de) | 2011-08-03 | 2013-02-07 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2013017189A1 (de) | 2011-07-29 | 2013-02-07 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| US8377332B2 (en) | 2008-06-10 | 2013-02-19 | Basf Se | Transition metal complexes and use thereof in organic light emitting diodes—III |
| US8383249B2 (en) * | 2007-10-04 | 2013-02-26 | Universal Display Corporation | Complexes with tridentate ligands |
| US8383828B2 (en) | 2006-04-04 | 2013-02-26 | Basf Aktiengesellschaft | Transition metal complexes comprising one noncarbene ligand and one or two carbene ligands and their use in OLEDs |
| US8384068B2 (en) | 2007-10-02 | 2013-02-26 | Basf Se | Use of acridine derivatives as matrix materials and/or electron blockers in OLEDs |
| WO2013041176A1 (de) | 2011-09-21 | 2013-03-28 | Merck Patent Gmbh | Carbazolderivate für organische elektrolumineszenzvorrichtungen |
| US8410270B2 (en) | 2008-06-10 | 2013-04-02 | Basf Se | Transition metal complexes and use thereof in organic light-emitting diodes V |
| US8409729B2 (en) | 2011-07-28 | 2013-04-02 | Universal Display Corporation | Host materials for phosphorescent OLEDs |
| US8415031B2 (en) | 2011-01-24 | 2013-04-09 | Universal Display Corporation | Electron transporting compounds |
| WO2013050862A1 (ja) | 2011-10-07 | 2013-04-11 | ユーディーシー アイルランド リミテッド | 有機電界発光素子及び該素子用発光材料並びに発光装置、表示装置及び照明装置 |
| DE102011116165A1 (de) | 2011-10-14 | 2013-04-18 | Merck Patent Gmbh | Benzodioxepin-3-on-Verbindungen |
| WO2013056776A1 (de) | 2011-10-20 | 2013-04-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2013060418A1 (en) | 2011-10-27 | 2013-05-02 | Merck Patent Gmbh | Materials for electronic devices |
| WO2013064206A1 (de) | 2011-11-01 | 2013-05-10 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2013064881A2 (ja) | 2011-11-02 | 2013-05-10 | ユーディーシー アイルランド リミテッド | 有機電界発光素子、有機電界発光素子用材料並びに該有機電界発光素子を用いた発光装置、表示装置及び照明装置 |
| US8440326B2 (en) | 2008-06-30 | 2013-05-14 | Universal Display Corporation | Hole transport materials containing triphenylene |
| WO2013069338A1 (ja) | 2011-11-11 | 2013-05-16 | 三菱化学株式会社 | 有機電界発光素子及び有機電界発光デバイス |
| WO2013068376A1 (en) | 2011-11-10 | 2013-05-16 | Basf Se | 4h-imidazo[1,2-a]imidazoles for electronic applications |
| WO2013080798A1 (ja) | 2011-11-30 | 2013-06-06 | 富士フイルム株式会社 | 光拡散性転写材料、光拡散層の形成方法、有機電界発光装置、及び有機電界発光装置の製造方法 |
| WO2013083216A1 (de) | 2011-11-17 | 2013-06-13 | Merck Patent Gmbh | Spiro -dihydroacridinderivate und ihre verwendung als materialien für organische elektrolumineszenzvorrichtungen |
| WO2013087142A1 (de) | 2011-12-12 | 2013-06-20 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102012022880A1 (de) | 2011-12-22 | 2013-06-27 | Merck Patent Gmbh | Elektronische Vorrichtungen enthaltend organische Schichten |
| WO2013104649A1 (en) | 2012-01-12 | 2013-07-18 | Basf Se | Metal complexes with dibenzo[f,h]quinoxalines |
| US8492006B2 (en) | 2011-02-24 | 2013-07-23 | Universal Display Corporation | Germanium-containing red emitter materials for organic light emitting diode |
| JP2013145811A (ja) * | 2012-01-13 | 2013-07-25 | Konica Minolta Inc | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| DE102013200942A1 (de) | 2012-01-23 | 2013-07-25 | Udc Ireland Ltd. | Organisches Elektrolumineszenz-Element, Ladungstransportmaterial für organisches Elektrolumineszenz-Element, und Licht-emittierende Vorrichtung, Anzeigevorrichtung und Beleuchtungsvorrichtung, die jeweils das Element verwenden |
| WO2013108069A2 (ja) | 2011-10-06 | 2013-07-25 | ユーディーシー アイルランド リミテッド | 有機電界発光素子とそれに用いることができる化合物および有機電界発光素子用材料、並びに該素子を用いた発光装置、表示装置及び照明装置 |
| WO2013108787A1 (ja) | 2012-01-17 | 2013-07-25 | 三菱化学株式会社 | 有機電界発光素子、有機el照明および有機el表示装置 |
| EP2623508A1 (de) | 2012-02-02 | 2013-08-07 | Konica Minolta Advanced Layers, Inc. | Iridiumkomplexverbindung, Material aus organischem elektrolumineszentem Material, organisches elektrolumineszentes Material, Beleuchtungsvorrichtung und Anzeigevorrichtung |
| DE102013201846A1 (de) | 2012-02-06 | 2013-08-14 | Udc Ireland Limited | Organisches Elektrolumineszenz-Element, Verbindung und Material für organisches Elektrolumineszenz-Element, die hier verrwendet werden können, Licht-emittierende Vorrichtung, Anzeigevorrichtung und Beleuchtungsvorrichtung, die jeweils das Element verwenden |
| WO2013120577A1 (en) | 2012-02-14 | 2013-08-22 | Merck Patent Gmbh | Spirobifluorene compounds for organic electroluminescent devices |
| WO2013135352A1 (de) | 2012-03-15 | 2013-09-19 | Merck Patent Gmbh | Elektronische vorrichtungen |
| WO2013139431A1 (de) | 2012-03-23 | 2013-09-26 | Merck Patent Gmbh | 9,9'-spirobixanthenderivate für elektrolumineszenzvorrichtungen |
| US8545996B2 (en) | 2009-11-02 | 2013-10-01 | The University Of Southern California | Ion-pairing soft salts based on organometallic complexes and their applications in organic light emitting diodes |
| US8563737B2 (en) | 2011-02-23 | 2013-10-22 | Universal Display Corporation | Methods of making bis-tridentate carbene complexes of ruthenium and osmium |
| WO2013176194A1 (ja) | 2012-05-24 | 2013-11-28 | 三菱化学株式会社 | 有機電界発光素子、有機電界発光照明装置及び有機電界発光表示装置 |
| DE102012011335A1 (de) | 2012-06-06 | 2013-12-12 | Merck Patent Gmbh | Verbindungen für Organische Elekronische Vorrichtungen |
| EP2677559A1 (de) | 2012-06-21 | 2013-12-25 | Konica Minolta, Inc. | Organisches elektrolumineszentes Element, Anzeigevorrichtung und Beleuchtungsvorrichtung |
| US8618533B2 (en) | 2008-10-07 | 2013-12-31 | Osram Opto Semiconductors Gmbh | Siloles substituted by fused ring systems and use thereof in organic electronics |
| WO2014008967A2 (de) | 2012-07-10 | 2014-01-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2014009317A1 (en) | 2012-07-10 | 2014-01-16 | Basf Se | Benzimidazo[1,2-a]benzimidazole derivatives for electronic applications |
| WO2014012972A1 (en) | 2012-07-19 | 2014-01-23 | Basf Se | Dinuclear metal complexes comprising carbene ligands and the use thereof in oleds |
| US8637857B2 (en) | 2010-04-06 | 2014-01-28 | Basf Se | Substituted carbazole derivatives and use thereof in organic electronics |
| WO2014015935A2 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Verbindungen und organische elektronische vorrichtungen |
| WO2014015938A1 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Derivate von 2-diarylaminofluoren und diese enthaltnde organische elektronische verbindungen |
| WO2014015937A1 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Verbindungen und organische elektrolumineszierende vorrichtungen |
| WO2014015931A1 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2014019711A1 (en) * | 2012-08-02 | 2014-02-06 | Roche Diagnostics Gmbh | New iridium-based complexes for ecl |
| WO2014023388A1 (de) | 2012-08-10 | 2014-02-13 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2014023377A2 (de) | 2012-08-07 | 2014-02-13 | Merck Patent Gmbh | Metallkomplexe |
| US8652656B2 (en) | 2011-11-14 | 2014-02-18 | Universal Display Corporation | Triphenylene silane hosts |
| US8659036B2 (en) | 2011-06-17 | 2014-02-25 | Universal Display Corporation | Fine tuning of emission spectra by combination of multiple emitter spectra |
| WO2014030666A1 (ja) | 2012-08-24 | 2014-02-27 | コニカミノルタ株式会社 | 透明電極、電子デバイス、および透明電極の製造方法 |
| WO2014044344A1 (de) | 2012-09-18 | 2014-03-27 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US8692241B1 (en) | 2012-11-08 | 2014-04-08 | Universal Display Corporation | Transition metal complexes containing triazole and tetrazole carbene ligands |
| US8691401B2 (en) | 2010-04-16 | 2014-04-08 | Basf Se | Bridged benzimidazole-carbene complexes and use thereof in OLEDS |
| WO2014054596A1 (ja) | 2012-10-02 | 2014-04-10 | 三菱化学株式会社 | 有機電界発光素子、有機el照明および有機el表示装置 |
| US8697255B2 (en) | 2007-07-05 | 2014-04-15 | Basf Se | Organic light-emitting diodes comprising at least one disilyl compound selected from disilylcarbazoles, disilyldibenzofurans, disilyldibenzothiophenes, disilyldibenzopholes, disilyldibenzothiophene S-oxides and disilyldibenzothiophene S,S-dioxides |
| WO2014056567A1 (de) | 2012-10-11 | 2014-04-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US8709615B2 (en) | 2011-07-28 | 2014-04-29 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US8716484B1 (en) | 2012-12-05 | 2014-05-06 | Universal Display Corporation | Hole transporting materials with twisted aryl groups |
| WO2014067614A1 (de) | 2012-10-31 | 2014-05-08 | Merck Patent Gmbh | Elektronische vorrichtung |
| US8723209B2 (en) | 2012-04-27 | 2014-05-13 | Universal Display Corporation | Out coupling layer containing particle polymer composite |
| WO2014072320A1 (en) | 2012-11-06 | 2014-05-15 | Basf Se | Phenoxasiline based compounds for electronic application |
| US8728632B2 (en) | 2007-10-17 | 2014-05-20 | Basf Se | Metal complexes comprising bridged carbene ligands and use thereof in OLEDs |
| US8734962B2 (en) | 2007-05-21 | 2014-05-27 | Osram Opto Semiconductors Gmbh | Phosphorescent metal complex compound radiation emitting component comprising a phosphorescent metal complex compound and method for production of a phosphorescent metal complex compound |
| WO2014079532A1 (de) | 2012-11-20 | 2014-05-30 | Merck Patent Gmbh | Formulierung in hochreinem l?sungsmittel zur herstellung elektronischer vorrichtungen |
| US8742657B2 (en) | 2010-06-11 | 2014-06-03 | Universal Display Corporation | Triplet-Triplet annihilation up conversion (TTA-UC) for display and lighting applications |
| WO2014082705A1 (de) | 2012-11-30 | 2014-06-05 | Merck Patent Gmbh | Elektronische vorrichtung |
| US8748012B2 (en) | 2011-05-25 | 2014-06-10 | Universal Display Corporation | Host materials for OLED |
| WO2014106522A1 (de) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2014106524A2 (de) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2014106523A1 (de) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Elektronische vorrichtung |
| US8795850B2 (en) | 2011-05-19 | 2014-08-05 | Universal Display Corporation | Phosphorescent heteroleptic phenylbenzimidazole dopants and new synthetic methodology |
| US8822708B2 (en) | 2007-08-08 | 2014-09-02 | Universal Display Corporation | Benzo-fused thiophene / triphenylene hybrid materials |
| WO2014147134A1 (en) | 2013-03-20 | 2014-09-25 | Basf Se | Azabenzimidazole carbene complexes as efficiency booster in oleds |
| WO2014157618A1 (ja) | 2013-03-29 | 2014-10-02 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、それを具備した照明装置及び表示装置 |
| WO2014157494A1 (ja) | 2013-03-29 | 2014-10-02 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| US8859110B2 (en) | 2008-06-20 | 2014-10-14 | Basf Se | Cyclic phosphazene compounds and use thereof in organic light emitting diodes |
| US8865321B2 (en) | 2008-11-11 | 2014-10-21 | Merck Patent Gmbh | Organic electroluminescent devices |
| WO2014177518A1 (en) | 2013-04-29 | 2014-11-06 | Basf Se | Transition metal complexes with carbene ligands and the use thereof in oleds |
| US8883322B2 (en) | 2011-03-08 | 2014-11-11 | Universal Display Corporation | Pyridyl carbene phosphorescent emitters |
| US8884316B2 (en) | 2011-06-17 | 2014-11-11 | Universal Display Corporation | Non-common capping layer on an organic device |
| US8927749B2 (en) | 2013-03-07 | 2015-01-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8927308B2 (en) | 2011-05-12 | 2015-01-06 | Universal Display Corporation | Method of forming bus line designs for large-area OLED lighting |
| WO2015000955A1 (en) | 2013-07-02 | 2015-01-08 | Basf Se | Monosubstituted diazabenzimidazole carbene metal complexes for use in organic light emitting diodes |
| US8932734B2 (en) | 2010-10-08 | 2015-01-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8946697B1 (en) | 2012-11-09 | 2015-02-03 | Universal Display Corporation | Iridium complexes with aza-benzo fused ligands |
| US8952363B2 (en) | 2009-01-16 | 2015-02-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8952362B2 (en) | 2012-08-31 | 2015-02-10 | The Regents Of The University Of Michigan | High efficiency and brightness fluorescent organic light emitting diode by triplet-triplet fusion |
| US8969592B2 (en) | 2012-01-10 | 2015-03-03 | Universal Display Corporation | Heterocyclic host materials |
| US8968887B2 (en) | 2010-04-28 | 2015-03-03 | Universal Display Corporation | Triphenylene-benzofuran/benzothiophene/benzoselenophene compounds with substituents joining to form fused rings |
| US8987451B2 (en) | 2012-01-03 | 2015-03-24 | Universal Display Corporation | Synthesis of cyclometallated platinum(II) complexes |
| US9005772B2 (en) | 2011-02-23 | 2015-04-14 | Universal Display Corporation | Thioazole and oxazole carbene metal complexes as phosphorescent OLED materials |
| WO2015063046A1 (en) | 2013-10-31 | 2015-05-07 | Basf Se | Azadibenzothiophenes for electronic applications |
| US9040962B2 (en) | 2010-04-28 | 2015-05-26 | Universal Display Corporation | Depositing premixed materials |
| US9054323B2 (en) | 2012-03-15 | 2015-06-09 | Universal Display Corporation | Secondary hole transporting layer with diarylamino-phenyl-carbazole compounds |
| WO2015082046A2 (de) | 2013-12-06 | 2015-06-11 | Merck Patent Gmbh | Substituierte oxepine |
| US9059412B2 (en) | 2012-07-19 | 2015-06-16 | Universal Display Corporation | Transition metal complexes containing substituted imidazole carbene as ligands and their application in OLEDs |
| WO2015086108A1 (de) | 2013-12-12 | 2015-06-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US9065063B2 (en) | 2006-02-10 | 2015-06-23 | Universal Display Corporation | Metal complexes of cyclometallated imidazo[1,2-f]phenanthridine and diimidazo[1,2-a:1′,2′-c]quinazoline ligands and isoelectronic and benzannulated analogs thereof |
| WO2015090504A2 (de) | 2013-12-19 | 2015-06-25 | Merck Patent Gmbh | Heterocyclische spiroverbindungen |
| US9076973B2 (en) | 2008-09-03 | 2015-07-07 | Universal Display Corporation | Phosphorescent materials |
| US9079872B2 (en) | 2010-10-07 | 2015-07-14 | Basf Se | Phenanthro[9, 10-B]furans for electronic applications |
| US9108998B2 (en) | 2009-10-14 | 2015-08-18 | Basf Se | Dinuclear platinum-carbene complexes and the use thereof in OLEDs |
| US9118017B2 (en) | 2012-02-27 | 2015-08-25 | Universal Display Corporation | Host compounds for red phosphorescent OLEDs |
| US9142792B2 (en) | 2010-06-18 | 2015-09-22 | Basf Se | Organic electronic devices comprising a layer comprising at least one metal organic compound and at least one metal oxide |
| US9142786B2 (en) | 2007-03-08 | 2015-09-22 | Universal Display Corporation | Phosphorescent materials |
| US9139764B2 (en) | 2007-09-28 | 2015-09-22 | Osram Opto Semiconductors Gmbh | Organic radiation-emitting component |
| US9166175B2 (en) | 2012-11-27 | 2015-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9163174B2 (en) | 2012-01-04 | 2015-10-20 | Universal Display Corporation | Highly efficient phosphorescent materials |
| US9175211B2 (en) | 2010-03-03 | 2015-11-03 | Universal Display Corporation | Phosphorescent materials |
| WO2015165563A1 (de) | 2014-04-30 | 2015-11-05 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US9181270B2 (en) | 2014-02-28 | 2015-11-10 | Universal Display Corporation | Method of making sulfide compounds |
| US9184399B2 (en) | 2012-05-04 | 2015-11-10 | Universal Display Corporation | Asymmetric hosts with triaryl silane side chains |
| WO2015169412A1 (de) | 2014-05-05 | 2015-11-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US9190620B2 (en) | 2014-03-01 | 2015-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9190623B2 (en) | 2012-11-20 | 2015-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9190621B2 (en) | 2007-03-08 | 2015-11-17 | Universal Display Corporation | Materials for organic light emitting diode |
| US9193745B2 (en) | 2011-11-15 | 2015-11-24 | Universal Display Corporation | Heteroleptic iridium complex |
| US9209411B2 (en) | 2012-12-07 | 2015-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9212197B2 (en) | 2011-05-19 | 2015-12-15 | Universal Display Corporation | Phosphorescent heteroleptic phenylbenzimidazole dopants |
| WO2015192941A1 (de) | 2014-06-18 | 2015-12-23 | Merck Patent Gmbh | Zusammensetzungen für elektronische vorrichtungen |
| US9224958B2 (en) | 2013-07-19 | 2015-12-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2015197156A1 (de) | 2014-06-25 | 2015-12-30 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US9231218B2 (en) | 2012-07-10 | 2016-01-05 | Universal Display Corporation | Phosphorescent emitters containing dibenzo[1,4]azaborinine structure |
| US9252377B2 (en) | 2011-07-14 | 2016-02-02 | Universal Display Corporation | Inorganic hosts in OLEDs |
| WO2016016791A1 (en) | 2014-07-28 | 2016-02-04 | Idemitsu Kosan Co., Ltd (Ikc) | 2,9-functionalized benzimidazolo[1,2-a]benzimidazoles as hosts for organic light emitting diodes (oleds) |
| EP2982676A1 (de) | 2014-08-07 | 2016-02-10 | Idemitsu Kosan Co., Ltd. | Benzimidazo[2,1-b]benzoxazole für elektronische Anwendungen |
| WO2016020516A1 (en) * | 2014-08-08 | 2016-02-11 | Basf Se | Electroluminescent imidazo-quinoxaline carbene metal complexes |
| WO2016027217A1 (en) | 2014-08-18 | 2016-02-25 | Basf Se | Organic semiconductor composition comprising liquid medium |
| EP2993215A1 (de) | 2014-09-04 | 2016-03-09 | Idemitsu Kosan Co., Ltd. | Azabenzimidazo[2,1-a]benzimidazole für elektronische Anwendungen |
| US9287513B2 (en) | 2012-09-24 | 2016-03-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9293712B2 (en) | 2013-10-11 | 2016-03-22 | Universal Display Corporation | Disubstituted pyrene compounds with amino group containing ortho aryl group and devices containing the same |
| US9306179B2 (en) | 2013-11-08 | 2016-04-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9312499B1 (en) | 2015-01-05 | 2016-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9313857B2 (en) | 2011-08-04 | 2016-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9312505B2 (en) | 2012-09-25 | 2016-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9318710B2 (en) | 2012-07-30 | 2016-04-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9315724B2 (en) | 2011-06-14 | 2016-04-19 | Basf Se | Metal complexes comprising azabenzimidazole carbene ligands and the use thereof in OLEDs |
| US9324949B2 (en) | 2013-07-16 | 2016-04-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3015469A1 (de) | 2014-10-30 | 2016-05-04 | Idemitsu Kosan Co., Ltd. | 5-((benz)imidazol-2-yl)benzimidazo[1,2-a]benzimidazole für elektronische anwendungen |
| WO2016074755A1 (de) | 2014-11-11 | 2016-05-19 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2016079667A1 (en) | 2014-11-17 | 2016-05-26 | Idemitsu Kosan Co., Ltd. | Indole derivatives for electronic applications |
| WO2016079169A1 (en) | 2014-11-18 | 2016-05-26 | Basf Se | Pt- or pd-carbene complexes for use in organic light emitting diodes |
| WO2016083914A1 (en) | 2014-11-26 | 2016-06-02 | Basf Se | 4-oxoquinoline compounds |
| US9365767B2 (en) | 2005-02-21 | 2016-06-14 | Mitsubishi Chemical Corporation | Organic electric field light emitting element and production therefor |
| EP3034506A1 (de) | 2014-12-15 | 2016-06-22 | Idemitsu Kosan Co., Ltd | 4-funktionalisierte Carbazolderivate für elektronische Anwendungen |
| EP3034507A1 (de) | 2014-12-15 | 2016-06-22 | Idemitsu Kosan Co., Ltd | 1-funktionalisierte Dibenzofurane und Dibenzothiophene für organische Leuchtdioden (OLEDS) |
| US9386657B2 (en) | 2012-03-15 | 2016-07-05 | Universal Display Corporation | Organic Electroluminescent materials and devices |
| US9385326B2 (en) | 2013-01-15 | 2016-07-05 | Basf Se | Triangulene oligomers and polymers and their use as hole conducting material |
| US9397312B2 (en) | 2011-05-11 | 2016-07-19 | Universal Display Corporation | Process for fabricating metal bus lines for OLED lighting panels |
| US9397310B2 (en) | 2011-07-14 | 2016-07-19 | Universal Display Corporation | Organice electroluminescent materials and devices |
| US9397302B2 (en) | 2014-10-08 | 2016-07-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9399654B2 (en) | 2012-08-02 | 2016-07-26 | Roche Diagnostics Operations, Inc. | Iridium-based complexes for ECL |
| US9406892B2 (en) | 2015-01-07 | 2016-08-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9403859B2 (en) | 2012-08-02 | 2016-08-02 | Roche Diagnostics Operations, Inc. | Iridium-based complexes for ECL |
| WO2016119992A1 (en) | 2015-01-30 | 2016-08-04 | Merck Patent Gmbh | Materials for electronic devices |
| EP3053918A1 (de) | 2015-02-06 | 2016-08-10 | Idemitsu Kosan Co., Ltd | 2-Carbazol substituierte Benzimidazole für elektronische Anwendungen |
| EP3054498A1 (de) | 2015-02-06 | 2016-08-10 | Idemitsu Kosan Co., Ltd. | Bisimidazodiazozine |
| WO2016124304A1 (de) | 2015-02-03 | 2016-08-11 | Merck Patent Gmbh | Metallkomplexe |
| DE102015101767A1 (de) | 2015-02-06 | 2016-08-11 | Technische Universität Dresden | Blaue Fluoreszenzemitter |
| US9416150B2 (en) | 2012-08-02 | 2016-08-16 | Roche Diagnostics Operations, Inc. | Iridium-based complexes for ECL |
| US9419225B2 (en) | 2013-03-14 | 2016-08-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3056504A1 (de) | 2015-02-16 | 2016-08-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3061759A1 (de) | 2015-02-24 | 2016-08-31 | Idemitsu Kosan Co., Ltd | Nitrilsubstituierte dibenzofurane |
| EP3061763A1 (de) | 2015-02-27 | 2016-08-31 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9435021B2 (en) | 2010-07-29 | 2016-09-06 | University Of Southern California | Co-deposition methods for the fabrication of organic optoelectronic devices |
| US9450195B2 (en) | 2014-12-17 | 2016-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3070144A1 (de) | 2015-03-17 | 2016-09-21 | Idemitsu Kosan Co., Ltd. | Siebengliedrige ringverbindungen |
| EP3072943A1 (de) | 2015-03-26 | 2016-09-28 | Idemitsu Kosan Co., Ltd. | Dibenzofuran/carbazol-substituierte benzonitrile |
| US9461254B2 (en) | 2012-01-03 | 2016-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3075737A1 (de) | 2015-03-31 | 2016-10-05 | Idemitsu Kosan Co., Ltd | Benzimidazolo[1,2-a]benzimidazol mit aryl- oder heteroarylnitrilgruppen für organische leuchtdioden |
| US9484541B2 (en) | 2014-10-20 | 2016-11-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9502656B2 (en) | 2014-02-24 | 2016-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9502672B2 (en) | 2012-06-21 | 2016-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3098229A1 (de) | 2015-05-15 | 2016-11-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9512136B2 (en) | 2012-11-26 | 2016-12-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3101021A1 (de) | 2015-06-01 | 2016-12-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2016193243A1 (en) | 2015-06-03 | 2016-12-08 | Udc Ireland Limited | Highly efficient oled devices with very short decay times |
| WO2016198144A1 (en) | 2015-06-10 | 2016-12-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US9537106B2 (en) | 2013-05-09 | 2017-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9543532B2 (en) | 2010-06-11 | 2017-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9540329B2 (en) | 2012-07-19 | 2017-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9553274B2 (en) | 2013-07-16 | 2017-01-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017012687A1 (en) | 2015-07-22 | 2017-01-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP3124488A1 (de) | 2015-07-29 | 2017-02-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2017016630A1 (en) | 2015-07-30 | 2017-02-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2017025166A1 (en) | 2015-08-13 | 2017-02-16 | Merck Patent Gmbh | Hexamethylindanes |
| WO2017028940A1 (en) | 2015-08-14 | 2017-02-23 | Merck Patent Gmbh | Phenoxazine derivatives for organic electroluminescent devices |
| US9590195B2 (en) | 2014-02-28 | 2017-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9590194B2 (en) | 2014-02-14 | 2017-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017036573A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | Compounds for electronic devices |
| US9608206B2 (en) | 2007-08-08 | 2017-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3150604A1 (de) | 2015-10-01 | 2017-04-05 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazol mit benzimidazolo[1,2-a]benzimidazolylgruppen, carbazolylgruppen, benzofurangruppen oder benzothiophengruppen für organische leuchtdioden |
| EP3150606A1 (de) | 2015-10-01 | 2017-04-05 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole mit benzofuran- oder benzothiophen- gruppen für organische licht emittierende dioden. |
| WO2017056055A1 (en) | 2015-10-01 | 2017-04-06 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole carrying triazine groups for organic light emitting diodes |
| US9634265B2 (en) | 2009-04-28 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9634264B2 (en) | 2012-11-09 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3159350A1 (de) | 2015-09-03 | 2017-04-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2017071791A1 (en) | 2015-10-27 | 2017-05-04 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US9647221B2 (en) | 2011-07-14 | 2017-05-09 | Universal Display Corporation | Organic light-emitting devices |
| US9647217B2 (en) | 2014-02-24 | 2017-05-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9647218B2 (en) | 2013-11-14 | 2017-05-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9647227B2 (en) | 2005-04-13 | 2017-05-09 | Universal Display Corporation | Organic light emitting devices |
| WO2017078182A1 (en) | 2015-11-04 | 2017-05-11 | Idemitsu Kosan Co., Ltd. | Benzimidazole fused heteroaryls |
| US9653691B2 (en) | 2012-12-12 | 2017-05-16 | Universal Display Corporation | Phosphorescence-sensitizing fluorescence material system |
| US9663544B2 (en) | 2012-07-25 | 2017-05-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9673406B2 (en) | 2009-05-20 | 2017-06-06 | Universal Display Corporation | Metal complexes with boron-nitrogen heterocycle containing ligands |
| US9673405B2 (en) | 2011-03-01 | 2017-06-06 | Konica Minolta Holdings, Inc. | Organic electroluminescent device, display apparatus, and lighting apparatus |
| US9673401B2 (en) | 2013-06-28 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9670404B2 (en) | 2012-06-06 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9673407B2 (en) | 2014-02-28 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017093958A1 (en) | 2015-12-04 | 2017-06-08 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole derivatives for organic light emitting diodes |
| US9685617B2 (en) | 2012-11-09 | 2017-06-20 | Universal Display Corporation | Organic electronuminescent materials and devices |
| US9691993B2 (en) | 2014-04-09 | 2017-06-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3184534A1 (de) | 2015-12-21 | 2017-06-28 | UDC Ireland Limited | Übergangsmetallkomplexe mit dreibeinigen liganden und verwendung davon in oleds |
| DE102015122869A1 (de) | 2015-12-28 | 2017-06-29 | Technische Universität Dresden | Neue Emittermaterialien und Matrixmaterialien für optoelektronische und elektronische Bauelemente, insbesondere organische lichtemittierende Dioden (OLEDs) |
| WO2017109722A1 (en) | 2015-12-21 | 2017-06-29 | Idemitsu Kosan Co., Ltd. | Nitrogen-containing heterocyclic compounds and organic electroluminescence devices containing them |
| US9711730B2 (en) | 2015-01-25 | 2017-07-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9725476B2 (en) | 2012-07-09 | 2017-08-08 | Universal Display Corporation | Silylated metal complexes |
| WO2017133829A1 (de) | 2016-02-05 | 2017-08-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US9735377B2 (en) | 2005-05-06 | 2017-08-15 | Universal Display Corporation | Phosphorescent emitters and host materials with improved stability |
| US9735373B2 (en) | 2013-06-10 | 2017-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9735378B2 (en) | 2013-09-09 | 2017-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3205658A1 (de) | 2016-02-09 | 2017-08-16 | Universal Display Corporation | Organische elektrolumineszenzmaterialien und vorrichtungen |
| US9741941B2 (en) | 2014-04-29 | 2017-08-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9748500B2 (en) | 2015-01-15 | 2017-08-29 | Universal Display Corporation | Organic light emitting materials |
| US9748503B2 (en) | 2013-09-13 | 2017-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9748504B2 (en) | 2014-03-25 | 2017-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9755164B2 (en) | 2011-06-08 | 2017-09-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9755159B2 (en) | 2014-01-23 | 2017-09-05 | Universal Display Corporation | Organic materials for OLEDs |
| WO2017148564A1 (de) | 2016-03-03 | 2017-09-08 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US9761814B2 (en) | 2014-11-18 | 2017-09-12 | Universal Display Corporation | Organic light-emitting materials and devices |
| US9761807B2 (en) | 2013-07-15 | 2017-09-12 | Universal Display Corporation | Organic light emitting diode materials |
| WO2017157983A1 (de) | 2016-03-17 | 2017-09-21 | Merck Patent Gmbh | Verbindungen mit spirobifluoren-strukturen |
| US9773985B2 (en) | 2012-05-21 | 2017-09-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9780316B2 (en) | 2015-03-16 | 2017-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9783564B2 (en) | 2011-07-25 | 2017-10-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3231809A2 (de) | 2016-04-11 | 2017-10-18 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2017178864A1 (en) | 2016-04-12 | 2017-10-19 | Idemitsu Kosan Co., Ltd. | Seven-membered ring compounds |
| WO2017178311A1 (de) | 2016-04-11 | 2017-10-19 | Merck Patent Gmbh | Heterocyclische verbindungen mit dibenzofuran- und/oder dibenzothiophen-strukturen |
| US9806270B2 (en) | 2011-03-25 | 2017-10-31 | Udc Ireland Limited | 4H-imidazo[1,2-a]imidazoles for electronic applications |
| EP3239161A1 (de) | 2013-07-31 | 2017-11-01 | UDC Ireland Limited | Lumineszente diazabenzimidazol-carben-metall-komplexe |
| WO2017186760A1 (en) | 2016-04-29 | 2017-11-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US9812653B2 (en) | 2013-11-28 | 2017-11-07 | Samsung Electronics Co., Ltd. | Carbazole compound and organic light-emitting device including the same |
| US9825260B2 (en) | 2014-11-26 | 2017-11-21 | Universal Display Corporation | Emissive display with photo-switchable polarization |
| US9831437B2 (en) | 2013-08-20 | 2017-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9831447B2 (en) | 2013-10-08 | 2017-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017207596A1 (en) | 2016-06-03 | 2017-12-07 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US9847497B2 (en) | 2014-02-18 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9847498B2 (en) | 2014-04-14 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9847496B2 (en) | 2013-12-23 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017216299A1 (de) | 2016-06-15 | 2017-12-21 | Technische Universität Dresden | Emittermoleküle auf basis dual fluoreszierender benzol-(poly)carboxylat-akzeptoren |
| US9853229B2 (en) | 2013-10-23 | 2017-12-26 | University Of Southern California | Organic electroluminescent materials and devices |
| US9853227B2 (en) | 2007-03-08 | 2017-12-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3261146A2 (de) | 2016-06-20 | 2017-12-27 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3261147A1 (de) | 2016-06-20 | 2017-12-27 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2017221999A1 (en) | 2016-06-22 | 2017-12-28 | Idemitsu Kosan Co., Ltd. | Specifically substituted benzofuro- and benzothienoquinolines for organic light emitting diodes |
| US9862739B2 (en) | 2014-03-31 | 2018-01-09 | Udc Ireland Limited | Metal complexes, comprising carbene ligands having an O-substituted non-cyclometalated aryl group and their use in organic light emitting diodes |
| WO2018007421A1 (en) | 2016-07-08 | 2018-01-11 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US9871214B2 (en) | 2015-03-23 | 2018-01-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9871212B2 (en) | 2014-11-14 | 2018-01-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3270435A2 (de) | 2016-06-20 | 2018-01-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9876173B2 (en) | 2013-12-09 | 2018-01-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9882151B2 (en) | 2014-11-14 | 2018-01-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9899612B2 (en) | 2006-12-08 | 2018-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9905784B2 (en) | 2013-11-15 | 2018-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9911928B2 (en) | 2015-03-19 | 2018-03-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9911931B2 (en) | 2014-06-26 | 2018-03-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3297051A1 (de) | 2016-09-14 | 2018-03-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2018050583A1 (de) | 2016-09-14 | 2018-03-22 | Merck Patent Gmbh | Verbindungen mit carbazol-strukturen |
| WO2018050584A1 (de) | 2016-09-14 | 2018-03-22 | Merck Patent Gmbh | Verbindungen mit spirobifluoren-strukturen |
| US9929360B2 (en) | 2016-07-08 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9929353B2 (en) | 2014-04-02 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9929357B2 (en) | 2014-07-22 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9935276B2 (en) | 2013-02-21 | 2018-04-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9932359B2 (en) | 2013-08-30 | 2018-04-03 | University Of Southern California | Organic electroluminescent materials and devices |
| US9935277B2 (en) | 2014-01-30 | 2018-04-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3301088A1 (de) | 2016-10-03 | 2018-04-04 | Universal Display Corporation | Kondensierte pyridine als organische elektrolumineszente materialien und vorrichtungen |
| WO2018060307A1 (de) | 2016-09-30 | 2018-04-05 | Merck Patent Gmbh | Verbindungen mit diazadibenzofuran- oder diazadibenzothiophen-strukturen |
| WO2018060218A1 (de) | 2016-09-30 | 2018-04-05 | Merck Patent Gmbh | Carbazole mit diazadibenzofuran- oder diazadibenzothiophen-strukturen |
| EP3305796A1 (de) | 2016-10-07 | 2018-04-11 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9947880B2 (en) | 2011-02-23 | 2018-04-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| DE102017008794A1 (de) | 2016-10-17 | 2018-04-19 | Merck Patent Gmbh | Materialien zur Verwendung in elektronischen Vorrichtungen |
| WO2018069167A1 (de) | 2016-10-10 | 2018-04-19 | Merck Patent Gmbh | Elektronische vorrichtung |
| US9954180B2 (en) | 2010-08-20 | 2018-04-24 | Universal Display Corporation | Bicarbazole compounds for OLEDs |
| EP3318566A1 (de) | 2012-09-20 | 2018-05-09 | UDC Ireland Limited | Azadibenzofurane für elektronische anwendungen |
| WO2018083053A1 (de) | 2016-11-02 | 2018-05-11 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP3321258A1 (de) | 2016-11-09 | 2018-05-16 | Universal Display Corporation | 4-phenylbenzo[g]quinazolin oder 4-(3,5-dimethylphenylbenzo[g]quinazoline iridiumkomplexe zur verwendung als nah-infrarot oder infrarot emittierende materialien in oleds |
| WO2018087020A1 (en) | 2016-11-08 | 2018-05-17 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2018087022A1 (de) | 2016-11-09 | 2018-05-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018087346A1 (de) | 2016-11-14 | 2018-05-17 | Merck Patent Gmbh | Verbindungen mit einer akzeptor- und einer donorgruppe |
| US9978961B2 (en) | 2014-01-08 | 2018-05-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9978958B2 (en) | 2012-08-24 | 2018-05-22 | Universal Display Corporation | Phosphorescent emitters with phenylimidazole ligands |
| US9978956B2 (en) | 2015-07-15 | 2018-05-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3323822A1 (de) | 2016-09-23 | 2018-05-23 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2018091435A1 (en) | 2016-11-17 | 2018-05-24 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2018095381A1 (zh) | 2016-11-23 | 2018-05-31 | 广州华睿光电材料有限公司 | 印刷油墨组合物及其制备方法和用途 |
| WO2018095392A1 (zh) | 2016-11-23 | 2018-05-31 | 广州华睿光电材料有限公司 | 有机混合物、组合物以及有机电子器件 |
| WO2018095888A1 (en) | 2016-11-25 | 2018-05-31 | Merck Patent Gmbh | Bisbenzofuran-fused 2,8-diaminoindeno[1,2-b]fluorene derivatives and related compounds as materials for organic electroluminescent devices (oled) |
| WO2018095395A1 (zh) | 2016-11-23 | 2018-05-31 | 广州华睿光电材料有限公司 | 高聚物、包含其的混合物、组合物和有机电子器件以及用于聚合的单体 |
| WO2018095940A1 (en) | 2016-11-25 | 2018-05-31 | Merck Patent Gmbh | Bisbenzofuran-fused indeno[1,2-b]fluorene derivatives and related compounds as materials for organic electroluminescent devices (oled) |
| WO2018095839A1 (de) | 2016-11-22 | 2018-05-31 | Merck Patent Gmbh | Verbrückte triarylamine für elektronische vorrichtungen |
| WO2018099846A1 (de) | 2016-11-30 | 2018-06-07 | Merck Patent Gmbh | Verbindungen mit valerolaktam-strukturen |
| US9997726B2 (en) | 2007-12-28 | 2018-06-12 | Universal Display Corporation | Dibenzothiophene-containing materials in phosphorescent light emitting diodes |
| US9997712B2 (en) | 2013-03-27 | 2018-06-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9997716B2 (en) | 2014-05-27 | 2018-06-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018104195A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen zur verwendung in oleds |
| WO2018104194A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018103744A1 (zh) | 2016-12-08 | 2018-06-14 | 广州华睿光电材料有限公司 | 混合物、组合物及有机电子器件 |
| WO2018104193A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10003033B2 (en) | 2014-02-18 | 2018-06-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10003034B2 (en) | 2013-09-30 | 2018-06-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10008679B2 (en) | 2014-04-14 | 2018-06-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10008677B2 (en) | 2011-01-13 | 2018-06-26 | Universal Display Corporation | Materials for organic light emitting diode |
| US10008678B2 (en) | 2008-12-12 | 2018-06-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018113785A1 (zh) | 2016-12-22 | 2018-06-28 | 广州华睿光电材料有限公司 | 含呋喃交联基团的聚合物及其应用 |
| WO2018114882A1 (de) | 2016-12-22 | 2018-06-28 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018114883A1 (de) | 2016-12-22 | 2018-06-28 | Merck Patent Gmbh | Mischungen umfassend mindestens zwei organisch funktionelle verbindungen |
| EP3345914A1 (de) | 2017-01-09 | 2018-07-11 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3345984A1 (de) | 2013-12-06 | 2018-07-11 | Merck Patent GmbH | Verbindungen und organische elektronische vorrichtungen |
| WO2018127465A1 (de) | 2017-01-04 | 2018-07-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10033004B2 (en) | 2015-06-01 | 2018-07-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018134392A1 (en) | 2017-01-23 | 2018-07-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10038151B2 (en) | 2014-11-12 | 2018-07-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3354654A2 (de) | 2016-11-11 | 2018-08-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2018138039A1 (de) | 2017-01-25 | 2018-08-02 | Merck Patent Gmbh | Carbazolderivate |
| WO2018138306A1 (de) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10043987B2 (en) | 2014-09-29 | 2018-08-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018141706A1 (de) | 2017-02-02 | 2018-08-09 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US10056565B2 (en) | 2013-11-20 | 2018-08-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018149769A1 (de) | 2017-02-14 | 2018-08-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10069090B2 (en) | 2012-11-20 | 2018-09-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018157981A1 (de) | 2017-03-02 | 2018-09-07 | Merck Patent Gmbh | Materialien für organische elektronische vorrichtungen |
| WO2018158232A1 (en) | 2017-03-01 | 2018-09-07 | Merck Patent Gmbh | Organic electroluminescent device |
| US10074806B2 (en) | 2013-08-20 | 2018-09-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10079349B2 (en) | 2011-05-27 | 2018-09-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018166934A1 (de) | 2017-03-15 | 2018-09-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018166932A1 (de) | 2017-03-13 | 2018-09-20 | Merck Patent Gmbh | Verbindungen mit arylamin-strukturen |
| US10084143B2 (en) | 2008-09-16 | 2018-09-25 | Universal Display Corporation | Phosphorescent materials |
| EP3378857A1 (de) | 2012-11-12 | 2018-09-26 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| EP3381927A1 (de) | 2017-03-29 | 2018-10-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2018189134A1 (de) | 2017-04-13 | 2018-10-18 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| US10109799B2 (en) | 2015-05-21 | 2018-10-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018197447A1 (de) | 2017-04-25 | 2018-11-01 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| US10121975B2 (en) | 2013-07-03 | 2018-11-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3401318A1 (de) | 2017-05-11 | 2018-11-14 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2018206526A1 (en) | 2017-05-11 | 2018-11-15 | Merck Patent Gmbh | Organoboron complexes for organic electroluminescent devices |
| WO2018206537A1 (en) | 2017-05-11 | 2018-11-15 | Merck Patent Gmbh | Carbazole-based bodipys for organic electroluminescent devices |
| US10135006B2 (en) | 2016-01-04 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10135007B2 (en) | 2014-09-29 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10135008B2 (en) | 2014-01-07 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018215318A1 (de) | 2017-05-22 | 2018-11-29 | Merck Patent Gmbh | Hexazyklische heteroaromatische verbindungen für elektronische vorrichtungen |
| US10144867B2 (en) | 2015-02-13 | 2018-12-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10147892B2 (en) | 2010-12-07 | 2018-12-04 | The University Of Southern California | Organic electroluminescent materials and devices |
| US10153443B2 (en) | 2016-07-19 | 2018-12-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10153445B2 (en) | 2016-11-21 | 2018-12-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10158089B2 (en) | 2011-05-27 | 2018-12-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3415521A1 (de) | 2011-06-14 | 2018-12-19 | UDC Ireland Limited | Metallkomplexe mit azabenzimidazolcarbenliganden und verwendung davon in oleds |
| US10164198B2 (en) | 2015-02-05 | 2018-12-25 | Samsung Electronics Co., Ltd. | Organometallic compound, composition containing organometallic compound, and organic light-emitting device including the same |
| EP3418286A1 (de) | 2017-06-23 | 2018-12-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3418285A1 (de) | 2017-06-20 | 2018-12-26 | Idemitsu Kosan Co., Ltd. | Zusammensetzung mit einem substituierten ir-komplex und einem mit einem heteroatom verbrückten phenylchinazolin |
| WO2018234220A1 (de) | 2017-06-21 | 2018-12-27 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018234346A1 (en) | 2017-06-23 | 2018-12-27 | Merck Patent Gmbh | MATERIALS FOR ORGANIC ELECTROLUMINESCENT DEVICES |
| WO2019002190A1 (en) | 2017-06-28 | 2019-01-03 | Merck Patent Gmbh | MATERIALS FOR ELECTRONIC DEVICES |
| WO2019002198A1 (en) | 2017-06-26 | 2019-01-03 | Merck Patent Gmbh | HOMOGENEOUS MIXTURES |
| US10177316B2 (en) | 2015-02-09 | 2019-01-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10177318B2 (en) | 2015-10-29 | 2019-01-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019007867A1 (de) | 2017-07-05 | 2019-01-10 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2019007866A1 (de) | 2017-07-05 | 2019-01-10 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| US10181564B2 (en) | 2015-08-26 | 2019-01-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10186664B2 (en) | 2014-06-17 | 2019-01-22 | Basf Se | N-fluoroalkyl-substituted dibromonaphthalene diimides and their use as semiconductor |
| WO2019020654A1 (en) | 2017-07-28 | 2019-01-31 | Merck Patent Gmbh | SPIROBIFLUORENE DERIVATIVES FOR USE IN ELECTRONIC DEVICES |
| US10199581B2 (en) | 2013-07-01 | 2019-02-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10199582B2 (en) | 2013-09-03 | 2019-02-05 | University Of Southern California | Organic electroluminescent materials and devices |
| US10205105B2 (en) | 2016-08-15 | 2019-02-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10208026B2 (en) | 2014-03-18 | 2019-02-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10211413B2 (en) | 2012-01-17 | 2019-02-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3444258A2 (de) | 2017-08-10 | 2019-02-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10227366B2 (en) | 2012-08-02 | 2019-03-12 | Roche Diagnostics Operations, Inc. | Bis-iridium-complexes for manufacturing of ECL-labels |
| WO2019048443A1 (de) | 2017-09-08 | 2019-03-14 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US10236458B2 (en) | 2016-10-24 | 2019-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019052933A1 (de) | 2017-09-12 | 2019-03-21 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10253252B2 (en) | 2014-12-30 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10256427B2 (en) | 2014-04-15 | 2019-04-09 | Universal Display Corporation | Efficient organic electroluminescent devices |
| US10256419B2 (en) | 2014-05-08 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10256411B2 (en) | 2015-05-21 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3466954A1 (de) | 2017-10-04 | 2019-04-10 | Idemitsu Kosan Co., Ltd. | Mit einem heteroatom verbrückte kondensierte phenylchinazoline |
| WO2019068679A1 (en) | 2017-10-06 | 2019-04-11 | Merck Patent Gmbh | MATERIALS FOR ORGANIC ELECTROLUMINESCENT DEVICES |
| US10270046B2 (en) | 2015-03-06 | 2019-04-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019076789A1 (en) | 2017-10-17 | 2019-04-25 | Merck Patent Gmbh | MATERIALS FOR ORGANIC ELECTROLUMINESCENT DEVICES |
| US10276809B2 (en) | 2016-04-05 | 2019-04-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019081391A1 (de) | 2017-10-24 | 2019-05-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10297770B2 (en) | 2015-03-27 | 2019-05-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10297762B2 (en) | 2014-07-09 | 2019-05-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019096717A2 (de) | 2017-11-14 | 2019-05-23 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| US10301338B2 (en) | 2014-05-08 | 2019-05-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3489243A1 (de) | 2017-11-28 | 2019-05-29 | University of Southern California | Carbenverbindungen und organische elektrolumineszente vorrichtungen |
| WO2019101835A1 (en) | 2017-11-24 | 2019-05-31 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2019101833A1 (en) | 2017-11-24 | 2019-05-31 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2019101719A1 (de) | 2017-11-23 | 2019-05-31 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP3492480A2 (de) | 2017-11-29 | 2019-06-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3492528A1 (de) | 2017-11-30 | 2019-06-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10323180B2 (en) | 2014-12-04 | 2019-06-18 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Deuterated organic compound, mixture and composition containing said compound, and organic electronic device |
| US10326086B2 (en) | 2015-02-06 | 2019-06-18 | Samsung Electronics Co., Ltd. | Organometallic compound, composition containing the organometallic compound, and organic light-emitting device including the organometallic compound or composition |
| WO2019115577A1 (en) | 2017-12-15 | 2019-06-20 | Merck Patent Gmbh | Substituted aromatic amines for use in organic electroluminescent devices |
| WO2019121458A1 (de) | 2017-12-19 | 2019-06-27 | Merck Patent Gmbh | Heterocyclische verbindung zur verwendung in electronischen vorrichtungen |
| WO2019121483A1 (en) | 2017-12-20 | 2019-06-27 | Merck Patent Gmbh | Heteroaromatic compounds |
| US10340464B2 (en) | 2016-11-10 | 2019-07-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10347848B2 (en) | 2013-09-03 | 2019-07-09 | Basf Se | Amorphous material and the use thereof |
| US10355227B2 (en) | 2013-12-16 | 2019-07-16 | Universal Display Corporation | Metal complex for phosphorescent OLED |
| US10355222B2 (en) | 2015-02-06 | 2019-07-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10361375B2 (en) | 2014-10-06 | 2019-07-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10364316B2 (en) | 2015-01-13 | 2019-07-30 | Guangzhou Chinaray Optoelectronics Materials Ltd. | Conjugated polymer containing ethynyl crosslinking group, mixture, formulation, organic electronic device containing the same and application therof |
| WO2019145316A1 (de) | 2018-01-25 | 2019-08-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10388893B2 (en) | 2015-10-29 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10388892B2 (en) | 2015-10-29 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10400163B2 (en) | 2013-02-08 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403830B2 (en) | 2014-05-08 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403826B2 (en) | 2015-05-07 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403825B2 (en) | 2014-02-27 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10411201B2 (en) | 2014-11-12 | 2019-09-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10411200B2 (en) | 2014-08-07 | 2019-09-10 | Universal Display Corporation | Electroluminescent (2-phenylpyridine)iridium complexes and devices |
| US10411199B2 (en) | 2012-12-12 | 2019-09-10 | Samsung Electronics Co., Ltd. | Organometallic complexes, and organic electroluminescent device and display using the same |
| WO2019170572A1 (en) | 2018-03-06 | 2019-09-12 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2019170578A1 (en) | 2018-03-06 | 2019-09-12 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10418562B2 (en) | 2015-02-06 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10418569B2 (en) | 2015-01-25 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019175149A1 (en) | 2018-03-16 | 2019-09-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10454046B2 (en) | 2011-12-09 | 2019-10-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10461260B2 (en) | 2014-06-03 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10457699B2 (en) | 2014-05-02 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10457864B2 (en) | 2016-02-09 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10468609B2 (en) | 2016-06-02 | 2019-11-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10476010B2 (en) | 2015-11-30 | 2019-11-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10490753B2 (en) | 2016-12-15 | 2019-11-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019229011A1 (de) | 2018-05-30 | 2019-12-05 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| US10505127B2 (en) | 2016-09-19 | 2019-12-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019233904A1 (de) | 2018-06-07 | 2019-12-12 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| US10510967B2 (en) | 2014-12-11 | 2019-12-17 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Organic compound, and mixture, formulation and organic device comprising the same |
| US10522769B2 (en) | 2015-08-18 | 2019-12-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10529931B2 (en) | 2015-03-24 | 2020-01-07 | Universal Display Corporation | Organic Electroluminescent materials and devices |
| WO2020011686A1 (de) | 2018-07-09 | 2020-01-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020016264A1 (en) | 2018-07-20 | 2020-01-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP3604477A1 (de) | 2018-07-30 | 2020-02-05 | Idemitsu Kosan Co., Ltd. | Polycyclische verbindung, organische elektrolumineszenzvorrichtung und elektronische vorrichtung |
| EP3608319A1 (de) | 2018-08-07 | 2020-02-12 | Idemitsu Kosan Co., Ltd. | Kondensierte azazyklen als organische lichtemittierende vorrichtungen und materialien zur verwendung darin |
| US10566552B2 (en) | 2016-04-13 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10566546B2 (en) | 2014-07-14 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10566547B2 (en) | 2016-07-11 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3613751A1 (de) | 2018-08-22 | 2020-02-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2020043640A1 (en) | 2018-08-28 | 2020-03-05 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020043657A1 (en) | 2018-08-28 | 2020-03-05 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020043646A1 (en) | 2018-08-28 | 2020-03-05 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10593890B2 (en) | 2015-04-06 | 2020-03-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10593892B2 (en) | 2015-10-01 | 2020-03-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2020053314A1 (de) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Elektrolumineszierende vorrichtungen |
| WO2020053315A1 (de) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Elektrolumineszierende vorrichtungen |
| WO2020053150A1 (en) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10600966B2 (en) | 2015-02-27 | 2020-03-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10600967B2 (en) | 2016-02-18 | 2020-03-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10608188B2 (en) | 2017-09-11 | 2020-03-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10608185B2 (en) | 2016-10-17 | 2020-03-31 | Univeral Display Corporation | Organic electroluminescent materials and devices |
| WO2020064662A2 (de) | 2018-09-27 | 2020-04-02 | Merck Patent Gmbh | Verfahren zur herstellung von sterisch gehinderten stickstoffhaltigen heteroaromatischen verbindungen |
| WO2020064666A1 (de) | 2018-09-27 | 2020-04-02 | Merck Patent Gmbh | Verbindungen, die in einer organischen elektronischen vorrichtung als aktive verbindungen einsetzbar sind |
| US10629820B2 (en) | 2017-01-18 | 2020-04-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10636978B2 (en) | 2014-12-30 | 2020-04-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10636983B2 (en) | 2014-05-08 | 2020-04-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10644251B2 (en) | 2013-12-04 | 2020-05-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10644247B2 (en) | 2015-02-06 | 2020-05-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3647393A1 (de) | 2013-07-30 | 2020-05-06 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2020089138A1 (en) | 2018-10-31 | 2020-05-07 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10651403B2 (en) | 2016-06-20 | 2020-05-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2020094539A1 (de) | 2018-11-05 | 2020-05-14 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2020094542A1 (de) | 2018-11-06 | 2020-05-14 | Merck Patent Gmbh | 5,6-diphenyl-5,6-dihydro-dibenz[c,e][1,2]azaphosphorin- und 6-phenyl-6h-dibenzo[c,e][1,2]thiazin-5,5-dioxid-derivate und ähnliche verbindungen als organische elektrolumineszenzmaterialien für oleds |
| WO2020099307A1 (de) | 2018-11-15 | 2020-05-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020099349A1 (de) | 2018-11-14 | 2020-05-22 | Merck Patent Gmbh | Zur herstellung einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| US10662196B2 (en) | 2016-11-17 | 2020-05-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10672998B2 (en) | 2017-03-23 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680183B2 (en) | 2015-02-15 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10686143B2 (en) | 2015-03-05 | 2020-06-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10686140B2 (en) | 2016-06-20 | 2020-06-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| DE102013200085B4 (de) | 2012-01-06 | 2020-06-18 | Universal Display Corporation | Hocheffiziente phosphoreszierende Materialien |
| WO2020127165A1 (de) | 2018-12-19 | 2020-06-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10707423B2 (en) | 2014-02-21 | 2020-07-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10707427B2 (en) | 2016-02-09 | 2020-07-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10720587B2 (en) | 2016-07-19 | 2020-07-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2020148303A1 (de) | 2019-01-17 | 2020-07-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020148243A1 (en) | 2019-01-16 | 2020-07-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10727423B2 (en) | 2016-06-20 | 2020-07-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3689889A1 (de) | 2019-02-01 | 2020-08-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3690973A1 (de) | 2019-01-30 | 2020-08-05 | University Of Southern California | Organische elektrolumineszente materialien und vorrichtungen |
| US10741762B2 (en) | 2012-05-02 | 2020-08-11 | Clap Co., Ltd. | Method for the deposition of an organic material |
| US10741780B2 (en) | 2017-03-10 | 2020-08-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10749113B2 (en) | 2014-09-29 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10745431B2 (en) | 2017-03-08 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2020169241A1 (de) | 2019-02-18 | 2020-08-27 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| US10770664B2 (en) | 2015-09-21 | 2020-09-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2020178230A1 (en) | 2019-03-04 | 2020-09-10 | Merck Patent Gmbh | Ligands for nano-sized materials |
| US10777754B2 (en) | 2017-04-11 | 2020-09-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10777749B2 (en) | 2015-05-07 | 2020-09-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2020182779A1 (de) | 2019-03-12 | 2020-09-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| EP3712229A1 (de) | 2013-07-30 | 2020-09-23 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2020187865A1 (de) | 2019-03-20 | 2020-09-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10790455B2 (en) | 2017-05-18 | 2020-09-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3715353A1 (de) | 2019-03-26 | 2020-09-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2020193447A1 (de) | 2019-03-25 | 2020-10-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10804475B2 (en) | 2017-01-11 | 2020-10-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10804470B2 (en) | 2016-11-23 | 2020-10-13 | Guangzhou Chinaray Optoelectronic Materials Ltd | Organic compound |
| WO2020208051A1 (en) | 2019-04-11 | 2020-10-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10811618B2 (en) | 2016-12-19 | 2020-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10825997B2 (en) | 2015-06-25 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10822361B2 (en) | 2017-02-22 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10822362B2 (en) | 2017-05-11 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10833276B2 (en) | 2016-11-21 | 2020-11-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10840450B2 (en) | 2014-12-04 | 2020-11-17 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Polymer, and mixture or formulation, and organic electronic device containing same, and monomer thereof |
| US10840458B2 (en) | 2016-05-25 | 2020-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10840459B2 (en) | 2017-05-18 | 2020-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10847728B2 (en) | 2015-10-01 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10854826B2 (en) | 2014-10-08 | 2020-12-01 | Universal Display Corporation | Organic electroluminescent compounds, compositions and devices |
| US10862055B2 (en) | 2017-05-05 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10862046B2 (en) | 2017-03-30 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10868261B2 (en) | 2014-11-10 | 2020-12-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3750897A1 (de) | 2019-06-10 | 2020-12-16 | Universal Display Corporation | Organische elektrolumineszente materialien und geräte |
| US10873036B2 (en) | 2015-07-07 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10870668B2 (en) | 2017-05-05 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10873037B2 (en) | 2017-03-28 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10882877B2 (en) | 2017-03-03 | 2021-01-05 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including the organometallic compound, and diagnostic compositions including the organometallic compound |
| US10897016B2 (en) | 2016-11-14 | 2021-01-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021013775A1 (de) | 2019-07-22 | 2021-01-28 | Merck Patent Gmbh | Verfahren zur herstellung ortho-metallierter metallverbindungen |
| US10910577B2 (en) | 2017-03-28 | 2021-02-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10910570B2 (en) | 2017-04-28 | 2021-02-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3771717A1 (de) | 2019-07-30 | 2021-02-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10923667B2 (en) | 2017-03-08 | 2021-02-16 | Samsung Electronics Co., Ltd. | Organometallic compound, composition containing the organometallic compound, and organic light-emitting device including the organometallic compound |
| EP3778614A1 (de) | 2019-08-16 | 2021-02-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10930866B2 (en) | 2013-07-25 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10930862B2 (en) | 2017-06-01 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10930864B2 (en) | 2017-05-10 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10934293B2 (en) | 2017-05-18 | 2021-03-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021037401A1 (de) | 2019-08-26 | 2021-03-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10944062B2 (en) | 2017-05-18 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10941170B2 (en) | 2017-05-03 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021043703A1 (de) | 2019-09-02 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021043755A1 (de) | 2019-09-03 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10950803B2 (en) | 2014-10-13 | 2021-03-16 | Universal Display Corporation | Compounds and uses in devices |
| US10957861B2 (en) | 2015-12-29 | 2021-03-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10957870B2 (en) | 2012-09-07 | 2021-03-23 | Universal Display Corporation | Organic light emitting device |
| US10957866B2 (en) | 2016-06-30 | 2021-03-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021052921A1 (de) | 2019-09-19 | 2021-03-25 | Merck Patent Gmbh | Mischung von zwei hostmaterialien und organische elektrolumineszierende vorrichtung damit |
| WO2021053046A1 (de) | 2019-09-20 | 2021-03-25 | Merck Patent Gmbh | Peri-kondensierte heterozyklische verbindungen als materialien für elektronische vorrichtungen |
| WO2021052924A1 (en) | 2019-09-16 | 2021-03-25 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10964904B2 (en) | 2017-01-20 | 2021-03-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10964893B2 (en) | 2016-11-17 | 2021-03-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10968226B2 (en) | 2017-06-23 | 2021-04-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10971687B2 (en) | 2017-12-14 | 2021-04-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10968243B2 (en) | 2015-12-04 | 2021-04-06 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Organometallic complex and application thereof in electronic devices |
| US10975113B2 (en) | 2017-04-21 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10978647B2 (en) | 2017-02-15 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10991895B2 (en) | 2015-10-06 | 2021-04-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021078710A1 (en) | 2019-10-22 | 2021-04-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021078831A1 (de) | 2019-10-25 | 2021-04-29 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| US10998507B2 (en) | 2015-11-23 | 2021-05-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3816175A1 (de) | 2019-11-04 | 2021-05-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2021089447A1 (de) | 2019-11-04 | 2021-05-14 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021089450A1 (en) | 2019-11-04 | 2021-05-14 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11011710B2 (en) | 2017-11-23 | 2021-05-18 | Samsung Electronics Co., Ltd. | Organometallic compound and organic light-emitting device including the same |
| WO2021094269A1 (en) | 2019-11-12 | 2021-05-20 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11018309B2 (en) | 2015-08-03 | 2021-05-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11024808B2 (en) | 2015-12-29 | 2021-06-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021110741A1 (en) | 2019-12-04 | 2021-06-10 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11038115B2 (en) | 2017-05-18 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and device |
| US11038137B2 (en) | 2017-04-28 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11038117B2 (en) | 2017-04-11 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021122538A1 (de) | 2019-12-18 | 2021-06-24 | Merck Patent Gmbh | Aromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021122535A1 (de) | 2019-12-17 | 2021-06-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021122740A1 (de) | 2019-12-19 | 2021-06-24 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| US11050028B2 (en) | 2017-01-24 | 2021-06-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11056658B2 (en) | 2017-03-29 | 2021-07-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11053268B2 (en) | 2017-01-20 | 2021-07-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3845545A1 (de) | 2020-01-06 | 2021-07-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11081659B2 (en) | 2018-01-10 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11081658B2 (en) | 2016-10-03 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11081647B2 (en) | 2016-04-22 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3858945A1 (de) | 2020-01-28 | 2021-08-04 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2021151922A1 (de) | 2020-01-29 | 2021-08-05 | Merck Patent Gmbh | Benzimidazol-derivate |
| US11084838B2 (en) | 2017-04-21 | 2021-08-10 | Universal Display Corporation | Organic electroluminescent materials and device |
| US11094891B2 (en) | 2016-03-16 | 2021-08-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11101434B2 (en) | 2017-04-21 | 2021-08-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11108000B2 (en) | 2014-08-07 | 2021-08-31 | Unniversal Display Corporation | Organic electroluminescent materials and devices |
| WO2021170886A2 (de) | 2020-08-06 | 2021-09-02 | Merck Patent Gmbh | Elektronische vorrichtung |
| WO2021170522A1 (de) | 2020-02-25 | 2021-09-02 | Merck Patent Gmbh | Verwendung von heterocyclischen verbindungen in einer organischen elektronischen vorrichtung |
| WO2021175706A1 (de) | 2020-03-02 | 2021-09-10 | Merck Patent Gmbh | Verwendung von sulfonverbindungen in einer organischen elektronischen vorrichtung |
| US11117897B2 (en) | 2017-05-01 | 2021-09-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021180614A1 (de) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021180625A1 (de) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| US11127906B2 (en) | 2016-10-03 | 2021-09-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021185712A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021185829A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021191183A1 (de) | 2020-03-26 | 2021-09-30 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021191117A1 (de) | 2020-03-24 | 2021-09-30 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2021191058A1 (en) | 2020-03-23 | 2021-09-30 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11139443B2 (en) | 2017-03-31 | 2021-10-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021198213A1 (de) | 2020-04-02 | 2021-10-07 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11142538B2 (en) | 2018-03-12 | 2021-10-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021204646A1 (de) | 2020-04-06 | 2021-10-14 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| US11152579B2 (en) | 2016-12-28 | 2021-10-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11158820B2 (en) | 2017-03-29 | 2021-10-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11161933B2 (en) | 2016-12-13 | 2021-11-02 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Conjugated polymer and use thereof in organic electronic device |
| US11165028B2 (en) | 2018-03-12 | 2021-11-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3904361A2 (de) | 2013-10-02 | 2021-11-03 | Merck Patent GmbH | Borenthaltende verbindungen |
| US11168103B2 (en) | 2017-11-17 | 2021-11-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11174259B2 (en) | 2017-06-23 | 2021-11-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11183646B2 (en) | 2017-11-07 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11180519B2 (en) | 2018-02-09 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11183642B2 (en) | 2016-10-03 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11189804B2 (en) | 2016-10-03 | 2021-11-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3916822A1 (de) | 2013-12-20 | 2021-12-01 | UDC Ireland Limited | Hocheffiziente oled-vorrichtungen mit sehr kurzer abklingzeit |
| WO2021239772A1 (de) | 2020-05-29 | 2021-12-02 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| US11201298B2 (en) | 2017-01-09 | 2021-12-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11201299B2 (en) | 2017-05-04 | 2021-12-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021254984A1 (de) | 2020-06-18 | 2021-12-23 | Merck Patent Gmbh | Indenoazanaphthaline |
| WO2021259824A1 (de) | 2020-06-23 | 2021-12-30 | Merck Patent Gmbh | Verfahren zur herstellung einer mischung |
| US11214587B2 (en) | 2017-11-07 | 2022-01-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11217757B2 (en) | 2018-03-12 | 2022-01-04 | Universal Display Corporation | Host materials for electroluminescent devices |
| WO2022002772A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022002771A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| EP3937268A1 (de) | 2020-07-10 | 2022-01-12 | Universal Display Corporation | Plasmonische oleds und vertikale dipolstrahler |
| US11228002B2 (en) | 2016-04-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228004B2 (en) | 2018-06-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228003B2 (en) | 2016-04-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228010B2 (en) | 2017-07-26 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11233205B2 (en) | 2017-12-14 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11233204B2 (en) | 2017-12-14 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11233203B2 (en) | 2018-09-06 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2022017997A1 (en) | 2020-07-22 | 2022-01-27 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11239433B2 (en) | 2017-07-26 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11239434B2 (en) | 2018-02-09 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11239432B2 (en) | 2016-10-14 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11239428B2 (en) | 2016-11-23 | 2022-02-01 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Boron-containing organic compound and applications thereof, organic mixture, and organic electronic device |
| WO2022029096A1 (de) | 2020-08-06 | 2022-02-10 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022034046A1 (de) | 2020-08-13 | 2022-02-17 | Merck Patent Gmbh | Metallkomplexe |
| WO2022038066A1 (de) | 2020-08-19 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022038065A1 (de) | 2020-08-18 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11261207B2 (en) | 2018-06-25 | 2022-03-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11271177B2 (en) | 2018-01-11 | 2022-03-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11276829B2 (en) | 2017-03-31 | 2022-03-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11279722B2 (en) | 2018-03-12 | 2022-03-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11292875B2 (en) | 2016-12-22 | 2022-04-05 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Cross-linkable polymer based on Diels-Alder reaction and use thereof in organic electronic device |
| US11296283B2 (en) | 2018-06-04 | 2022-04-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2022069422A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Verbindungen zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen |
| WO2022069421A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen einsetzbare verbindungen |
| US11302872B2 (en) | 2015-09-09 | 2022-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2022079068A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022079067A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Verbindungen mit heteroatomen für organische elektrolumineszenzvorrichtungen |
| US11322691B2 (en) | 2017-07-26 | 2022-05-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11325932B2 (en) | 2019-02-08 | 2022-05-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2022101171A1 (de) | 2020-11-10 | 2022-05-19 | Merck Patent Gmbh | Schwefelhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| US11339182B2 (en) | 2018-06-07 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342509B2 (en) | 2018-02-09 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342513B2 (en) | 2018-05-04 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4001287A1 (de) | 2020-11-24 | 2022-05-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4001286A1 (de) | 2020-11-24 | 2022-05-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11349083B2 (en) | 2017-08-10 | 2022-05-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2022117473A1 (de) | 2020-12-02 | 2022-06-09 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022122682A2 (de) | 2020-12-10 | 2022-06-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11367840B2 (en) | 2018-01-26 | 2022-06-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4016659A1 (de) | 2020-11-16 | 2022-06-22 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2022129113A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| WO2022129116A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Indolo[3.2.1-jk]carbazole-6-carbonitril-derivate als blau fluoreszierende emitter zur verwendung in oleds |
| WO2022129114A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| US11374181B2 (en) | 2019-08-14 | 2022-06-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11370809B2 (en) | 2019-02-08 | 2022-06-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4019526A1 (de) | 2018-01-26 | 2022-06-29 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2022148717A1 (de) | 2021-01-05 | 2022-07-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11390639B2 (en) | 2018-04-13 | 2022-07-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2022157343A1 (de) | 2021-01-25 | 2022-07-28 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| US11404651B2 (en) | 2017-12-14 | 2022-08-02 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Transition metal complex material and application thereof in electronic devices |
| EP4037000A1 (de) | 2014-07-21 | 2022-08-03 | Merck Patent GmbH | Materialen für elektronische vorrichtungen |
| EP4039692A1 (de) | 2021-02-03 | 2022-08-10 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11424420B2 (en) | 2017-09-07 | 2022-08-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11437591B2 (en) | 2017-08-24 | 2022-09-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4053137A1 (de) | 2021-03-05 | 2022-09-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2022184601A1 (de) | 2021-03-02 | 2022-09-09 | Merck Patent Gmbh | Verbindungen für organische elektrolumineszenzvorrichtungen |
| US11444249B2 (en) | 2017-09-07 | 2022-09-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4056578A1 (de) | 2021-03-12 | 2022-09-14 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11447496B2 (en) | 2016-11-23 | 2022-09-20 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Nitrogen-containing fused heterocyclic ring compound and application thereof |
| US11450822B2 (en) | 2018-05-25 | 2022-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4059941A1 (de) | 2021-03-15 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4059915A2 (de) | 2021-02-26 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4060758A2 (de) | 2021-02-26 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2022194799A1 (de) | 2021-03-18 | 2022-09-22 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022200638A1 (de) | 2021-07-06 | 2022-09-29 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11459349B2 (en) | 2018-05-25 | 2022-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11462697B2 (en) | 2017-08-22 | 2022-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11469382B2 (en) | 2017-07-12 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11469383B2 (en) | 2018-10-08 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11469384B2 (en) | 2018-11-02 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11476430B2 (en) | 2018-10-15 | 2022-10-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4075531A1 (de) | 2021-04-13 | 2022-10-19 | Universal Display Corporation | Plasmonische oleds und vertikale dipolstrahler |
| EP4075530A1 (de) | 2021-04-14 | 2022-10-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4074723A1 (de) | 2021-04-05 | 2022-10-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4079743A1 (de) | 2021-04-23 | 2022-10-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11485706B2 (en) | 2018-09-11 | 2022-11-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2022229298A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229126A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229234A1 (de) | 2021-04-30 | 2022-11-03 | Merck Patent Gmbh | Stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| US11495756B2 (en) | 2019-05-07 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495752B2 (en) | 2018-10-08 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495757B2 (en) | 2017-06-23 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4086266A1 (de) | 2021-04-23 | 2022-11-09 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11508913B2 (en) | 2017-08-10 | 2022-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2022243403A1 (de) | 2021-05-21 | 2022-11-24 | Merck Patent Gmbh | Verfahren zur kontinuierlichen aufreinigung von mindestens einem funktionalen material und vorrichtung zur kontinuierlichen aufreinigung von mindestens einem funktionalen material |
| US11515493B2 (en) | 2018-01-11 | 2022-11-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11515482B2 (en) | 2018-10-23 | 2022-11-29 | Universal Display Corporation | Deep HOMO (highest occupied molecular orbital) emitter device structures |
| US11515494B2 (en) | 2018-05-04 | 2022-11-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11512093B2 (en) | 2019-03-04 | 2022-11-29 | Universal Display Corporation | Compound used for organic light emitting device (OLED), consumer product and formulation |
| US11515489B2 (en) | 2018-11-28 | 2022-11-29 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11522140B2 (en) | 2015-08-17 | 2022-12-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11545636B2 (en) | 2016-12-15 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11545637B2 (en) | 2017-01-13 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4112701A2 (de) | 2021-06-08 | 2023-01-04 | University of Southern California | Molekulare ausrichtung homoleptischer iridiumphosphore |
| US11548905B2 (en) | 2016-12-15 | 2023-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11552261B2 (en) | 2017-06-23 | 2023-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11557738B2 (en) | 2019-02-22 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11555128B2 (en) | 2015-11-12 | 2023-01-17 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Printing composition, electronic device comprising same and preparation method for functional material thin film |
| US11557733B2 (en) | 2018-03-12 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11555048B2 (en) | 2016-12-01 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11569480B2 (en) | 2019-03-12 | 2023-01-31 | Universal Display Corporation | Plasmonic OLEDs and vertical dipole emitters |
| US11594690B2 (en) | 2017-12-14 | 2023-02-28 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Organometallic complex, and polymer, mixture and formulation comprising same, and use thereof in electronic device |
| US11600787B2 (en) | 2019-08-30 | 2023-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11605791B2 (en) | 2017-09-01 | 2023-03-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2023036976A1 (en) | 2021-09-13 | 2023-03-16 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11608321B2 (en) | 2017-06-23 | 2023-03-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4151699A1 (de) | 2021-09-17 | 2023-03-22 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2023041454A1 (de) | 2021-09-14 | 2023-03-23 | Merck Patent Gmbh | Borhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| US11616203B2 (en) | 2018-04-17 | 2023-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11613550B2 (en) | 2019-04-30 | 2023-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices comprising benzimidazole-containing metal complexes |
| WO2023052275A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052314A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052272A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052313A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US11623936B2 (en) | 2018-12-11 | 2023-04-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11637261B2 (en) | 2019-03-12 | 2023-04-25 | Universal Display Corporation | Nanopatch antenna outcoupling structure for use in OLEDs |
| US11634444B2 (en) | 2016-11-23 | 2023-04-25 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Metal organic complex, high polymer, composition, and organic electronic component |
| US11634445B2 (en) | 2019-05-21 | 2023-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11637251B2 (en) | 2009-03-23 | 2023-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11639363B2 (en) | 2019-04-22 | 2023-05-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2023072799A1 (de) | 2021-10-27 | 2023-05-04 | Merck Patent Gmbh | Bor- und stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| US11647667B2 (en) | 2019-06-14 | 2023-05-09 | Universal Display Corporation | Organic electroluminescent compounds and organic light emitting devices using the same |
| WO2023094412A1 (de) | 2021-11-25 | 2023-06-01 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US11672176B2 (en) | 2018-11-28 | 2023-06-06 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11672165B2 (en) | 2018-11-28 | 2023-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2023099543A1 (en) | 2021-11-30 | 2023-06-08 | Merck Patent Gmbh | Compounds having fluorene structures |
| US11678565B2 (en) | 2017-06-23 | 2023-06-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11674080B2 (en) | 2017-12-14 | 2023-06-13 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Transition metal complex, polymer, mixture, formulation and use thereof |
| US11680059B2 (en) | 2017-12-21 | 2023-06-20 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Organic mixture and application thereof in organic electronic devices |
| WO2023110742A1 (de) | 2021-12-13 | 2023-06-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11690285B2 (en) | 2018-11-28 | 2023-06-27 | Universal Display Corporation | Electroluminescent devices |
| US11685754B2 (en) | 2019-07-22 | 2023-06-27 | Universal Display Corporation | Heteroleptic organic electroluminescent materials |
| WO2023117837A1 (de) | 2021-12-21 | 2023-06-29 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| US11696492B2 (en) | 2017-09-07 | 2023-07-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11697653B2 (en) | 2019-10-21 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11700765B2 (en) | 2018-01-10 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4212539A1 (de) | 2021-12-16 | 2023-07-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11708355B2 (en) | 2019-08-01 | 2023-07-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11716899B2 (en) | 2018-11-28 | 2023-08-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11716900B2 (en) | 2018-05-30 | 2023-08-01 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11723269B2 (en) | 2017-08-22 | 2023-08-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11718634B2 (en) | 2018-09-14 | 2023-08-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11725022B2 (en) | 2017-06-23 | 2023-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2023152063A1 (de) | 2022-02-09 | 2023-08-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023152346A1 (de) | 2022-02-14 | 2023-08-17 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP4231804A2 (de) | 2022-02-16 | 2023-08-23 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11739081B2 (en) | 2019-03-11 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11744141B2 (en) | 2017-08-09 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2023161168A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Aromatische heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2023161167A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| US11753425B2 (en) | 2018-07-11 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11758804B2 (en) | 2017-06-23 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11753427B2 (en) | 2018-05-04 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4242285A1 (de) | 2022-03-09 | 2023-09-13 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11765968B2 (en) | 2017-01-23 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11765965B2 (en) | 2019-10-30 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11765970B2 (en) | 2017-07-26 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11773320B2 (en) | 2019-02-21 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11778897B2 (en) | 2017-09-20 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11778895B2 (en) | 2020-01-13 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11778899B2 (en) | 2019-06-13 | 2023-10-03 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including the same, and diagnostic composition including the organometallic compound |
| US11793073B2 (en) | 2018-05-06 | 2023-10-17 | Universal Display Corporation | Host materials for electroluminescent devices |
| EP4265626A2 (de) | 2022-04-18 | 2023-10-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11802136B2 (en) | 2017-06-23 | 2023-10-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4271160A2 (de) | 2015-02-13 | 2023-11-01 | Merck Patent GmbH | Aromatisches heterocyclisches derivat und organisches elektrolumineszenzelement, beleuchtungsvorrichtung und anzeigevorrichtung mit dem aromatischen heterocyclischen derivat |
| US11812622B2 (en) | 2015-09-25 | 2023-11-07 | Universal Display Corporation | Organic electroluminescent compounds and devices |
| US11807654B2 (en) | 2019-05-10 | 2023-11-07 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including organometallic compound, and diagnostic composition including organometallic compound |
| US11812624B2 (en) | 2019-01-30 | 2023-11-07 | The University Of Southern California | Organic electroluminescent materials and devices |
| WO2023213837A1 (de) | 2022-05-06 | 2023-11-09 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| US11814403B2 (en) | 2017-06-23 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11818949B2 (en) | 2015-04-06 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11820783B2 (en) | 2019-09-06 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11825735B2 (en) | 2017-11-28 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11825736B2 (en) | 2018-11-19 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2023222559A1 (de) | 2022-05-18 | 2023-11-23 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| US11832510B2 (en) | 2017-06-23 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11827651B2 (en) | 2019-05-13 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11832509B2 (en) | 2019-06-13 | 2023-11-28 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including the same, and diagnostic composition including the organometallic compound |
| EP4282863A1 (de) | 2022-05-24 | 2023-11-29 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11834459B2 (en) | 2018-12-12 | 2023-12-05 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11844266B2 (en) | 2019-01-31 | 2023-12-12 | Samsung Electronics Co., Ltd. | Organometallic compound and organic light-emitting device including the same |
| EP4293001A1 (de) | 2022-06-08 | 2023-12-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2023247663A1 (de) | 2022-06-24 | 2023-12-28 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2023247662A1 (de) | 2022-06-24 | 2023-12-28 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| US11864458B2 (en) | 2019-10-08 | 2024-01-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11858949B2 (en) | 2019-06-13 | 2024-01-02 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including the same, and diagnostic composition including the organometallic compound |
| EP4299693A1 (de) | 2022-06-28 | 2024-01-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11871653B2 (en) | 2019-02-22 | 2024-01-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2024013004A1 (de) | 2022-07-11 | 2024-01-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US11882759B2 (en) | 2018-04-13 | 2024-01-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11889708B2 (en) | 2019-11-14 | 2024-01-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11889749B2 (en) | 2019-08-09 | 2024-01-30 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including organometallic compound, and diagnostic composition including organometallic compound |
| US11903305B2 (en) | 2018-09-24 | 2024-02-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2024033282A1 (en) | 2022-08-09 | 2024-02-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11910700B2 (en) | 2009-03-23 | 2024-02-20 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US11910702B2 (en) | 2017-11-07 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent devices |
| US11910699B2 (en) | 2017-08-10 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4326030A1 (de) | 2022-08-17 | 2024-02-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11917900B2 (en) | 2020-01-28 | 2024-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11917843B2 (en) | 2017-07-26 | 2024-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11925103B2 (en) | 2018-06-05 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11925102B2 (en) | 2015-06-04 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11925105B2 (en) | 2019-08-26 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11920070B2 (en) | 2019-07-12 | 2024-03-05 | The University Of Southern California | Luminescent janus-type, two-coordinated metal complexes |
| US11919914B2 (en) | 2019-10-25 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11926638B2 (en) | 2019-07-22 | 2024-03-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11930699B2 (en) | 2019-08-15 | 2024-03-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11937494B2 (en) | 2019-08-28 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11932660B2 (en) | 2020-01-29 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11944000B2 (en) | 2013-10-29 | 2024-03-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2024061948A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024061942A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| US11950493B2 (en) | 2019-10-15 | 2024-04-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11957050B2 (en) | 2018-02-09 | 2024-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11963441B2 (en) | 2018-11-26 | 2024-04-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11963438B2 (en) | 2019-03-26 | 2024-04-16 | The University Of Southern California | Organic electroluminescent materials and devices |
Families Citing this family (69)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10338550A1 (de) * | 2003-08-19 | 2005-03-31 | Basf Ag | Übergangsmetallkomplexe mit Carbenliganden als Emitter für organische Licht-emittierende Dioden (OLEDs) |
| US7598388B2 (en) | 2004-05-18 | 2009-10-06 | The University Of Southern California | Carbene containing metal complexes as OLEDs |
| US7601436B2 (en) | 2004-05-18 | 2009-10-13 | The University Of Southern California | Carbene metal complexes as OLED materials |
| US7491823B2 (en) * | 2004-05-18 | 2009-02-17 | The University Of Southern California | Luminescent compounds with carbene ligands |
| US7534505B2 (en) * | 2004-05-18 | 2009-05-19 | The University Of Southern California | Organometallic compounds for use in electroluminescent devices |
| US7655323B2 (en) * | 2004-05-18 | 2010-02-02 | The University Of Southern California | OLEDs utilizing macrocyclic ligand systems |
| US7393599B2 (en) * | 2004-05-18 | 2008-07-01 | The University Of Southern California | Luminescent compounds with carbene ligands |
| JP5130606B2 (ja) * | 2005-02-25 | 2013-01-30 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、その製造方法、表示装置及び照明装置 |
| US9051344B2 (en) * | 2005-05-06 | 2015-06-09 | Universal Display Corporation | Stability OLED materials and devices |
| DE102005032332A1 (de) * | 2005-07-08 | 2007-01-11 | Merck Patent Gmbh | Metallkomplexe |
| US20080233410A1 (en) * | 2005-11-17 | 2008-09-25 | Idemitsu Kosan Co., Ltd. | Transition metal complex compound |
| TWI313292B (en) * | 2005-11-25 | 2009-08-11 | Chi Mei Optoelectronics Corp | Light-emitting element and iridium complex |
| EP1803789A1 (de) | 2005-12-28 | 2007-07-04 | Novaled AG | Verwendung von Metallkomplexen als Emitter in einem elektronischen Bauelement und elektronisches Bauelement |
| DE102006006412A1 (de) * | 2006-02-13 | 2007-08-16 | Merck Patent Gmbh | Elektronisches Bauteil, Verfahren zu dessen Herstellung und dessen Verwendung |
| JP5356213B2 (ja) | 2006-03-30 | 2013-12-04 | ノヴァレッド・アクチエンゲゼルシャフト | ボラ−テトラアザペンタレンの使用 |
| EP1860709B1 (de) | 2006-05-24 | 2012-08-08 | Novaled AG | Verwendung von quadratisch planaren Übergangsmetallkomplexen als Dotand |
| DE102006030860A1 (de) | 2006-07-04 | 2008-01-10 | Universität Regensburg | Oligomere von Isonitril-Metallkomplexen als Triplett-Emitter für OLED-Anwendungen |
| DE102006035018B4 (de) | 2006-07-28 | 2009-07-23 | Novaled Ag | Oxazol-Triplett-Emitter für OLED-Anwendungen |
| DE102006048202A1 (de) * | 2006-10-11 | 2008-04-17 | Universität Regensburg | Lanthanoid-Emitter für OLED-Anwendungen |
| DE102006051975B4 (de) | 2006-11-03 | 2012-04-19 | Merck Patent Gmbh | Photophysikalische OLED-Effizienz-Steigerung |
| JP5194568B2 (ja) * | 2006-11-27 | 2013-05-08 | 住友化学株式会社 | 発光性膜 |
| DE102007002420A1 (de) | 2007-01-17 | 2008-07-24 | Universität Regensburg | Polymere Anionen/Kationen |
| JP5260905B2 (ja) * | 2007-07-12 | 2013-08-14 | 株式会社ジャパンディスプレイ | 有機el表示装置 |
| US20100258790A1 (en) * | 2007-10-24 | 2010-10-14 | Basf Se | Use of diphenylamino-bis(phenoxy)- and bis(diphenylamino)-phenoxytriazine compounds |
| US7960547B2 (en) * | 2007-12-03 | 2011-06-14 | Chien-Hong Cheng | Transition metal complexes with carbene ligands and their application |
| KR101462653B1 (ko) * | 2008-05-20 | 2014-11-17 | 삼성전자 주식회사 | 카르벤 유도체를 이용한 나노입자 제조방법 |
| JP4991634B2 (ja) * | 2008-06-09 | 2012-08-01 | キヤノン株式会社 | 有機el発光装置 |
| DE102008033563A1 (de) * | 2008-07-17 | 2010-01-21 | Merck Patent Gmbh | Komplexe mit kleinen Singulett-Triplett-Energie-Abständen zur Verwendung in opto-elektronischen Bauteilen (Singulett-Harvesting-Effekt) |
| DE102008048336A1 (de) | 2008-09-22 | 2010-03-25 | Merck Patent Gmbh | Einkernige neutrale Kupfer(I)-Komplexe und deren Verwendung zur Herstellung von optoelektronischen Bauelementen |
| EP3185333B1 (de) | 2008-09-25 | 2023-09-06 | Universal Display Corporation | Organoselenmaterialien und deren verwendung in organischen lichtemittierenden vorrichtungen |
| US8119037B2 (en) | 2008-10-16 | 2012-02-21 | Novaled Ag | Square planar transition metal complexes and organic semiconductive materials using them as well as electronic or optoelectric components |
| DE102008053121A1 (de) | 2008-10-24 | 2010-04-29 | Merck Patent Gmbh | Doppelkomplex-Salze als Emitter in OLED-Vorrichtungen |
| JP5540507B2 (ja) * | 2009-01-22 | 2014-07-02 | 宇部興産株式会社 | 有機エレクトロルミネッセンス素子 |
| DE102009030475A1 (de) | 2009-06-24 | 2011-01-05 | Hartmut Prof. Dr. Yersin | Kupfer-Komplexe für optoelektronische Anwendungen |
| US8288187B2 (en) | 2010-01-20 | 2012-10-16 | Universal Display Corporation | Electroluminescent devices for lighting applications |
| US9156870B2 (en) | 2010-02-25 | 2015-10-13 | Universal Display Corporation | Phosphorescent emitters |
| EP2550690B1 (de) | 2010-03-25 | 2018-12-26 | Universal Display Corporation | Lösungsverarbeitbare dotierte triarylaminlochinjektionsmaterialien |
| KR101806586B1 (ko) * | 2010-06-18 | 2017-12-07 | 유디씨 아일랜드 리미티드 | 하나 이상의 금속 유기 화합물 및 하나 이상의 금속 산화물을 함유하는 층을 포함하는 유기 전자 소자 |
| US20110309344A1 (en) * | 2010-06-18 | 2011-12-22 | Basf Se | Organic electronic devices comprising a layer of a pyridine compound and a 8-hydroxypquinolinolato earth alkaline metal, or alkali metal complex |
| US9203037B2 (en) * | 2010-06-18 | 2015-12-01 | Basf Se | Organic electronic devices comprising a layer of a dibenzofurane compound and a 8-hydroxypquinolinolato earth alkaline metal, or alkali metal complex |
| CN103154189B (zh) * | 2010-10-06 | 2016-04-13 | 夏普株式会社 | 发光材料和使用其的有机发光元件、波长变换发光元件、光变换发光元件、有机激光二极管发光元件、色素激光器、显示装置以及照明装置 |
| US20130303777A1 (en) * | 2010-10-06 | 2013-11-14 | Sharp Kabushiki Kaisha | Luminescent material, and organic light-emitting element, wavelength-converting light-emitting element, light-converting light-emitting element, organic laser diode light-emitting element, dye laser, display device, and illumination device using same |
| JP2014141415A (ja) * | 2011-05-19 | 2014-08-07 | Sharp Corp | 遷移金属錯体、及びこれを用いた有機発光素子、色変換発光素子、光変換発光素子、有機レーザーダイオード発光素子、色素レーザー、表示装置、照明装置並びに電子機器 |
| JP5316583B2 (ja) * | 2011-05-24 | 2013-10-16 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、それを用いた表示装置および照明装置 |
| US9493698B2 (en) | 2011-08-31 | 2016-11-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| TWI506030B (zh) * | 2011-09-06 | 2015-11-01 | Nat Univ Tsing Hua | 含有碳烯配位基的過渡金屬錯合物結構及其在發光材料的應用 |
| US9289759B2 (en) * | 2011-09-13 | 2016-03-22 | Rutgers, The State University Of New Jersey | Iridium catalyst complexes and C—H bond activated products therefrom |
| EP2594571A1 (de) | 2011-11-16 | 2013-05-22 | Cynora GmbH | Kupfer-Komplexe für optoelektronische Anwendungen |
| US9217004B2 (en) | 2011-11-21 | 2015-12-22 | Universal Display Corporation | Organic light emitting materials |
| US20130146875A1 (en) | 2011-12-13 | 2013-06-13 | Universal Display Corporation | Split electrode for organic devices |
| JP5929512B2 (ja) * | 2012-05-24 | 2016-06-08 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、その製造方法及び照明装置 |
| US9196860B2 (en) | 2012-12-04 | 2015-11-24 | Universal Display Corporation | Compounds for triplet-triplet annihilation upconversion |
| JP5626384B2 (ja) * | 2013-02-06 | 2014-11-19 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| DE102013225682A1 (de) * | 2013-12-12 | 2015-06-18 | Friedrich-Alexander-Universität Erlangen-Nürnberg | Metallionaddukte von neutralen phosphoreszenten Emittern zur Verwendung in lichtemittierenden organischen optoelektronischen Bauteilen |
| US9397309B2 (en) | 2014-03-13 | 2016-07-19 | Universal Display Corporation | Organic electroluminescent devices |
| US9450198B2 (en) | 2014-04-15 | 2016-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9929365B2 (en) * | 2014-05-28 | 2018-03-27 | The Regents Of The University Of Michigan | Excited state management |
| WO2016055557A1 (de) | 2014-10-08 | 2016-04-14 | Cynora Gmbh | Metall-komplexe mit tridentaten liganden für optoelektronische anwendungen |
| GB201421390D0 (en) | 2014-12-02 | 2015-01-14 | Univ St Andrews | Luminescent complexes for OLEDs |
| US9478758B1 (en) | 2015-05-08 | 2016-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10290816B2 (en) | 2015-11-16 | 2019-05-14 | The Regents Of The University Of Michigan | Organic electroluminescent materials and devices |
| DE102016208298A1 (de) * | 2016-05-13 | 2017-11-16 | Siemens Aktiengesellschaft | Organische elektronenleitende Schicht mit n-Dotierstoff |
| US10916714B2 (en) * | 2016-09-27 | 2021-02-09 | Samsung Display Co., Ltd. | Organometallic compound and organic light-emitting device including the same |
| WO2018190043A1 (ja) * | 2017-04-12 | 2018-10-18 | コニカミノルタ株式会社 | 塗布液、塗布液の製造方法、塗布膜及び有機エレクトロルミネッセンス素子 |
| US11968883B2 (en) | 2017-07-26 | 2024-04-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| KR102456073B1 (ko) | 2017-07-28 | 2022-10-19 | 삼성디스플레이 주식회사 | 유기금속 화합물 및 이를 포함한 유기 발광 소자 |
| US11845764B2 (en) | 2018-01-26 | 2023-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| KR20210067007A (ko) | 2019-11-28 | 2021-06-08 | 삼성디스플레이 주식회사 | 유기금속 화합물, 이를 포함하는 유기 발광 소자 및 이를 포함하는 장치 |
| CN113244964B (zh) * | 2021-06-03 | 2023-04-21 | 陕西延长石油(集团)有限责任公司 | 金属配合物催化剂及碳酸二苯酯的合成工艺 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| WO2001041512A1 (en) | 1999-12-01 | 2001-06-07 | The Trustees Of Princeton University | Complexes of form l2mx as phosphorescent dopants for organic leds |
| WO2002015645A1 (en) | 2000-08-11 | 2002-02-21 | The Trustees Of Princeton University | Organometallic compounds and emission-shifting organic electrophosphorescence |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5312940A (en) * | 1992-04-03 | 1994-05-17 | California Institute Of Technology | Ruthenium and osmium metal carbene complexes for olefin metathesis polymerization |
| US6830828B2 (en) * | 1998-09-14 | 2004-12-14 | The Trustees Of Princeton University | Organometallic complexes as phosphorescent emitters in organic LEDs |
| US6160267A (en) | 1999-01-05 | 2000-12-12 | Regents Of The University Of Minnesota | Vapochromic led |
| JP2001185628A (ja) * | 1999-12-22 | 2001-07-06 | Nec Corp | 半導体装置及びその製造方法 |
| DE10062577B4 (de) * | 2000-12-15 | 2006-06-29 | Umicore Ag & Co. Kg | Carben-Dien-Komplexe von Nickel,Palladium und Platin |
| EP1421828B1 (de) * | 2001-08-29 | 2015-10-14 | The Trustees Of Princeton University | Organische lichtemittierende einrichtungen mit trägertransportschichten mit metallkomplexen |
| CN1239672C (zh) * | 2002-09-23 | 2006-02-01 | 清华大学 | 一种电致发光磷光材料及其应用 |
| DE10338550A1 (de) * | 2003-08-19 | 2005-03-31 | Basf Ag | Übergangsmetallkomplexe mit Carbenliganden als Emitter für organische Licht-emittierende Dioden (OLEDs) |
| DE102004057072A1 (de) | 2004-11-25 | 2006-06-01 | Basf Ag | Verwendung von Übergangsmetall-Carbenkomplexen in organischen Licht-emittierenden Dioden (OLEDs) |
-
2003
- 2003-08-19 DE DE10338550A patent/DE10338550A1/de not_active Withdrawn
-
2004
- 2004-08-18 JP JP2006523602A patent/JP4351702B2/ja active Active
- 2004-08-18 EP EP20191338.1A patent/EP3805338A1/de active Pending
- 2004-08-18 WO PCT/EP2004/009269 patent/WO2005019373A2/de active Search and Examination
- 2004-08-18 EP EP04764255.8A patent/EP1658349B1/de active Active
- 2004-08-18 KR KR1020067003352A patent/KR101186706B1/ko active IP Right Grant
- 2004-08-18 US US10/568,344 patent/US7846763B2/en active Active
- 2004-08-18 CN CNB2004800306492A patent/CN100573961C/zh active Active
- 2004-08-18 EP EP17191410.4A patent/EP3299437B1/de active Active
- 2004-08-18 CN CN2009101719891A patent/CN101654466B/zh active Active
-
2010
- 2010-10-11 US US12/901,610 patent/US9748498B2/en active Active
- 2010-10-14 US US12/904,290 patent/US8377740B2/en active Active
- 2010-10-15 US US12/905,112 patent/US8916853B2/en active Active
-
2014
- 2014-11-13 US US14/540,838 patent/US9024308B2/en active Active
-
2017
- 2017-07-31 US US15/663,900 patent/US10573828B2/en active Active
-
2020
- 2020-02-24 US US16/798,526 patent/US11539005B2/en active Active
-
2022
- 2022-12-02 US US18/061,111 patent/US20230108701A1/en active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| WO2001041512A1 (en) | 1999-12-01 | 2001-06-07 | The Trustees Of Princeton University | Complexes of form l2mx as phosphorescent dopants for organic leds |
| WO2002015645A1 (en) | 2000-08-11 | 2002-02-21 | The Trustees Of Princeton University | Organometallic compounds and emission-shifting organic electrophosphorescence |
Cited By (1348)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006018292A2 (de) * | 2004-08-18 | 2006-02-23 | Basf Aktiengesellschaft | In polymermatrices eingebettete übergansmetallcarbenkomplexe zur verwendung in oleds |
| WO2006018292A3 (de) * | 2004-08-18 | 2006-05-11 | Basf Ag | In polymermatrices eingebettete übergansmetallcarbenkomplexe zur verwendung in oleds |
| WO2006056418A2 (de) * | 2004-11-25 | 2006-06-01 | Basf Aktiengesellschaft | Verwendung von übergangsmetall-carbenkomplexen in organischen licht-emittierenden dioden (oleds) |
| US10522768B2 (en) | 2004-11-25 | 2019-12-31 | Udc Ireland Limited | Use of transition metal carbene complexes in organic light-emitting diodes (OLEDs) |
| WO2006056418A3 (de) * | 2004-11-25 | 2007-01-11 | Basf Ag | Verwendung von übergangsmetall-carbenkomplexen in organischen licht-emittierenden dioden (oleds) |
| US8492749B2 (en) | 2004-12-23 | 2013-07-23 | Basf Se | Electroluminescent metal complexes with nucleophilic carbene ligands |
| US9012899B2 (en) | 2004-12-23 | 2015-04-21 | Basf Se | Electroluminescent metal complexes with nucleophilic carbene ligands |
| JP2008525366A (ja) * | 2004-12-23 | 2008-07-17 | チバ ホールディング インコーポレーテッド | 求核性カルベン配位子を持つエレクトロルミネセント金属錯体 |
| WO2006067074A1 (en) * | 2004-12-23 | 2006-06-29 | Ciba Specialty Chemicals Holding Inc. | Electroluminescent metal complexes with nucleophilic carbene ligands |
| CN101087863B (zh) * | 2004-12-23 | 2012-06-20 | 西巴特殊化学品控股有限公司 | 具有亲核卡宾配体的电致发光金属络合物 |
| EP2080796A1 (de) * | 2004-12-23 | 2009-07-22 | Ciba Holding Inc. | Elektrolumineszente Metallkomplexe mit nukleophilen Carbenliganden |
| US9365767B2 (en) | 2005-02-21 | 2016-06-14 | Mitsubishi Chemical Corporation | Organic electric field light emitting element and production therefor |
| US9640769B2 (en) | 2005-02-21 | 2017-05-02 | Mitsubishi Chemical Corporation | Organic electric field light emitting element and production therefor |
| WO2006106842A1 (ja) * | 2005-03-31 | 2006-10-12 | Idemitsu Kosan Co., Ltd. | 遷移金属錯体化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| US9871219B2 (en) | 2005-04-13 | 2018-01-16 | Universal Display Corporation | Organic light emitting devices |
| US9647227B2 (en) | 2005-04-13 | 2017-05-09 | Universal Display Corporation | Organic light emitting devices |
| JP2007096259A (ja) * | 2005-04-25 | 2007-04-12 | Fujifilm Corp | 有機電界発光素子 |
| TWI418606B (zh) * | 2005-04-25 | 2013-12-11 | Udc Ireland Ltd | 有機電致發光裝置 |
| US8048538B2 (en) * | 2005-04-25 | 2011-11-01 | Fujifilm Corporation | Organic electroluminescent device |
| US9735377B2 (en) | 2005-05-06 | 2017-08-15 | Universal Display Corporation | Phosphorescent emitters and host materials with improved stability |
| CN100390185C (zh) * | 2005-05-11 | 2008-05-28 | 友达光电股份有限公司 | 发光材料及应用其的有机电激发光器件 |
| US7803948B2 (en) | 2005-06-14 | 2010-09-28 | Basf Aktiengesellschaft | Method for the isomerisation of transition metal complexes containing cyclometallated, carbene ligands |
| WO2006134113A1 (de) * | 2005-06-14 | 2006-12-21 | Basf Aktiengesellschaft | Verfahren zur isomerisierung cyclometallierter, carbenliganden enthaltender übergangsmetallkomplexe |
| JP2011256191A (ja) * | 2005-08-01 | 2011-12-22 | Mitsubishi Chemicals Corp | 遷移金属錯体の製造方法 |
| WO2007018067A1 (ja) * | 2005-08-05 | 2007-02-15 | Idemitsu Kosan Co., Ltd. | 遷移金属錯体化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP2007045742A (ja) * | 2005-08-10 | 2007-02-22 | Mitsubishi Chemicals Corp | 遷移金属錯体の製造方法及び遷移金属錯体 |
| EP1923930A4 (de) * | 2005-09-05 | 2012-03-21 | Idemitsu Kosan Co | Blaues licht emittierendes organisches elektrolumineszenzelement |
| EP1923930A1 (de) * | 2005-09-05 | 2008-05-21 | Idemitsu Kosan Co., Ltd. | Blaues licht emittierendes organisches elektrolumineszenzelement |
| KR101308282B1 (ko) * | 2005-09-05 | 2013-09-13 | 이데미쓰 고산 가부시키가이샤 | 청색 발광 유기 전계 발광 소자 |
| WO2007029426A1 (ja) | 2005-09-05 | 2007-03-15 | Idemitsu Kosan Co., Ltd. | 青色発光有機エレクトロルミネッセンス素子 |
| WO2007058255A1 (ja) * | 2005-11-17 | 2007-05-24 | Idemitsu Kosan Co., Ltd. | 遷移金属錯体化合物 |
| WO2007058104A1 (ja) * | 2005-11-17 | 2007-05-24 | Idemitsu Kosan Co., Ltd. | 金属錯体化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| US7501521B2 (en) | 2005-11-17 | 2009-03-10 | Idemitsu Kosan Co., Ltd. | Metal-complex compound and organic electroluminescence device using the compound |
| JPWO2007060826A1 (ja) * | 2005-11-24 | 2009-05-07 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP2013093593A (ja) * | 2005-12-15 | 2013-05-16 | Konica Minolta Inc | 有機エレクトロルミネッセンス素子、表示装置および照明装置 |
| WO2007069539A1 (ja) * | 2005-12-15 | 2007-06-21 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子、表示装置および照明装置 |
| JPWO2007069539A1 (ja) * | 2005-12-15 | 2009-05-21 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、表示装置および照明装置 |
| US8877937B2 (en) | 2006-01-31 | 2014-11-04 | Basf Se | Process for preparing transition metal-carbene complexes |
| EP2338593A1 (de) | 2006-01-31 | 2011-06-29 | Basf Se | Verfahren zur Herstellung von Übergangsmetall-Carbenkomplexen |
| US8410280B2 (en) | 2006-01-31 | 2013-04-02 | Basf Se | Process for preparing transition metal-carbene complexes |
| US10749121B2 (en) | 2006-02-10 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9893306B2 (en) | 2006-02-10 | 2018-02-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403831B2 (en) | 2006-02-10 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9065063B2 (en) | 2006-02-10 | 2015-06-23 | Universal Display Corporation | Metal complexes of cyclometallated imidazo[1,2-f]phenanthridine and diimidazo[1,2-a:1′,2′-c]quinazoline ligands and isoelectronic and benzannulated analogs thereof |
| US10978649B2 (en) | 2006-02-10 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10158090B2 (en) | 2006-02-10 | 2018-12-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8383828B2 (en) | 2006-04-04 | 2013-02-26 | Basf Aktiengesellschaft | Transition metal complexes comprising one noncarbene ligand and one or two carbene ligands and their use in OLEDs |
| US10385263B2 (en) | 2006-04-05 | 2019-08-20 | Udc Ireland Limited | Heteroleptic transition metal-carbene complexes and their use in organic light-emitting diodes (OLEDS) |
| KR101431844B1 (ko) | 2006-04-05 | 2014-08-25 | 바스프 에스이 | 이종 리간드 전이 금속-카르벤 착체 및 이의 유기 발광 다이오드(oled)에서의 용도 |
| US11692131B2 (en) | 2006-04-05 | 2023-07-04 | Udc Ireland Limited | Heteroleptic transition metal-carbene complexes and their use in organic light-emitting diodes |
| JP2009532431A (ja) * | 2006-04-05 | 2009-09-10 | ビーエーエスエフ ソシエタス・ヨーロピア | ヘテロレプティックな遷移金属−カルベン錯体及びそれを有機発光ダイオード(oled)において用いる使用 |
| JP2009542026A (ja) * | 2006-06-26 | 2009-11-26 | ビーエーエスエフ ソシエタス・ヨーロピア | 架橋カルベン配位子を有するPtとPdのビスカルベン錯体及びテトラカルベン錯体のOLED内での利用 |
| US8940904B2 (en) | 2006-06-26 | 2015-01-27 | Basf Se | Use of transition metal-carbene complexes which do not comprise any cyclometallation via non-carbenes in OLEDs |
| WO2008000727A1 (de) * | 2006-06-26 | 2008-01-03 | Basf Se | Verwendung von übergangsmetallcarbenkomplexen, die keine cyclometallierung über nicht-carbene enthalten, in oleds |
| US8247574B2 (en) | 2006-06-26 | 2012-08-21 | Basf Se | Use of PT -and PD-BIS- and tetra-carbon complexes with bridged carbon ligands in OLEDs |
| WO2008031743A1 (en) | 2006-09-14 | 2008-03-20 | Ciba Holding Inc. | Heterocyclic bridged biphenyls and their use in oleds |
| US10934262B2 (en) | 2006-09-14 | 2021-03-02 | Udc Ireland Limited | Heterocyclic bridged biphenyls |
| CN100465168C (zh) * | 2006-09-15 | 2009-03-04 | 华东理工大学 | 噁二唑衍生物及其在电致发光材料中应用 |
| EP3457452B1 (de) * | 2006-09-21 | 2022-11-02 | UDC Ireland Limited | Oled-anzeige mit verlängerter lebensdauer |
| WO2008034758A2 (de) * | 2006-09-21 | 2008-03-27 | Basf Se | Oled-anzeige mit verlängerter lebensdauer |
| EP3457452A2 (de) | 2006-09-21 | 2019-03-20 | UDC Ireland Limited | Oled-anzeige mit verlängerter lebensdauer |
| US8241764B2 (en) | 2006-09-21 | 2012-08-14 | Basf Aktiengesellschaft | OLED display with extended lifetime |
| EP3457452A3 (de) * | 2006-09-21 | 2019-03-27 | UDC Ireland Limited | Oled-anzeige mit verlängerter lebensdauer |
| KR101069302B1 (ko) | 2006-09-21 | 2011-10-05 | 바스프 에스이 | 수명이 연장된 oled 디스플레이 |
| WO2008034758A3 (de) * | 2006-09-21 | 2008-07-10 | Basf Se | Oled-anzeige mit verlängerter lebensdauer |
| US9899612B2 (en) | 2006-12-08 | 2018-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2008096609A1 (ja) * | 2007-02-05 | 2008-08-14 | Idemitsu Kosan Co., Ltd. | 遷移金属錯体化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2008108430A1 (ja) | 2007-03-07 | 2008-09-12 | Mitsubishi Chemical Corporation | 有機デバイス用組成物、高分子膜および有機電界発光素子 |
| EP3173456A1 (de) | 2007-03-07 | 2017-05-31 | Mitsubishi Chemical Corporation | Zusammensetzung zur verwendung in einer organischen vorrichtung, polymerfolie und organisches elektrolumineszentes element |
| US9911930B2 (en) | 2007-03-08 | 2018-03-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9142786B2 (en) | 2007-03-08 | 2015-09-22 | Universal Display Corporation | Phosphorescent materials |
| US9853227B2 (en) | 2007-03-08 | 2017-12-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10230060B2 (en) | 2007-03-08 | 2019-03-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9190621B2 (en) | 2007-03-08 | 2015-11-17 | Universal Display Corporation | Materials for organic light emitting diode |
| US10600975B2 (en) | 2007-03-08 | 2020-03-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495755B2 (en) | 2007-03-08 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3305871A1 (de) | 2007-05-18 | 2018-04-11 | UDC Ireland Limited | Deuterierte carbazole und ihre verwendung in organischen elektrolumineszenten vorrichtungen |
| EP1995292A1 (de) | 2007-05-18 | 2008-11-26 | FUJIFILM Corporation | Organische elektrolumineszente Vorrichtung |
| US8734962B2 (en) | 2007-05-21 | 2014-05-27 | Osram Opto Semiconductors Gmbh | Phosphorescent metal complex compound radiation emitting component comprising a phosphorescent metal complex compound and method for production of a phosphorescent metal complex compound |
| US9966544B2 (en) | 2007-05-21 | 2018-05-08 | Osram Oled Gmbh | Phosphorescent metal complex compound radiation emitting component comprising a phosphorescent metal complex compound and method for production of a phosphorescent metal complex compound |
| WO2009003898A1 (de) * | 2007-07-05 | 2009-01-08 | Basf Se | Organische leuchtdioden enthaltend carben-übergangsmetall-komplex-emitter und mindestens eine verbindung ausgewählt aus disilylcarbazolen; disilyldibenzofuranen, disilyldibenzothiophenen, disilyldibenzophospholen, disilyldibenzothiophen-s-oxiden und disilyldibenzothiophen-s,s-dioxiden |
| US8373159B2 (en) | 2007-07-05 | 2013-02-12 | Basf Se | Organic light-emitting diodes comprising carbene-transition metal complex emitter, and at least one compound selected from disilylcarbazoles, disilyldibenzofurans, disilyldibenzothiophenes, disilyldibenzophospholes, disilyldibenzothiophene s-oxides and disilyldibe |
| EP3345983A1 (de) | 2007-07-05 | 2018-07-11 | UDC Ireland Limited | Verbindungen enthaltend mindestens eine disilylverbindung ausgewählt aus disilylcarbazolen, disilyldibenzofuranen, disilyldibenzothiophenen, disilyldibenzophospholen, disilyldibenzothiophen-s-oxiden und disilyldibenzothiophen-s, s-dioxiden |
| US8697255B2 (en) | 2007-07-05 | 2014-04-15 | Basf Se | Organic light-emitting diodes comprising at least one disilyl compound selected from disilylcarbazoles, disilyldibenzofurans, disilyldibenzothiophenes, disilyldibenzopholes, disilyldibenzothiophene S-oxides and disilyldibenzothiophene S,S-dioxides |
| KR101577465B1 (ko) | 2007-07-05 | 2015-12-14 | 바스프 에스이 | 카르벤 전이 금속 착체 이미터, 및 디실릴카르바졸, 디실릴디벤조푸란, 디실릴디벤조티오펜, 디실릴디벤조포스폴, 디실릴디벤조티오펜 s-옥사이드 및 디실릴디벤조티오펜 s,s-디옥사이드로부터 선택된 1종 이상의 화합물을 포함하는 유기 발광 다이오드 |
| US11690286B2 (en) | 2007-08-08 | 2023-06-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10312450B2 (en) | 2007-08-08 | 2019-06-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10957858B2 (en) | 2007-08-08 | 2021-03-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9997727B2 (en) | 2007-08-08 | 2018-06-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8822708B2 (en) | 2007-08-08 | 2014-09-02 | Universal Display Corporation | Benzo-fused thiophene / triphenylene hybrid materials |
| US10374171B2 (en) | 2007-08-08 | 2019-08-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9608206B2 (en) | 2007-08-08 | 2017-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP2031037A1 (de) | 2007-08-29 | 2009-03-04 | Fujifilm Corporation | Organische Elektrolumineszenzvorrichtung |
| JP2009057505A (ja) * | 2007-09-03 | 2009-03-19 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| EP2036907A1 (de) | 2007-09-14 | 2009-03-18 | FUJIFILM Corporation | Organische Elektrolumineszenzvorrichtung |
| WO2009037155A1 (en) | 2007-09-20 | 2009-03-26 | Basf Se | Electroluminescent device |
| EP2042508A1 (de) | 2007-09-25 | 2009-04-01 | FUJIFILM Corporation | Organische Elektrolumineszenzvorrichtung |
| US9379338B1 (en) | 2007-09-25 | 2016-06-28 | Universal Display Corporation | Organic electroluminescence device |
| US9139764B2 (en) | 2007-09-28 | 2015-09-22 | Osram Opto Semiconductors Gmbh | Organic radiation-emitting component |
| DE102007046445A1 (de) | 2007-09-28 | 2009-04-16 | Osram Opto Semiconductors Gmbh | Organisches selbstemittierendes Bauteil |
| US8384068B2 (en) | 2007-10-02 | 2013-02-26 | Basf Se | Use of acridine derivatives as matrix materials and/or electron blockers in OLEDs |
| US8383249B2 (en) * | 2007-10-04 | 2013-02-26 | Universal Display Corporation | Complexes with tridentate ligands |
| US8067100B2 (en) * | 2007-10-04 | 2011-11-29 | Universal Display Corporation | Complexes with tridentate ligands |
| US8258297B2 (en) | 2007-10-17 | 2012-09-04 | Basf Se | Transition metal complexes with bridged carbene ligands and use thereof in OLEDs |
| US8728632B2 (en) | 2007-10-17 | 2014-05-20 | Basf Se | Metal complexes comprising bridged carbene ligands and use thereof in OLEDs |
| EP2061087A2 (de) | 2007-11-15 | 2009-05-20 | FUJIFILM Corporation | Dünnschicht-Feldeffekttransistor und Anzeige unter Benutzung desselben |
| EP2061086A2 (de) | 2007-11-15 | 2009-05-20 | FUJIFILM Corporation | Dünnschicht-Feldeffekttransistor und Anzeige unter Benutzung desselben |
| EP2070936A1 (de) | 2007-12-14 | 2009-06-17 | Fujifilm Corporation | Platinkomplexverbindungen und organische Elektrolumineszenzvorrichtung dafür |
| US9997726B2 (en) | 2007-12-28 | 2018-06-12 | Universal Display Corporation | Dibenzothiophene-containing materials in phosphorescent light emitting diodes |
| WO2009100991A1 (en) | 2008-02-12 | 2009-08-20 | Basf Se | Electroluminescent metal complexes with dibenzo[f,h]quinoxalines |
| EP2096690A2 (de) | 2008-02-28 | 2009-09-02 | FUJIFILM Corporation | Organische Elektrolumineszenzvorrichtung |
| EP2105967A1 (de) | 2008-03-24 | 2009-09-30 | FUJIFILM Corporation | Dünnschicht-Feldeffekttransistor und Anzeige |
| EP2112213A2 (de) | 2008-04-22 | 2009-10-28 | FUJIFILM Corporation | Organische Elektrolumineszenzvorrichtung, neue Platinkomplexverbindung und neue Verbindung, die als Ligand dafür geeignet ist |
| EP2113548A1 (de) | 2008-04-24 | 2009-11-04 | FUJIFILM Corporation | Organische Elektrolumineszenzvorrichtung |
| EP3081618A1 (de) | 2008-04-24 | 2016-10-19 | UDC Ireland Limited | Organische elektrolumineszenzvorrichtung |
| US10214525B2 (en) | 2008-06-06 | 2019-02-26 | Basf Se | Chlorinated napthalenetetracarboxylic acid derivatives, preparation thereof and use thereof in organic electronics |
| WO2009147237A1 (en) | 2008-06-06 | 2009-12-10 | Basf Se | Chlorinated naphthalenetetracarboxylic acid derivatives, preparation thereof and use thereof in organic electronics |
| US9512354B2 (en) | 2008-06-06 | 2016-12-06 | Basf Se | Chlorinated naphthalenetetracarboxylic acid derivatives, preparation thereof and use thereof in organic electronics |
| US8377332B2 (en) | 2008-06-10 | 2013-02-19 | Basf Se | Transition metal complexes and use thereof in organic light emitting diodes—III |
| US8410270B2 (en) | 2008-06-10 | 2013-04-02 | Basf Se | Transition metal complexes and use thereof in organic light-emitting diodes V |
| US8592586B2 (en) | 2008-06-10 | 2013-11-26 | Basf Se | Transition metal complexes and use thereof in organic light-emitting diodes V |
| US8859110B2 (en) | 2008-06-20 | 2014-10-14 | Basf Se | Cyclic phosphazene compounds and use thereof in organic light emitting diodes |
| US8440326B2 (en) | 2008-06-30 | 2013-05-14 | Universal Display Corporation | Hole transport materials containing triphenylene |
| US9012038B2 (en) | 2008-07-18 | 2015-04-21 | Osram Gmbh | Phosphorescent metal complex compound, method for the preparation thereof and radiating component |
| WO2010007107A1 (de) | 2008-07-18 | 2010-01-21 | Siemens Aktiengesellschaft | Phosphoreszente metallkomplexverbindung, verfahren zur herstellung dazu und strahlungsemittierendes bauelement |
| DE102008033929A1 (de) | 2008-07-18 | 2010-01-21 | Siemens Aktiengesellschaft | Phosphoreszente Metallkomplexverbindung, Verfahren zur Herstellung dazu und strahlungsemittierendes Bauelement |
| US9076973B2 (en) | 2008-09-03 | 2015-07-07 | Universal Display Corporation | Phosphorescent materials |
| US10186672B2 (en) | 2008-09-03 | 2019-01-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10892426B2 (en) | 2008-09-03 | 2021-01-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10593896B2 (en) | 2008-09-03 | 2020-03-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11482685B2 (en) | 2008-09-03 | 2022-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9630983B2 (en) | 2008-09-03 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent material and devices |
| US10084143B2 (en) | 2008-09-16 | 2018-09-25 | Universal Display Corporation | Phosphorescent materials |
| US8618533B2 (en) | 2008-10-07 | 2013-12-31 | Osram Opto Semiconductors Gmbh | Siloles substituted by fused ring systems and use thereof in organic electronics |
| US8865321B2 (en) | 2008-11-11 | 2014-10-21 | Merck Patent Gmbh | Organic electroluminescent devices |
| DE102008056688A1 (de) | 2008-11-11 | 2010-05-12 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| US8367223B2 (en) | 2008-11-11 | 2013-02-05 | Universal Display Corporation | Heteroleptic phosphorescent emitters |
| US10008678B2 (en) | 2008-12-12 | 2018-06-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8952363B2 (en) | 2009-01-16 | 2015-02-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9067947B2 (en) | 2009-01-16 | 2015-06-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9831442B2 (en) | 2009-01-16 | 2017-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2010083871A1 (de) | 2009-01-20 | 2010-07-29 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| US9034485B2 (en) | 2009-01-20 | 2015-05-19 | Merck Patent Gmbh | Compounds for electronic devices |
| EP2214223A2 (de) | 2009-02-03 | 2010-08-04 | Fujifilm Corporation | Organische Elektrolumineszenzanzeigevorrichtung |
| WO2010093062A1 (en) | 2009-02-13 | 2010-08-19 | Fujifilm Corporation | Organic electroluminescence device, and method for producing the same |
| WO2010097433A1 (de) | 2009-02-26 | 2010-09-02 | Basf Se | Chinonverbindungen als dotierstoff in der organischen elektronik |
| WO2010101011A1 (en) | 2009-03-03 | 2010-09-10 | Fujifilm Corporation | Method for producing light-emitting display device, light-emitting display device and light-emitting display |
| EP2226867A2 (de) | 2009-03-05 | 2010-09-08 | Fujifilm Corporation | Organische Elektrolumineszenzvorrichtung |
| US11910700B2 (en) | 2009-03-23 | 2024-02-20 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US11380854B2 (en) | 2009-03-23 | 2022-07-05 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US11637251B2 (en) | 2009-03-23 | 2023-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10312458B2 (en) | 2009-03-23 | 2019-06-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11910701B2 (en) | 2009-03-23 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10374173B2 (en) | 2009-04-28 | 2019-08-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9634265B2 (en) | 2009-04-28 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9673406B2 (en) | 2009-05-20 | 2017-06-06 | Universal Display Corporation | Metal complexes with boron-nitrogen heterocycle containing ligands |
| DE102009022858A1 (de) | 2009-05-27 | 2011-12-15 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| CN102482574A (zh) * | 2009-06-18 | 2012-05-30 | 巴斯夫欧洲公司 | 用作场致发光器件的空穴传输材料的菲并唑化合物 |
| DE102009031021A1 (de) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011000455A1 (de) | 2009-06-30 | 2011-01-06 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102009031683A1 (de) | 2009-07-03 | 2011-03-24 | Siemens Aktiengesellschaft | Phophoreszente Metallkomplexverbindung, Verfahren zur Herstellung dazu und strahlungsemittierendes Bauelement |
| DE102009032922A1 (de) | 2009-07-14 | 2011-01-20 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011006574A1 (de) | 2009-07-14 | 2011-01-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2011013626A1 (ja) | 2009-07-31 | 2011-02-03 | 富士フイルム株式会社 | 有機デバイス用蒸着材料及び有機デバイスの製造方法 |
| WO2011024922A1 (ja) | 2009-08-27 | 2011-03-03 | 三菱化学株式会社 | モノアミン化合物、電荷輸送材料、電荷輸送膜用組成物、有機電界発光素子、有機el表示装置及び有機el照明 |
| WO2011024976A1 (ja) | 2009-08-31 | 2011-03-03 | 富士フイルム株式会社 | 有機電界発光素子 |
| WO2011030620A1 (en) | 2009-09-09 | 2011-03-17 | Fujifilm Corporation | Organic el device optical member and organic el device |
| WO2011030882A1 (en) | 2009-09-14 | 2011-03-17 | Fujifilm Corporation | Color filter and light-emitting display element |
| WO2011030883A1 (en) | 2009-09-14 | 2011-03-17 | Fujifilm Corporation | Color filter and light-emitting display element |
| WO2011042107A2 (de) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102009048791A1 (de) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| US9108998B2 (en) | 2009-10-14 | 2015-08-18 | Basf Se | Dinuclear platinum-carbene complexes and the use thereof in OLEDs |
| US11871654B2 (en) | 2009-10-28 | 2024-01-09 | Udc Ireland Limited | Heteroleptic carbene complexes and the use thereof in organic electronics |
| US11189806B2 (en) | 2009-10-28 | 2021-11-30 | Udc Ireland Limited | Heteroleptic carbene complexes and the use thereof in organic electronics |
| WO2011051404A1 (de) | 2009-10-28 | 2011-05-05 | Basf Se | Heteroleptische carben-komplexe und deren verwendung in der organischen elektronik |
| US8545996B2 (en) | 2009-11-02 | 2013-10-01 | The University Of Southern California | Ion-pairing soft salts based on organometallic complexes and their applications in organic light emitting diodes |
| WO2011057701A1 (de) | 2009-11-10 | 2011-05-19 | Merck Patent Gmbh | Organische verbindungen für elektroluminiszenz vorrichtungen |
| DE102009052428A1 (de) | 2009-11-10 | 2011-05-12 | Merck Patent Gmbh | Verbindung für elektronische Vorrichtungen |
| WO2011057706A2 (de) | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| DE102009053382A1 (de) | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| WO2011060859A1 (de) | 2009-11-17 | 2011-05-26 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102009053644A1 (de) | 2009-11-17 | 2011-05-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009053644B4 (de) | 2009-11-17 | 2019-07-04 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011060867A1 (de) | 2009-11-18 | 2011-05-26 | Merck Patent Gmbh | Stickstoffhaltige kondensierte heterozyklen für oleds |
| DE102009053836A1 (de) | 2009-11-18 | 2011-05-26 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| US9773986B2 (en) | 2009-11-19 | 2017-09-26 | The University Of Southern California | Copper(I)-carbene complexes and organic electroluminescent devices |
| KR101822668B1 (ko) | 2009-11-19 | 2018-01-26 | 유니버시티 오브 써던 캘리포니아 | 3-배위 구리(i)-카르벤 착체 |
| WO2011063083A1 (en) | 2009-11-19 | 2011-05-26 | The University Of Southern California | 3-coordinate copper (i) - carbene complexes |
| US8580394B2 (en) | 2009-11-19 | 2013-11-12 | Universal Display Corporation | 3-coordinate copper(I)-carbene complexes |
| EP2501707A1 (de) * | 2009-11-19 | 2012-09-26 | The University Of Southern California | 3-koordinatige kupfer (i)-carben-komplexe |
| EP2501707A4 (de) * | 2009-11-19 | 2014-03-26 | Univ Southern California | 3-koordinatige kupfer (i)-carben-komplexe |
| US10090476B2 (en) | 2009-12-14 | 2018-10-02 | Udc Ireland Limited | Metal complexes comprising diazabenzmidazolocarbene ligands and the use thereof in OLEDs |
| WO2011073149A1 (de) | 2009-12-14 | 2011-06-23 | Basf Se | Metallkomplexe, enthaltend diazabenzimidazolcarben-liganden und deren verwendung in oleds |
| US11839140B2 (en) | 2009-12-14 | 2023-12-05 | Udc Ireland Limited | Metal complexes comprising diazabenzmidazolocarbene ligands and the use thereof in OLEDS |
| US11444254B2 (en) | 2009-12-14 | 2022-09-13 | Udc Ireland Limited | Metal complexes comprising diazabenzmidazolocarbene ligands and the use thereof in OLEDs |
| US9487548B2 (en) | 2009-12-14 | 2016-11-08 | Udc Ireland Limited | Metal complexes comprising diazabenzimidazolocarbene ligands and the use thereof in OLEDs |
| US10916716B2 (en) | 2009-12-14 | 2021-02-09 | Udc Ireland Limited | Metal complexes comprising diazabenzmidazolocarbene ligands and the use thereof in OLEDS |
| WO2011085781A1 (de) | 2010-01-16 | 2011-07-21 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102010004803A1 (de) | 2010-01-16 | 2011-07-21 | Merck Patent GmbH, 64293 | Materialien für organische Elektrolumineszenzvorrichtungen |
| US9169434B2 (en) | 2010-01-25 | 2015-10-27 | Osram Ag | Phosphorescent metal complex, process for production and light-emitting component |
| WO2011088918A1 (de) | 2010-01-25 | 2011-07-28 | Siemens Aktiengesellschaft | Verwendung des guanidinium-kations in einem lichtemittierenden bauelement |
| DE102010005697A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent GmbH, 64293 | Verbindungen für elektronische Vorrichtungen |
| DE102010005634A1 (de) | 2010-01-25 | 2011-07-28 | Siemens Aktiengesellschaft, 80333 | Neuartige Verwendung des Guanidinium-Kations und lichtemittierendes Bauelement |
| WO2011088877A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| US9375392B2 (en) | 2010-01-25 | 2016-06-28 | Osram Ag | Use of the guanidinium cation and light-emitting component |
| DE102010005632A1 (de) | 2010-01-25 | 2011-07-28 | Siemens Aktiengesellschaft, 80333 | Phosphoreszente Metallkomplexverbindung, Verfahren zur Herstellung und lichtemittierendes Bauelement |
| DE102010009903A1 (de) | 2010-03-02 | 2011-09-08 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| WO2011107186A2 (de) | 2010-03-02 | 2011-09-09 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| US9175211B2 (en) | 2010-03-03 | 2015-11-03 | Universal Display Corporation | Phosphorescent materials |
| WO2011115075A1 (ja) | 2010-03-15 | 2011-09-22 | 三菱化学株式会社 | 有機電界発光素子及びその製造方法、有機el表示装置、有機el照明、並びに有機電界発光素子の製造装置 |
| WO2011116865A1 (de) | 2010-03-25 | 2011-09-29 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102010012738A1 (de) | 2010-03-25 | 2011-09-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011116869A1 (de) | 2010-03-26 | 2011-09-29 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102010013068A1 (de) | 2010-03-26 | 2011-09-29 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| US8637857B2 (en) | 2010-04-06 | 2014-01-28 | Basf Se | Substituted carbazole derivatives and use thereof in organic electronics |
| WO2011126095A1 (ja) | 2010-04-09 | 2011-10-13 | 三菱化学株式会社 | 有機電界発光素子用組成物の製造方法、有機電界発光素子用組成物、有機電界発光素子の製造方法、有機電界発光素子、有機el表示装置および有機el照明 |
| WO2011128017A1 (de) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Überbrückte triarylamine und -phosphine als materialien für elektronische vorrichtungen |
| DE102010014933A1 (de) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| US8691401B2 (en) | 2010-04-16 | 2014-04-08 | Basf Se | Bridged benzimidazole-carbene complexes and use thereof in OLEDS |
| DE102010018321A1 (de) | 2010-04-27 | 2011-10-27 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| WO2011134577A1 (de) | 2010-04-27 | 2011-11-03 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| US9040962B2 (en) | 2010-04-28 | 2015-05-26 | Universal Display Corporation | Depositing premixed materials |
| US8968887B2 (en) | 2010-04-28 | 2015-03-03 | Universal Display Corporation | Triphenylene-benzofuran/benzothiophene/benzoselenophene compounds with substituents joining to form fused rings |
| DE102010019306A1 (de) | 2010-05-04 | 2011-11-10 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| WO2011137951A1 (de) | 2010-05-04 | 2011-11-10 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| US9140428B2 (en) | 2010-06-11 | 2015-09-22 | Universal Display Corporation | Triplet-triplet annihilation up-conversation for display and lighting applications |
| US8742657B2 (en) | 2010-06-11 | 2014-06-03 | Universal Display Corporation | Triplet-Triplet annihilation up conversion (TTA-UC) for display and lighting applications |
| US9543532B2 (en) | 2010-06-11 | 2017-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9142792B2 (en) | 2010-06-18 | 2015-09-22 | Basf Se | Organic electronic devices comprising a layer comprising at least one metal organic compound and at least one metal oxide |
| WO2011157346A1 (de) | 2010-06-18 | 2011-12-22 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2011157779A1 (en) | 2010-06-18 | 2011-12-22 | Basf Se | Organic electronic devices comprising a layer of a pyridine compound and a 8-hydroxyquinolinolato earth alkaline metal, or alkali metal complex |
| WO2011157790A1 (en) | 2010-06-18 | 2011-12-22 | Basf Se | Organic electronic devices comprising a layer of a dibenzofurane compound and a 8-hydroxyquinolinolato earth alkaline metal, or alkali metal complex |
| DE102010024335A1 (de) | 2010-06-18 | 2011-12-22 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| WO2011160757A1 (de) | 2010-06-22 | 2011-12-29 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| DE102010024542A1 (de) | 2010-06-22 | 2011-12-22 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102010024897A1 (de) | 2010-06-24 | 2011-12-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011160758A1 (de) | 2010-06-24 | 2011-12-29 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2012005329A1 (ja) | 2010-07-08 | 2012-01-12 | 三菱化学株式会社 | 有機電界発光素子、有機電界発光デバイス、有機el表示装置及び有機el照明 |
| US9435021B2 (en) | 2010-07-29 | 2016-09-06 | University Of Southern California | Co-deposition methods for the fabrication of organic optoelectronic devices |
| WO2012016630A1 (de) | 2010-08-05 | 2012-02-09 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| DE102010033548A1 (de) | 2010-08-05 | 2012-02-09 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| US11316113B2 (en) | 2010-08-20 | 2022-04-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11289659B2 (en) | 2010-08-20 | 2022-03-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9954180B2 (en) | 2010-08-20 | 2018-04-24 | Universal Display Corporation | Bicarbazole compounds for OLEDs |
| WO2012034627A1 (de) | 2010-09-15 | 2012-03-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102010045405A1 (de) | 2010-09-15 | 2012-03-15 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| US9310766B2 (en) | 2010-09-29 | 2016-04-12 | Basf Se | Security element |
| WO2012041851A1 (en) | 2010-09-29 | 2012-04-05 | Basf Se | Security element |
| US9079872B2 (en) | 2010-10-07 | 2015-07-14 | Basf Se | Phenanthro[9, 10-B]furans for electronic applications |
| WO2012045710A1 (en) | 2010-10-07 | 2012-04-12 | Basf Se | Phenanthro[9,10-b]furans for electronic applications |
| US8932734B2 (en) | 2010-10-08 | 2015-01-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9401482B2 (en) | 2010-10-08 | 2016-07-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2012045384A1 (de) | 2010-10-09 | 2012-04-12 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| DE102010048074A1 (de) | 2010-10-09 | 2012-04-12 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| WO2012048781A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Materialien auf basis von triphenylen für organische elektrolumineszenzvorrichtungen |
| DE102010048608A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010048607A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| WO2012048780A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| US8269317B2 (en) | 2010-11-11 | 2012-09-18 | Universal Display Corporation | Phosphorescent materials |
| WO2012069121A1 (de) | 2010-11-24 | 2012-05-31 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US9029541B2 (en) | 2010-12-02 | 2015-05-12 | Ube Industries, Ltd. | Binuclear metal complex, and organic electroluminescence element comprising same |
| WO2012074111A1 (ja) | 2010-12-02 | 2012-06-07 | 宇部興産株式会社 | 二核金属錯体、及びそれを用いた有機エレクトロルミネッセンス素子 |
| US10147892B2 (en) | 2010-12-07 | 2018-12-04 | The University Of Southern California | Organic electroluminescent materials and devices |
| WO2012079678A1 (de) | 2010-12-13 | 2012-06-21 | Merck Patent Gmbh | Substituierte tetraarylbenzole |
| DE102010054316A1 (de) | 2010-12-13 | 2012-06-14 | Merck Patent Gmbh | Substituierte Tetraarylbenzole |
| US8362246B2 (en) | 2010-12-13 | 2013-01-29 | Basf Se | Bispyrimidines for electronic applications |
| WO2012080052A1 (en) | 2010-12-13 | 2012-06-21 | Basf Se | Bispyrimidines for electronic applications |
| US10008677B2 (en) | 2011-01-13 | 2018-06-26 | Universal Display Corporation | Materials for organic light emitting diode |
| US11374180B2 (en) | 2011-01-13 | 2022-06-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680189B2 (en) | 2011-01-13 | 2020-06-09 | Universal Display Corporation | Materials for organic light emitting diodes |
| WO2012096352A1 (ja) | 2011-01-14 | 2012-07-19 | 三菱化学株式会社 | 有機電界発光素子、有機電界発光素子用組成物、及び有機電界発光装置 |
| DE102012000064A1 (de) | 2011-01-21 | 2012-07-26 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| US8415031B2 (en) | 2011-01-24 | 2013-04-09 | Universal Display Corporation | Electron transporting compounds |
| EP2482159A2 (de) | 2011-01-28 | 2012-08-01 | Honeywell International, Inc. | Verfahren und umkonfigurierbare System zur Optimierung der Leistung eines zustandsabhängigen Wartungssystems |
| DE102011010841A1 (de) | 2011-02-10 | 2012-08-16 | Merck Patent Gmbh | (1,3)-Dioxan-5-on-Verbindungen |
| WO2012107158A1 (de) | 2011-02-10 | 2012-08-16 | Merck Patent Gmbh | 1,3 - dioxan-5-on-verbindungen |
| DE102011011104A1 (de) | 2011-02-12 | 2012-08-16 | Merck Patent Gmbh | Substituierte Dibenzonaphtacene |
| WO2012107163A1 (de) | 2011-02-12 | 2012-08-16 | Merck Patent Gmbh | Substituierte dibenzonaphtacene |
| WO2012110182A1 (de) | 2011-02-17 | 2012-08-23 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102011011539A1 (de) | 2011-02-17 | 2012-08-23 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| US8748011B2 (en) | 2011-02-23 | 2014-06-10 | Universal Display Corporation | Ruthenium carbene complexes for OLED material |
| US10381580B2 (en) | 2011-02-23 | 2019-08-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| TWI567080B (zh) * | 2011-02-23 | 2017-01-21 | 環球展覽公司 | 用於有機發光裝置材料之釕碳烯錯合物 |
| US9947880B2 (en) | 2011-02-23 | 2018-04-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2012116240A1 (en) * | 2011-02-23 | 2012-08-30 | Universal Display Corporation | Ruthenium carbene complexes for oled material |
| US9005772B2 (en) | 2011-02-23 | 2015-04-14 | Universal Display Corporation | Thioazole and oxazole carbene metal complexes as phosphorescent OLED materials |
| US10388890B2 (en) | 2011-02-23 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent heterocyclic carbene metal complexes and devices containing the same |
| US8563737B2 (en) | 2011-02-23 | 2013-10-22 | Universal Display Corporation | Methods of making bis-tridentate carbene complexes of ruthenium and osmium |
| US8754232B2 (en) | 2011-02-23 | 2014-06-17 | Universal Display Corporation | Methods of making bis-tridentate carbene complexes of ruthenium and osmium |
| US8492006B2 (en) | 2011-02-24 | 2013-07-23 | Universal Display Corporation | Germanium-containing red emitter materials for organic light emitting diode |
| US9673405B2 (en) | 2011-03-01 | 2017-06-06 | Konica Minolta Holdings, Inc. | Organic electroluminescent device, display apparatus, and lighting apparatus |
| US10873038B2 (en) | 2011-03-08 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11600791B2 (en) | 2011-03-08 | 2023-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8883322B2 (en) | 2011-03-08 | 2014-11-11 | Universal Display Corporation | Pyridyl carbene phosphorescent emitters |
| US9972793B2 (en) | 2011-03-08 | 2018-05-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2012130709A1 (en) | 2011-03-25 | 2012-10-04 | Basf Se | 4h-imidazo[1,2-a]imidazoles for electronic applications |
| US10431750B2 (en) | 2011-03-25 | 2019-10-01 | Udc Ireland Limited | 4H-imidazo[1,2-a]imidazoles for electronic applications |
| EP3640252A1 (de) | 2011-03-25 | 2020-04-22 | UDC Ireland Limited | 4h-imidazo[1,2-a]imidazole für elektronische anwendungen |
| US11450812B2 (en) | 2011-03-25 | 2022-09-20 | Udc Ireland Limited | 4H-imidazo[1,2-a]imidazoles for electronic applications |
| US9806270B2 (en) | 2011-03-25 | 2017-10-31 | Udc Ireland Limited | 4H-imidazo[1,2-a]imidazoles for electronic applications |
| EP3034508A1 (de) | 2011-03-25 | 2016-06-22 | Basf Se | 4h-imidazo[1,2-a]imidazole für elektronische anwendungen |
| WO2012139692A1 (de) | 2011-04-13 | 2012-10-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2012139693A1 (de) | 2011-04-13 | 2012-10-18 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012143080A2 (de) | 2011-04-18 | 2012-10-26 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2012143079A1 (de) | 2011-04-18 | 2012-10-26 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012149992A1 (de) | 2011-05-04 | 2012-11-08 | Merck Patent Gmbh | Vorrichtung zur aufbewahrung von frischwaren |
| WO2012150001A1 (de) | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012149999A1 (de) | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| US9397312B2 (en) | 2011-05-11 | 2016-07-19 | Universal Display Corporation | Process for fabricating metal bus lines for OLED lighting panels |
| US8927308B2 (en) | 2011-05-12 | 2015-01-06 | Universal Display Corporation | Method of forming bus line designs for large-area OLED lighting |
| US9450027B2 (en) | 2011-05-12 | 2016-09-20 | Universal Display Corporation | Method of forming bus line designs for large-area OLED lighting |
| US9212197B2 (en) | 2011-05-19 | 2015-12-15 | Universal Display Corporation | Phosphorescent heteroleptic phenylbenzimidazole dopants |
| US8795850B2 (en) | 2011-05-19 | 2014-08-05 | Universal Display Corporation | Phosphorescent heteroleptic phenylbenzimidazole dopants and new synthetic methodology |
| US9257658B2 (en) | 2011-05-19 | 2016-02-09 | Universal Display Corporation | Method of making organic electroluminescent materials |
| US8748012B2 (en) | 2011-05-25 | 2014-06-10 | Universal Display Corporation | Host materials for OLED |
| DE112012002237B4 (de) | 2011-05-25 | 2022-12-22 | Universal Display Corporation | Host Materialien für OLEDS |
| US11189805B2 (en) | 2011-05-27 | 2021-11-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10158089B2 (en) | 2011-05-27 | 2018-12-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10079349B2 (en) | 2011-05-27 | 2018-09-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2012163465A1 (de) | 2011-06-03 | 2012-12-06 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| US11063229B2 (en) | 2011-06-08 | 2021-07-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9847495B2 (en) | 2011-06-08 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9812656B2 (en) | 2011-06-08 | 2017-11-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10978648B2 (en) | 2011-06-08 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9755164B2 (en) | 2011-06-08 | 2017-09-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10297769B2 (en) | 2011-06-08 | 2019-05-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3415521A1 (de) | 2011-06-14 | 2018-12-19 | UDC Ireland Limited | Metallkomplexe mit azabenzimidazolcarbenliganden und verwendung davon in oleds |
| US9315724B2 (en) | 2011-06-14 | 2016-04-19 | Basf Se | Metal complexes comprising azabenzimidazole carbene ligands and the use thereof in OLEDs |
| US11751455B2 (en) | 2011-06-17 | 2023-09-05 | Universal Display Corporation | Non-common capping layer on an organic device |
| US10340313B2 (en) | 2011-06-17 | 2019-07-02 | Universal Display Corporation | Non-common capping layer on an organic device |
| US8884316B2 (en) | 2011-06-17 | 2014-11-11 | Universal Display Corporation | Non-common capping layer on an organic device |
| US8659036B2 (en) | 2011-06-17 | 2014-02-25 | Universal Display Corporation | Fine tuning of emission spectra by combination of multiple emitter spectra |
| US9054343B2 (en) | 2011-06-17 | 2015-06-09 | Universal Display Corporation | Fine tuning of emission spectra by combination of multiple emitter spectra |
| US9397310B2 (en) | 2011-07-14 | 2016-07-19 | Universal Display Corporation | Organice electroluminescent materials and devices |
| US9647221B2 (en) | 2011-07-14 | 2017-05-09 | Universal Display Corporation | Organic light-emitting devices |
| US9252377B2 (en) | 2011-07-14 | 2016-02-02 | Universal Display Corporation | Inorganic hosts in OLEDs |
| US9783564B2 (en) | 2011-07-25 | 2017-10-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10214551B2 (en) | 2011-07-25 | 2019-02-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8709615B2 (en) | 2011-07-28 | 2014-04-29 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US8409729B2 (en) | 2011-07-28 | 2013-04-02 | Universal Display Corporation | Host materials for phosphorescent OLEDs |
| WO2013017189A1 (de) | 2011-07-29 | 2013-02-07 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| EP3439065A1 (de) | 2011-08-03 | 2019-02-06 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2013017192A1 (de) | 2011-08-03 | 2013-02-07 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US9313857B2 (en) | 2011-08-04 | 2016-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2013041176A1 (de) | 2011-09-21 | 2013-03-28 | Merck Patent Gmbh | Carbazolderivate für organische elektrolumineszenzvorrichtungen |
| WO2013108069A2 (ja) | 2011-10-06 | 2013-07-25 | ユーディーシー アイルランド リミテッド | 有機電界発光素子とそれに用いることができる化合物および有機電界発光素子用材料、並びに該素子を用いた発光装置、表示装置及び照明装置 |
| WO2013050862A1 (ja) | 2011-10-07 | 2013-04-11 | ユーディーシー アイルランド リミテッド | 有機電界発光素子及び該素子用発光材料並びに発光装置、表示装置及び照明装置 |
| DE102011116165A1 (de) | 2011-10-14 | 2013-04-18 | Merck Patent Gmbh | Benzodioxepin-3-on-Verbindungen |
| WO2013056776A1 (de) | 2011-10-20 | 2013-04-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2013060418A1 (en) | 2011-10-27 | 2013-05-02 | Merck Patent Gmbh | Materials for electronic devices |
| WO2013064206A1 (de) | 2011-11-01 | 2013-05-10 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2013064881A2 (ja) | 2011-11-02 | 2013-05-10 | ユーディーシー アイルランド リミテッド | 有機電界発光素子、有機電界発光素子用材料並びに該有機電界発光素子を用いた発光装置、表示装置及び照明装置 |
| US9502664B2 (en) | 2011-11-10 | 2016-11-22 | Udc Ireland Limited | 4H-imidazo[1,2-a]imidazoles for electronic applications |
| WO2013068376A1 (en) | 2011-11-10 | 2013-05-16 | Basf Se | 4h-imidazo[1,2-a]imidazoles for electronic applications |
| WO2013069338A1 (ja) | 2011-11-11 | 2013-05-16 | 三菱化学株式会社 | 有機電界発光素子及び有機電界発光デバイス |
| US9142788B2 (en) | 2011-11-14 | 2015-09-22 | Universal Display Corporation | Host materials for OLEDs |
| US8652656B2 (en) | 2011-11-14 | 2014-02-18 | Universal Display Corporation | Triphenylene silane hosts |
| US9193745B2 (en) | 2011-11-15 | 2015-11-24 | Universal Display Corporation | Heteroleptic iridium complex |
| WO2013083216A1 (de) | 2011-11-17 | 2013-06-13 | Merck Patent Gmbh | Spiro -dihydroacridinderivate und ihre verwendung als materialien für organische elektrolumineszenzvorrichtungen |
| WO2013080798A1 (ja) | 2011-11-30 | 2013-06-06 | 富士フイルム株式会社 | 光拡散性転写材料、光拡散層の形成方法、有機電界発光装置、及び有機電界発光装置の製造方法 |
| US10454046B2 (en) | 2011-12-09 | 2019-10-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11482684B2 (en) | 2011-12-09 | 2022-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2013087142A1 (de) | 2011-12-12 | 2013-06-20 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102012022880A1 (de) | 2011-12-22 | 2013-06-27 | Merck Patent Gmbh | Elektronische Vorrichtungen enthaltend organische Schichten |
| US8987451B2 (en) | 2012-01-03 | 2015-03-24 | Universal Display Corporation | Synthesis of cyclometallated platinum(II) complexes |
| US9461254B2 (en) | 2012-01-03 | 2016-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9163174B2 (en) | 2012-01-04 | 2015-10-20 | Universal Display Corporation | Highly efficient phosphorescent materials |
| DE102013200085B4 (de) | 2012-01-06 | 2020-06-18 | Universal Display Corporation | Hocheffiziente phosphoreszierende Materialien |
| US8969592B2 (en) | 2012-01-10 | 2015-03-03 | Universal Display Corporation | Heterocyclic host materials |
| US9447113B2 (en) | 2012-01-10 | 2016-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10167303B2 (en) | 2012-01-12 | 2019-01-01 | Udc Ireland Limited | Iridium organometallic complex containing a substituted dibenzo[f,h]quinoxaline and an electronic device having an emitting layer containing the iridium complex |
| WO2013104649A1 (en) | 2012-01-12 | 2013-07-18 | Basf Se | Metal complexes with dibenzo[f,h]quinoxalines |
| US9472762B2 (en) | 2012-01-12 | 2016-10-18 | Udc Ireland Limited | Iridium organometallic complex containing a substituted dibenzo[f,h]quinoxaline and an electronic device having an emitting layer containing the iridium complex |
| JP2013145811A (ja) * | 2012-01-13 | 2013-07-25 | Konica Minolta Inc | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| WO2013108787A1 (ja) | 2012-01-17 | 2013-07-25 | 三菱化学株式会社 | 有機電界発光素子、有機el照明および有機el表示装置 |
| US10211413B2 (en) | 2012-01-17 | 2019-02-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| DE102013200942B4 (de) | 2012-01-23 | 2023-07-27 | Udc Ireland Ltd. | Organisches Elektrolumineszenz-Element, Ladungstransportmaterial für organisches Elektrolumineszenz-Element, und Licht-emittierende Vorrichtung, Anzeigevorrichtung und Beleuchtungsvorrichtung, die jeweils das Element umfassen |
| DE102013200942A1 (de) | 2012-01-23 | 2013-07-25 | Udc Ireland Ltd. | Organisches Elektrolumineszenz-Element, Ladungstransportmaterial für organisches Elektrolumineszenz-Element, und Licht-emittierende Vorrichtung, Anzeigevorrichtung und Beleuchtungsvorrichtung, die jeweils das Element verwenden |
| EP2623508A1 (de) | 2012-02-02 | 2013-08-07 | Konica Minolta Advanced Layers, Inc. | Iridiumkomplexverbindung, Material aus organischem elektrolumineszentem Material, organisches elektrolumineszentes Material, Beleuchtungsvorrichtung und Anzeigevorrichtung |
| DE102013201846A1 (de) | 2012-02-06 | 2013-08-14 | Udc Ireland Limited | Organisches Elektrolumineszenz-Element, Verbindung und Material für organisches Elektrolumineszenz-Element, die hier verrwendet werden können, Licht-emittierende Vorrichtung, Anzeigevorrichtung und Beleuchtungsvorrichtung, die jeweils das Element verwenden |
| DE102013201846B4 (de) | 2012-02-06 | 2021-09-09 | Udc Ireland Limited | Organisches Elektrolumineszenz-Element, Verbindung für organisches Elektrolumineszenz-Element, die hier verwendet werden kann, Licht-emittierende Vorrichtung, Anzeigevorrichtung und Beleuchtungsvorrichtung, die jeweils das Element verwenden |
| WO2013120577A1 (en) | 2012-02-14 | 2013-08-22 | Merck Patent Gmbh | Spirobifluorene compounds for organic electroluminescent devices |
| EP3235892A1 (de) | 2012-02-14 | 2017-10-25 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| EP3101088A1 (de) | 2012-02-14 | 2016-12-07 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| US9118017B2 (en) | 2012-02-27 | 2015-08-25 | Universal Display Corporation | Host compounds for red phosphorescent OLEDs |
| EP3460864A1 (de) | 2012-03-15 | 2019-03-27 | Merck Patent GmbH | Elektronische vorrichtungen |
| US9386657B2 (en) | 2012-03-15 | 2016-07-05 | Universal Display Corporation | Organic Electroluminescent materials and devices |
| WO2013135352A1 (de) | 2012-03-15 | 2013-09-19 | Merck Patent Gmbh | Elektronische vorrichtungen |
| DE102013003605B4 (de) | 2012-03-15 | 2023-08-17 | Universal Display Corporation | Sekundäre Lochtransportschicht mit Tricarbazolverbindungen |
| US9054323B2 (en) | 2012-03-15 | 2015-06-09 | Universal Display Corporation | Secondary hole transporting layer with diarylamino-phenyl-carbazole compounds |
| US9548459B2 (en) | 2012-03-15 | 2017-01-17 | Universal Display Corporation | Organic materials for organic light emitting devices |
| WO2013139431A1 (de) | 2012-03-23 | 2013-09-26 | Merck Patent Gmbh | 9,9'-spirobixanthenderivate für elektrolumineszenzvorrichtungen |
| US8723209B2 (en) | 2012-04-27 | 2014-05-13 | Universal Display Corporation | Out coupling layer containing particle polymer composite |
| US10741762B2 (en) | 2012-05-02 | 2020-08-11 | Clap Co., Ltd. | Method for the deposition of an organic material |
| US9184399B2 (en) | 2012-05-04 | 2015-11-10 | Universal Display Corporation | Asymmetric hosts with triaryl silane side chains |
| US9773985B2 (en) | 2012-05-21 | 2017-09-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2013176194A1 (ja) | 2012-05-24 | 2013-11-28 | 三菱化学株式会社 | 有機電界発光素子、有機電界発光照明装置及び有機電界発光表示装置 |
| US9670404B2 (en) | 2012-06-06 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| DE102012011335A1 (de) | 2012-06-06 | 2013-12-12 | Merck Patent Gmbh | Verbindungen für Organische Elekronische Vorrichtungen |
| WO2013182263A1 (de) | 2012-06-06 | 2013-12-12 | Merck Patent Gmbh | Phenanthrenverbindungen für organische elektronische vorrichtungen |
| EP2677559A1 (de) | 2012-06-21 | 2013-12-25 | Konica Minolta, Inc. | Organisches elektrolumineszentes Element, Anzeigevorrichtung und Beleuchtungsvorrichtung |
| US9502672B2 (en) | 2012-06-21 | 2016-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9725476B2 (en) | 2012-07-09 | 2017-08-08 | Universal Display Corporation | Silylated metal complexes |
| US9620724B2 (en) | 2012-07-10 | 2017-04-11 | Udc Ireland Limited | Benzimidazo[1,2-A]benzimidazole derivatives for electronic applications |
| US10862051B2 (en) | 2012-07-10 | 2020-12-08 | Udc Ireland Limited | Benzimidazo[1,2-a]benzimidazole derivatives for electronic applications |
| US9231218B2 (en) | 2012-07-10 | 2016-01-05 | Universal Display Corporation | Phosphorescent emitters containing dibenzo[1,4]azaborinine structure |
| US11744152B2 (en) | 2012-07-10 | 2023-08-29 | Udc Ireland Limited | Benzimidazo[1,2-a]benzimidazole derivatives for electronic applications |
| WO2014008967A2 (de) | 2012-07-10 | 2014-01-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2014009317A1 (en) | 2012-07-10 | 2014-01-16 | Basf Se | Benzimidazo[1,2-a]benzimidazole derivatives for electronic applications |
| EP3232485A1 (de) | 2012-07-10 | 2017-10-18 | UDC Ireland Limited | Benzimidazo[1,2-a]benzimidazol-derivate für elektronische anwendungen |
| US10243150B2 (en) | 2012-07-10 | 2019-03-26 | Udc Ireland Limited | Benzimidazo[1,2-a]benzimidazole derivatives for electronic applications |
| WO2014012972A1 (en) | 2012-07-19 | 2014-01-23 | Basf Se | Dinuclear metal complexes comprising carbene ligands and the use thereof in oleds |
| US9590196B2 (en) | 2012-07-19 | 2017-03-07 | Udc Ireland Limited | Dinuclear metal complexes comprising carbene ligands and the use thereof in OLEDs |
| US9540329B2 (en) | 2012-07-19 | 2017-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3133079A1 (de) | 2012-07-19 | 2017-02-22 | UDC Ireland Limited | Dinukleare metallkomplexe mit carbenliganden und verwendung davon in oleds |
| US9059412B2 (en) | 2012-07-19 | 2015-06-16 | Universal Display Corporation | Transition metal complexes containing substituted imidazole carbene as ligands and their application in OLEDs |
| DE102013214144B4 (de) | 2012-07-19 | 2023-02-16 | Universal Display Corp. | Diarylamino-substituierte Metallkomplexe |
| WO2014015935A2 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Verbindungen und organische elektronische vorrichtungen |
| EP3424907A2 (de) | 2012-07-23 | 2019-01-09 | Merck Patent GmbH | Verbindungen und organische elektronische vorrichtungen |
| WO2014015937A1 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Verbindungen und organische elektrolumineszierende vorrichtungen |
| DE202013012401U1 (de) | 2012-07-23 | 2016-10-12 | Merck Patent Gmbh | Verbindungen und Organische Elektronische Vorrichtungen |
| WO2014015931A1 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2014015938A1 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Derivate von 2-diarylaminofluoren und diese enthaltnde organische elektronische verbindungen |
| US9663544B2 (en) | 2012-07-25 | 2017-05-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9627631B2 (en) | 2012-07-30 | 2017-04-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9318710B2 (en) | 2012-07-30 | 2016-04-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9403859B2 (en) | 2012-08-02 | 2016-08-02 | Roche Diagnostics Operations, Inc. | Iridium-based complexes for ECL |
| US10227366B2 (en) | 2012-08-02 | 2019-03-12 | Roche Diagnostics Operations, Inc. | Bis-iridium-complexes for manufacturing of ECL-labels |
| WO2014019711A1 (en) * | 2012-08-02 | 2014-02-06 | Roche Diagnostics Gmbh | New iridium-based complexes for ecl |
| US9399654B2 (en) | 2012-08-02 | 2016-07-26 | Roche Diagnostics Operations, Inc. | Iridium-based complexes for ECL |
| US9416150B2 (en) | 2012-08-02 | 2016-08-16 | Roche Diagnostics Operations, Inc. | Iridium-based complexes for ECL |
| US9499573B2 (en) | 2012-08-02 | 2016-11-22 | Roche Diagnostics Operations, Inc. | Iridium-based complexes for ECL |
| EP3424936A1 (de) | 2012-08-07 | 2019-01-09 | Merck Patent GmbH | Metallkomplexe |
| WO2014023377A2 (de) | 2012-08-07 | 2014-02-13 | Merck Patent Gmbh | Metallkomplexe |
| WO2014023388A1 (de) | 2012-08-10 | 2014-02-13 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2014030666A1 (ja) | 2012-08-24 | 2014-02-27 | コニカミノルタ株式会社 | 透明電極、電子デバイス、および透明電極の製造方法 |
| US9978958B2 (en) | 2012-08-24 | 2018-05-22 | Universal Display Corporation | Phosphorescent emitters with phenylimidazole ligands |
| US8952362B2 (en) | 2012-08-31 | 2015-02-10 | The Regents Of The University Of Michigan | High efficiency and brightness fluorescent organic light emitting diode by triplet-triplet fusion |
| US10957870B2 (en) | 2012-09-07 | 2021-03-23 | Universal Display Corporation | Organic light emitting device |
| US11696459B2 (en) | 2012-09-07 | 2023-07-04 | Universal Display Corporation | Phosphorescence-sensitized delayed fluorescence light emitting system |
| WO2014044344A1 (de) | 2012-09-18 | 2014-03-27 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US10249827B2 (en) | 2012-09-20 | 2019-04-02 | Udc Ireland Limited | Azadibenzofurans for electronic applications |
| EP3318566A1 (de) | 2012-09-20 | 2018-05-09 | UDC Ireland Limited | Azadibenzofurane für elektronische anwendungen |
| US9287513B2 (en) | 2012-09-24 | 2016-03-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9312505B2 (en) | 2012-09-25 | 2016-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10388894B2 (en) | 2012-09-25 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11917902B2 (en) | 2012-09-25 | 2024-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2014054596A1 (ja) | 2012-10-02 | 2014-04-10 | 三菱化学株式会社 | 有機電界発光素子、有機el照明および有機el表示装置 |
| WO2014056567A1 (de) | 2012-10-11 | 2014-04-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2014067614A1 (de) | 2012-10-31 | 2014-05-08 | Merck Patent Gmbh | Elektronische vorrichtung |
| EP3806176A1 (de) | 2012-10-31 | 2021-04-14 | Merck Patent GmbH | Elektronische vorrichtung |
| US11031559B2 (en) | 2012-11-06 | 2021-06-08 | Udc Ireland Limited | Phenoxasiline based compounds for electronic application |
| WO2014072320A1 (en) | 2012-11-06 | 2014-05-15 | Basf Se | Phenoxasiline based compounds for electronic application |
| US10319917B2 (en) | 2012-11-06 | 2019-06-11 | Udc Ireland Limited | Phenoxasiline based compounds for electronic application |
| US8692241B1 (en) | 2012-11-08 | 2014-04-08 | Universal Display Corporation | Transition metal complexes containing triazole and tetrazole carbene ligands |
| US10033002B2 (en) | 2012-11-09 | 2018-07-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10510968B2 (en) | 2012-11-09 | 2019-12-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9634264B2 (en) | 2012-11-09 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11380855B2 (en) | 2012-11-09 | 2022-07-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8946697B1 (en) | 2012-11-09 | 2015-02-03 | Universal Display Corporation | Iridium complexes with aza-benzo fused ligands |
| US9685617B2 (en) | 2012-11-09 | 2017-06-20 | Universal Display Corporation | Organic electronuminescent materials and devices |
| EP3378857A1 (de) | 2012-11-12 | 2018-09-26 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| US10847729B2 (en) | 2012-11-20 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9190623B2 (en) | 2012-11-20 | 2015-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11145831B2 (en) | 2012-11-20 | 2021-10-12 | Universal Display Corporation | Osmium(IV) complexes for OLED materials |
| US10069090B2 (en) | 2012-11-20 | 2018-09-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2014079532A1 (de) | 2012-11-20 | 2014-05-30 | Merck Patent Gmbh | Formulierung in hochreinem l?sungsmittel zur herstellung elektronischer vorrichtungen |
| US9512136B2 (en) | 2012-11-26 | 2016-12-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9166175B2 (en) | 2012-11-27 | 2015-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2014082705A1 (de) | 2012-11-30 | 2014-06-05 | Merck Patent Gmbh | Elektronische vorrichtung |
| US8716484B1 (en) | 2012-12-05 | 2014-05-06 | Universal Display Corporation | Hole transporting materials with twisted aryl groups |
| US10069081B2 (en) | 2012-12-07 | 2018-09-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9209411B2 (en) | 2012-12-07 | 2015-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10910564B2 (en) | 2012-12-07 | 2021-02-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11716902B2 (en) | 2012-12-07 | 2023-08-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9670185B2 (en) | 2012-12-07 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10411199B2 (en) | 2012-12-12 | 2019-09-10 | Samsung Electronics Co., Ltd. | Organometallic complexes, and organic electroluminescent device and display using the same |
| US9653691B2 (en) | 2012-12-12 | 2017-05-16 | Universal Display Corporation | Phosphorescence-sensitizing fluorescence material system |
| WO2014106524A2 (de) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2014106523A1 (de) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Elektronische vorrichtung |
| WO2014106522A1 (de) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US9385326B2 (en) | 2013-01-15 | 2016-07-05 | Basf Se | Triangulene oligomers and polymers and their use as hole conducting material |
| US10400163B2 (en) | 2013-02-08 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9935276B2 (en) | 2013-02-21 | 2018-04-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10367154B2 (en) | 2013-02-21 | 2019-07-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11871652B2 (en) | 2013-02-21 | 2024-01-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8927749B2 (en) | 2013-03-07 | 2015-01-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9419225B2 (en) | 2013-03-14 | 2016-08-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2014147134A1 (en) | 2013-03-20 | 2014-09-25 | Basf Se | Azabenzimidazole carbene complexes as efficiency booster in oleds |
| US9997712B2 (en) | 2013-03-27 | 2018-06-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2014157618A1 (ja) | 2013-03-29 | 2014-10-02 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、それを具備した照明装置及び表示装置 |
| WO2014157494A1 (ja) | 2013-03-29 | 2014-10-02 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| WO2014177518A1 (en) | 2013-04-29 | 2014-11-06 | Basf Se | Transition metal complexes with carbene ligands and the use thereof in oleds |
| US9537106B2 (en) | 2013-05-09 | 2017-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9735373B2 (en) | 2013-06-10 | 2017-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9673401B2 (en) | 2013-06-28 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10199581B2 (en) | 2013-07-01 | 2019-02-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10991896B2 (en) | 2013-07-01 | 2021-04-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3608329A1 (de) | 2013-07-02 | 2020-02-12 | UDC Ireland Limited | Monosubstituierte diazabenzimidazolcarben-metall-komplexe zur verwendung in organischen leuchtdioden |
| WO2015000955A1 (en) | 2013-07-02 | 2015-01-08 | Basf Se | Monosubstituted diazabenzimidazole carbene metal complexes for use in organic light emitting diodes |
| EP3266789A1 (de) | 2013-07-02 | 2018-01-10 | UDC Ireland Limited | Monosubstituierte diazabenzimidazolcarben-metall-komplexe zur verwendung in organischen leuchtdioden |
| US11605790B2 (en) | 2013-07-02 | 2023-03-14 | Udc Ireland Limited | Monosubstituted diazabenzimidazole carbene metal complexes for use in organic light emitting diodes |
| US10121975B2 (en) | 2013-07-03 | 2018-11-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9761807B2 (en) | 2013-07-15 | 2017-09-12 | Universal Display Corporation | Organic light emitting diode materials |
| US9553274B2 (en) | 2013-07-16 | 2017-01-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9324949B2 (en) | 2013-07-16 | 2016-04-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9224958B2 (en) | 2013-07-19 | 2015-12-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10930866B2 (en) | 2013-07-25 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3647393A1 (de) | 2013-07-30 | 2020-05-06 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| EP3712229A1 (de) | 2013-07-30 | 2020-09-23 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| EP3239161A1 (de) | 2013-07-31 | 2017-11-01 | UDC Ireland Limited | Lumineszente diazabenzimidazol-carben-metall-komplexe |
| US11611042B2 (en) | 2013-08-20 | 2023-03-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9831437B2 (en) | 2013-08-20 | 2017-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10749114B2 (en) | 2013-08-20 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10074806B2 (en) | 2013-08-20 | 2018-09-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9932359B2 (en) | 2013-08-30 | 2018-04-03 | University Of Southern California | Organic electroluminescent materials and devices |
| US10199582B2 (en) | 2013-09-03 | 2019-02-05 | University Of Southern California | Organic electroluminescent materials and devices |
| US10347848B2 (en) | 2013-09-03 | 2019-07-09 | Basf Se | Amorphous material and the use thereof |
| US9735378B2 (en) | 2013-09-09 | 2017-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9748503B2 (en) | 2013-09-13 | 2017-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10003034B2 (en) | 2013-09-30 | 2018-06-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3904361A2 (de) | 2013-10-02 | 2021-11-03 | Merck Patent GmbH | Borenthaltende verbindungen |
| US9831447B2 (en) | 2013-10-08 | 2017-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9293712B2 (en) | 2013-10-11 | 2016-03-22 | Universal Display Corporation | Disubstituted pyrene compounds with amino group containing ortho aryl group and devices containing the same |
| US9853229B2 (en) | 2013-10-23 | 2017-12-26 | University Of Southern California | Organic electroluminescent materials and devices |
| US10128450B2 (en) | 2013-10-23 | 2018-11-13 | University Of Southern California | Organic electroluminescent materials and devices |
| US11944000B2 (en) | 2013-10-29 | 2024-03-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2015063046A1 (en) | 2013-10-31 | 2015-05-07 | Basf Se | Azadibenzothiophenes for electronic applications |
| US9306179B2 (en) | 2013-11-08 | 2016-04-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9647218B2 (en) | 2013-11-14 | 2017-05-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9905784B2 (en) | 2013-11-15 | 2018-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10056565B2 (en) | 2013-11-20 | 2018-08-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9812653B2 (en) | 2013-11-28 | 2017-11-07 | Samsung Electronics Co., Ltd. | Carbazole compound and organic light-emitting device including the same |
| US10644251B2 (en) | 2013-12-04 | 2020-05-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2015082046A2 (de) | 2013-12-06 | 2015-06-11 | Merck Patent Gmbh | Substituierte oxepine |
| EP3693437A1 (de) | 2013-12-06 | 2020-08-12 | Merck Patent GmbH | Verbindungen und organische elektronische vorrichtungen |
| EP3345984A1 (de) | 2013-12-06 | 2018-07-11 | Merck Patent GmbH | Verbindungen und organische elektronische vorrichtungen |
| US9876173B2 (en) | 2013-12-09 | 2018-01-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2015086108A1 (de) | 2013-12-12 | 2015-06-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US10355227B2 (en) | 2013-12-16 | 2019-07-16 | Universal Display Corporation | Metal complex for phosphorescent OLED |
| US11653558B2 (en) | 2013-12-16 | 2023-05-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3708634A1 (de) | 2013-12-19 | 2020-09-16 | Merck Patent GmbH | Heterocyclische spiroverbindungen |
| WO2015090504A2 (de) | 2013-12-19 | 2015-06-25 | Merck Patent Gmbh | Heterocyclische spiroverbindungen |
| EP3916822A1 (de) | 2013-12-20 | 2021-12-01 | UDC Ireland Limited | Hocheffiziente oled-vorrichtungen mit sehr kurzer abklingzeit |
| US9847496B2 (en) | 2013-12-23 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10985331B2 (en) | 2014-01-07 | 2021-04-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10135008B2 (en) | 2014-01-07 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10749122B2 (en) | 2014-01-07 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11943999B2 (en) | 2014-01-07 | 2024-03-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9978961B2 (en) | 2014-01-08 | 2018-05-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11005051B2 (en) | 2014-01-08 | 2021-05-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9755159B2 (en) | 2014-01-23 | 2017-09-05 | Universal Display Corporation | Organic materials for OLEDs |
| US9935277B2 (en) | 2014-01-30 | 2018-04-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9590194B2 (en) | 2014-02-14 | 2017-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9847497B2 (en) | 2014-02-18 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11024816B2 (en) | 2014-02-18 | 2021-06-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10003033B2 (en) | 2014-02-18 | 2018-06-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10707423B2 (en) | 2014-02-21 | 2020-07-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9647217B2 (en) | 2014-02-24 | 2017-05-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9502656B2 (en) | 2014-02-24 | 2016-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11600782B2 (en) | 2014-02-27 | 2023-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403825B2 (en) | 2014-02-27 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9673407B2 (en) | 2014-02-28 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9590195B2 (en) | 2014-02-28 | 2017-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9181270B2 (en) | 2014-02-28 | 2015-11-10 | Universal Display Corporation | Method of making sulfide compounds |
| US9190620B2 (en) | 2014-03-01 | 2015-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10208026B2 (en) | 2014-03-18 | 2019-02-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9748504B2 (en) | 2014-03-25 | 2017-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9862739B2 (en) | 2014-03-31 | 2018-01-09 | Udc Ireland Limited | Metal complexes, comprising carbene ligands having an O-substituted non-cyclometalated aryl group and their use in organic light emitting diodes |
| US10118939B2 (en) | 2014-03-31 | 2018-11-06 | Udc Ireland Limited | Metal complexes, comprising carbene ligands having an o-substituted non-cyclometalated aryl group and their use in organic light emitting diodes |
| US10370396B2 (en) | 2014-03-31 | 2019-08-06 | Udc Ireland Limited | Metal complexes, comprising carbene ligands having an O-substituted non-cyclometallated aryl group and their use in organic light emitting diodes |
| US9929353B2 (en) | 2014-04-02 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9691993B2 (en) | 2014-04-09 | 2017-06-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10008679B2 (en) | 2014-04-14 | 2018-06-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11005052B2 (en) | 2014-04-14 | 2021-05-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9847498B2 (en) | 2014-04-14 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11793066B2 (en) | 2014-04-14 | 2023-10-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9905785B2 (en) | 2014-04-14 | 2018-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10825998B2 (en) | 2014-04-14 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10256427B2 (en) | 2014-04-15 | 2019-04-09 | Universal Display Corporation | Efficient organic electroluminescent devices |
| US9741941B2 (en) | 2014-04-29 | 2017-08-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3533794A2 (de) | 2014-04-30 | 2019-09-04 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2015165563A1 (de) | 2014-04-30 | 2015-11-05 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US10457699B2 (en) | 2014-05-02 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11919916B2 (en) | 2014-05-02 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11427607B2 (en) | 2014-05-02 | 2022-08-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2015169412A1 (de) | 2014-05-05 | 2015-11-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10256419B2 (en) | 2014-05-08 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403830B2 (en) | 2014-05-08 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10301338B2 (en) | 2014-05-08 | 2019-05-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495754B2 (en) | 2014-05-08 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10636983B2 (en) | 2014-05-08 | 2020-04-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10263198B2 (en) | 2014-05-08 | 2019-04-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10276805B2 (en) | 2014-05-08 | 2019-04-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9997716B2 (en) | 2014-05-27 | 2018-06-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10461260B2 (en) | 2014-06-03 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10186664B2 (en) | 2014-06-17 | 2019-01-22 | Basf Se | N-fluoroalkyl-substituted dibromonaphthalene diimides and their use as semiconductor |
| WO2015192941A1 (de) | 2014-06-18 | 2015-12-23 | Merck Patent Gmbh | Zusammensetzungen für elektronische vorrichtungen |
| DE102014008722A1 (de) | 2014-06-18 | 2015-12-24 | Merck Patent Gmbh | Zusammensetzungen für elektronische Vorrichtungen |
| WO2015197156A1 (de) | 2014-06-25 | 2015-12-30 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10700293B2 (en) | 2014-06-26 | 2020-06-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9911931B2 (en) | 2014-06-26 | 2018-03-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11957047B2 (en) | 2014-07-09 | 2024-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10297762B2 (en) | 2014-07-09 | 2019-05-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11456423B2 (en) | 2014-07-09 | 2022-09-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11024811B2 (en) | 2014-07-09 | 2021-06-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10566546B2 (en) | 2014-07-14 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4037000A1 (de) | 2014-07-21 | 2022-08-03 | Merck Patent GmbH | Materialen für elektronische vorrichtungen |
| US9929357B2 (en) | 2014-07-22 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016016791A1 (en) | 2014-07-28 | 2016-02-04 | Idemitsu Kosan Co., Ltd (Ikc) | 2,9-functionalized benzimidazolo[1,2-a]benzimidazoles as hosts for organic light emitting diodes (oleds) |
| US10411200B2 (en) | 2014-08-07 | 2019-09-10 | Universal Display Corporation | Electroluminescent (2-phenylpyridine)iridium complexes and devices |
| EP2982676A1 (de) | 2014-08-07 | 2016-02-10 | Idemitsu Kosan Co., Ltd. | Benzimidazo[2,1-b]benzoxazole für elektronische Anwendungen |
| US11108000B2 (en) | 2014-08-07 | 2021-08-31 | Unniversal Display Corporation | Organic electroluminescent materials and devices |
| TWI690534B (zh) * | 2014-08-08 | 2020-04-11 | 愛爾蘭商Udc愛爾蘭責任有限公司 | 電致發光咪唑并喹噁啉碳烯金屬錯合物 |
| WO2016020516A1 (en) * | 2014-08-08 | 2016-02-11 | Basf Se | Electroluminescent imidazo-quinoxaline carbene metal complexes |
| EP3466957A1 (de) | 2014-08-08 | 2019-04-10 | UDC Ireland Limited | Oled enthaltend einen elektrolumineszenten imidazo-chinoxalin-carben-metallkomplexe |
| TWI663173B (zh) * | 2014-08-08 | 2019-06-21 | 愛爾蘭商Udc愛爾蘭責任有限公司 | 電致發光咪唑并喹噁啉碳烯金屬錯合物 |
| US10784448B2 (en) | 2014-08-08 | 2020-09-22 | Udc Ireland Limited | Electroluminescent imidazo-quinoxaline carbene metal complexes |
| WO2016027217A1 (en) | 2014-08-18 | 2016-02-25 | Basf Se | Organic semiconductor composition comprising liquid medium |
| US10224485B2 (en) | 2014-08-18 | 2019-03-05 | Basf Se | Process for preparing a crystalline organic semiconductor material |
| WO2016027218A1 (en) | 2014-08-18 | 2016-02-25 | Basf Se | Process for preparing crystalline organic semiconductor material |
| US10454037B2 (en) | 2014-08-18 | 2019-10-22 | Basf Se | Organic semiconductor composition comprising a liquid medium |
| EP2993215A1 (de) | 2014-09-04 | 2016-03-09 | Idemitsu Kosan Co., Ltd. | Azabenzimidazo[2,1-a]benzimidazole für elektronische Anwendungen |
| US10135007B2 (en) | 2014-09-29 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10043987B2 (en) | 2014-09-29 | 2018-08-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11641774B2 (en) | 2014-09-29 | 2023-05-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10749113B2 (en) | 2014-09-29 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342510B2 (en) | 2014-10-06 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10361375B2 (en) | 2014-10-06 | 2019-07-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342516B2 (en) | 2014-10-08 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9397302B2 (en) | 2014-10-08 | 2016-07-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10854826B2 (en) | 2014-10-08 | 2020-12-01 | Universal Display Corporation | Organic electroluminescent compounds, compositions and devices |
| US10998508B2 (en) | 2014-10-08 | 2021-05-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9799838B2 (en) | 2014-10-08 | 2017-10-24 | Universal Display Corporation | Fluorinated organic electroluminescent materials and devices |
| US10950803B2 (en) | 2014-10-13 | 2021-03-16 | Universal Display Corporation | Compounds and uses in devices |
| US9484541B2 (en) | 2014-10-20 | 2016-11-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3015469A1 (de) | 2014-10-30 | 2016-05-04 | Idemitsu Kosan Co., Ltd. | 5-((benz)imidazol-2-yl)benzimidazo[1,2-a]benzimidazole für elektronische anwendungen |
| WO2016067261A1 (en) | 2014-10-30 | 2016-05-06 | Idemitsu Kosan Co., Ltd. | 5-((benz)imidazol-2-yl)benzimidazo[1,2-a]benzimidazoles for electronic applications |
| US10868261B2 (en) | 2014-11-10 | 2020-12-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016074755A1 (de) | 2014-11-11 | 2016-05-19 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10038151B2 (en) | 2014-11-12 | 2018-07-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10411201B2 (en) | 2014-11-12 | 2019-09-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11043641B2 (en) | 2014-11-12 | 2021-06-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11832507B2 (en) | 2014-11-12 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9871212B2 (en) | 2014-11-14 | 2018-01-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9882151B2 (en) | 2014-11-14 | 2018-01-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016079667A1 (en) | 2014-11-17 | 2016-05-26 | Idemitsu Kosan Co., Ltd. | Indole derivatives for electronic applications |
| WO2016079169A1 (en) | 2014-11-18 | 2016-05-26 | Basf Se | Pt- or pd-carbene complexes for use in organic light emitting diodes |
| US9761814B2 (en) | 2014-11-18 | 2017-09-12 | Universal Display Corporation | Organic light-emitting materials and devices |
| US10522767B2 (en) | 2014-11-26 | 2019-12-31 | Basf Se | 4-oxoquinoline compounds |
| WO2016083914A1 (en) | 2014-11-26 | 2016-06-02 | Basf Se | 4-oxoquinoline compounds |
| US9825260B2 (en) | 2014-11-26 | 2017-11-21 | Universal Display Corporation | Emissive display with photo-switchable polarization |
| US10323180B2 (en) | 2014-12-04 | 2019-06-18 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Deuterated organic compound, mixture and composition containing said compound, and organic electronic device |
| US10840450B2 (en) | 2014-12-04 | 2020-11-17 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Polymer, and mixture or formulation, and organic electronic device containing same, and monomer thereof |
| US10510967B2 (en) | 2014-12-11 | 2019-12-17 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Organic compound, and mixture, formulation and organic device comprising the same |
| EP3034506A1 (de) | 2014-12-15 | 2016-06-22 | Idemitsu Kosan Co., Ltd | 4-funktionalisierte Carbazolderivate für elektronische Anwendungen |
| EP3034507A1 (de) | 2014-12-15 | 2016-06-22 | Idemitsu Kosan Co., Ltd | 1-funktionalisierte Dibenzofurane und Dibenzothiophene für organische Leuchtdioden (OLEDS) |
| WO2016097983A1 (en) | 2014-12-15 | 2016-06-23 | Idemitsu Kosan Co., Ltd. | 1-functionalized dibenzofurans and dibenzothiophenes for organic light emitting diodes (oleds) |
| US9680113B2 (en) | 2014-12-17 | 2017-06-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10000517B2 (en) | 2014-12-17 | 2018-06-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9450195B2 (en) | 2014-12-17 | 2016-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10253252B2 (en) | 2014-12-30 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10636978B2 (en) | 2014-12-30 | 2020-04-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9312499B1 (en) | 2015-01-05 | 2016-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9406892B2 (en) | 2015-01-07 | 2016-08-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10364316B2 (en) | 2015-01-13 | 2019-07-30 | Guangzhou Chinaray Optoelectronics Materials Ltd. | Conjugated polymer containing ethynyl crosslinking group, mixture, formulation, organic electronic device containing the same and application therof |
| US9748500B2 (en) | 2015-01-15 | 2017-08-29 | Universal Display Corporation | Organic light emitting materials |
| US10418569B2 (en) | 2015-01-25 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9711730B2 (en) | 2015-01-25 | 2017-07-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016119992A1 (en) | 2015-01-30 | 2016-08-04 | Merck Patent Gmbh | Materials for electronic devices |
| WO2016124304A1 (de) | 2015-02-03 | 2016-08-11 | Merck Patent Gmbh | Metallkomplexe |
| US10164198B2 (en) | 2015-02-05 | 2018-12-25 | Samsung Electronics Co., Ltd. | Organometallic compound, composition containing organometallic compound, and organic light-emitting device including the same |
| US10326086B2 (en) | 2015-02-06 | 2019-06-18 | Samsung Electronics Co., Ltd. | Organometallic compound, composition containing the organometallic compound, and organic light-emitting device including the organometallic compound or composition |
| US11245081B2 (en) | 2015-02-06 | 2022-02-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3054498A1 (de) | 2015-02-06 | 2016-08-10 | Idemitsu Kosan Co., Ltd. | Bisimidazodiazozine |
| DE102015101767A1 (de) | 2015-02-06 | 2016-08-11 | Technische Universität Dresden | Blaue Fluoreszenzemitter |
| EP3053918A1 (de) | 2015-02-06 | 2016-08-10 | Idemitsu Kosan Co., Ltd | 2-Carbazol substituierte Benzimidazole für elektronische Anwendungen |
| US10355222B2 (en) | 2015-02-06 | 2019-07-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016125110A1 (en) | 2015-02-06 | 2016-08-11 | Idemitsu Kosan Co., Ltd. | Bisimidazolodiazocines |
| WO2016124704A1 (de) | 2015-02-06 | 2016-08-11 | Technische Universität Dresden | Blaue fluoreszenzemitter |
| US10418562B2 (en) | 2015-02-06 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10644247B2 (en) | 2015-02-06 | 2020-05-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10177316B2 (en) | 2015-02-09 | 2019-01-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11795385B2 (en) | 2015-02-13 | 2023-10-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4271160A2 (de) | 2015-02-13 | 2023-11-01 | Merck Patent GmbH | Aromatisches heterocyclisches derivat und organisches elektrolumineszenzelement, beleuchtungsvorrichtung und anzeigevorrichtung mit dem aromatischen heterocyclischen derivat |
| US10144867B2 (en) | 2015-02-13 | 2018-12-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10889754B2 (en) | 2015-02-13 | 2021-01-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11535797B2 (en) | 2015-02-13 | 2022-12-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680183B2 (en) | 2015-02-15 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9929361B2 (en) | 2015-02-16 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3056504A1 (de) | 2015-02-16 | 2016-08-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3061759A1 (de) | 2015-02-24 | 2016-08-31 | Idemitsu Kosan Co., Ltd | Nitrilsubstituierte dibenzofurane |
| US11678567B2 (en) | 2015-02-27 | 2023-06-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3061763A1 (de) | 2015-02-27 | 2016-08-31 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11056657B2 (en) | 2015-02-27 | 2021-07-06 | University Display Corporation | Organic electroluminescent materials and devices |
| US10600966B2 (en) | 2015-02-27 | 2020-03-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10686143B2 (en) | 2015-03-05 | 2020-06-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10270046B2 (en) | 2015-03-06 | 2019-04-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9780316B2 (en) | 2015-03-16 | 2017-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3070144A1 (de) | 2015-03-17 | 2016-09-21 | Idemitsu Kosan Co., Ltd. | Siebengliedrige ringverbindungen |
| US9911928B2 (en) | 2015-03-19 | 2018-03-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9871214B2 (en) | 2015-03-23 | 2018-01-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10529931B2 (en) | 2015-03-24 | 2020-01-07 | Universal Display Corporation | Organic Electroluminescent materials and devices |
| EP3072943A1 (de) | 2015-03-26 | 2016-09-28 | Idemitsu Kosan Co., Ltd. | Dibenzofuran/carbazol-substituierte benzonitrile |
| US10297770B2 (en) | 2015-03-27 | 2019-05-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016157113A1 (en) | 2015-03-31 | 2016-10-06 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole carrying aryl- or heteroarylnitril groups for organic light emitting diodes |
| EP3075737A1 (de) | 2015-03-31 | 2016-10-05 | Idemitsu Kosan Co., Ltd | Benzimidazolo[1,2-a]benzimidazol mit aryl- oder heteroarylnitrilgruppen für organische leuchtdioden |
| US11818949B2 (en) | 2015-04-06 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10693082B2 (en) | 2015-04-06 | 2020-06-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11672175B2 (en) | 2015-04-06 | 2023-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10593890B2 (en) | 2015-04-06 | 2020-03-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11245080B2 (en) | 2015-04-06 | 2022-02-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403826B2 (en) | 2015-05-07 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11744151B2 (en) | 2015-05-07 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10777749B2 (en) | 2015-05-07 | 2020-09-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9859510B2 (en) | 2015-05-15 | 2018-01-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3098229A1 (de) | 2015-05-15 | 2016-11-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11335864B2 (en) | 2015-05-15 | 2022-05-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| USRE48809E1 (en) | 2015-05-15 | 2021-11-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10547013B2 (en) | 2015-05-15 | 2020-01-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10109799B2 (en) | 2015-05-21 | 2018-10-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10256411B2 (en) | 2015-05-21 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10033004B2 (en) | 2015-06-01 | 2018-07-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10418568B2 (en) | 2015-06-01 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3101021A1 (de) | 2015-06-01 | 2016-12-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2016193243A1 (en) | 2015-06-03 | 2016-12-08 | Udc Ireland Limited | Highly efficient oled devices with very short decay times |
| EP4060757A1 (de) | 2015-06-03 | 2022-09-21 | UDC Ireland Limited | Hocheffiziente oled-vorrichtungen mit sehr kurzer abklingzeit |
| US11925102B2 (en) | 2015-06-04 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016198144A1 (en) | 2015-06-10 | 2016-12-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10825997B2 (en) | 2015-06-25 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10873036B2 (en) | 2015-07-07 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9978956B2 (en) | 2015-07-15 | 2018-05-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017012687A1 (en) | 2015-07-22 | 2017-01-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11127905B2 (en) | 2015-07-29 | 2021-09-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3124488A1 (de) | 2015-07-29 | 2017-02-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4301110A2 (de) | 2015-07-30 | 2024-01-03 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2017016630A1 (en) | 2015-07-30 | 2017-02-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11018309B2 (en) | 2015-08-03 | 2021-05-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017025166A1 (en) | 2015-08-13 | 2017-02-16 | Merck Patent Gmbh | Hexamethylindanes |
| WO2017028940A1 (en) | 2015-08-14 | 2017-02-23 | Merck Patent Gmbh | Phenoxazine derivatives for organic electroluminescent devices |
| US11522140B2 (en) | 2015-08-17 | 2022-12-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10522769B2 (en) | 2015-08-18 | 2019-12-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10181564B2 (en) | 2015-08-26 | 2019-01-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017036573A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | Compounds for electronic devices |
| EP3159350A1 (de) | 2015-09-03 | 2017-04-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10672996B2 (en) | 2015-09-03 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3760635A1 (de) | 2015-09-03 | 2021-01-06 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11626563B2 (en) | 2015-09-03 | 2023-04-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11605789B2 (en) | 2015-09-03 | 2023-03-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10361381B2 (en) | 2015-09-03 | 2019-07-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11302872B2 (en) | 2015-09-09 | 2022-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10770664B2 (en) | 2015-09-21 | 2020-09-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11812622B2 (en) | 2015-09-25 | 2023-11-07 | Universal Display Corporation | Organic electroluminescent compounds and devices |
| EP3150604A1 (de) | 2015-10-01 | 2017-04-05 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazol mit benzimidazolo[1,2-a]benzimidazolylgruppen, carbazolylgruppen, benzofurangruppen oder benzothiophengruppen für organische leuchtdioden |
| US10847728B2 (en) | 2015-10-01 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10593892B2 (en) | 2015-10-01 | 2020-03-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017056052A1 (en) | 2015-10-01 | 2017-04-06 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole carrying benzimidazolo[1,2-a]benzimidazolyl groups, carbazolyl groups, benzofurane groups or benzothiophene groups for organic light emitting diodes |
| US11889747B2 (en) | 2015-10-01 | 2024-01-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3150606A1 (de) | 2015-10-01 | 2017-04-05 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole mit benzofuran- oder benzothiophen- gruppen für organische licht emittierende dioden. |
| WO2017056055A1 (en) | 2015-10-01 | 2017-04-06 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole carrying triazine groups for organic light emitting diodes |
| US10991895B2 (en) | 2015-10-06 | 2021-04-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017071791A1 (en) | 2015-10-27 | 2017-05-04 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10388893B2 (en) | 2015-10-29 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11349087B2 (en) | 2015-10-29 | 2022-05-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10388892B2 (en) | 2015-10-29 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10177318B2 (en) | 2015-10-29 | 2019-01-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017078182A1 (en) | 2015-11-04 | 2017-05-11 | Idemitsu Kosan Co., Ltd. | Benzimidazole fused heteroaryls |
| US11555128B2 (en) | 2015-11-12 | 2023-01-17 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Printing composition, electronic device comprising same and preparation method for functional material thin film |
| US10998507B2 (en) | 2015-11-23 | 2021-05-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11832456B2 (en) | 2015-11-23 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10476010B2 (en) | 2015-11-30 | 2019-11-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017093958A1 (en) | 2015-12-04 | 2017-06-08 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole derivatives for organic light emitting diodes |
| US10968243B2 (en) | 2015-12-04 | 2021-04-06 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Organometallic complex and application thereof in electronic devices |
| US10490754B2 (en) | 2015-12-21 | 2019-11-26 | Udc Ireland Limited | Transition metal complexes with tripodal ligands and the use thereof in OLEDs |
| WO2017109722A1 (en) | 2015-12-21 | 2017-06-29 | Idemitsu Kosan Co., Ltd. | Nitrogen-containing heterocyclic compounds and organic electroluminescence devices containing them |
| EP3184534A1 (de) | 2015-12-21 | 2017-06-28 | UDC Ireland Limited | Übergangsmetallkomplexe mit dreibeinigen liganden und verwendung davon in oleds |
| DE102015122869A1 (de) | 2015-12-28 | 2017-06-29 | Technische Universität Dresden | Neue Emittermaterialien und Matrixmaterialien für optoelektronische und elektronische Bauelemente, insbesondere organische lichtemittierende Dioden (OLEDs) |
| US10957861B2 (en) | 2015-12-29 | 2021-03-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11818948B2 (en) | 2015-12-29 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11024808B2 (en) | 2015-12-29 | 2021-06-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10135006B2 (en) | 2016-01-04 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017133829A1 (de) | 2016-02-05 | 2017-08-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US11716898B2 (en) | 2016-02-09 | 2023-08-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11098245B2 (en) | 2016-02-09 | 2021-08-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10457864B2 (en) | 2016-02-09 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3205658A1 (de) | 2016-02-09 | 2017-08-16 | Universal Display Corporation | Organische elektrolumineszenzmaterialien und vorrichtungen |
| US10707427B2 (en) | 2016-02-09 | 2020-07-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3858842A1 (de) | 2016-02-09 | 2021-08-04 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11692132B2 (en) | 2016-02-09 | 2023-07-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10600967B2 (en) | 2016-02-18 | 2020-03-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017148565A1 (de) | 2016-03-03 | 2017-09-08 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2017148564A1 (de) | 2016-03-03 | 2017-09-08 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11094891B2 (en) | 2016-03-16 | 2021-08-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017157983A1 (de) | 2016-03-17 | 2017-09-21 | Merck Patent Gmbh | Verbindungen mit spirobifluoren-strukturen |
| US10276809B2 (en) | 2016-04-05 | 2019-04-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017178311A1 (de) | 2016-04-11 | 2017-10-19 | Merck Patent Gmbh | Heterocyclische verbindungen mit dibenzofuran- und/oder dibenzothiophen-strukturen |
| EP4122941A1 (de) | 2016-04-11 | 2023-01-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10236456B2 (en) | 2016-04-11 | 2019-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3231809A2 (de) | 2016-04-11 | 2017-10-18 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2017178864A1 (en) | 2016-04-12 | 2017-10-19 | Idemitsu Kosan Co., Ltd. | Seven-membered ring compounds |
| US11825734B2 (en) | 2016-04-13 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10566552B2 (en) | 2016-04-13 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342515B2 (en) | 2016-04-13 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11081647B2 (en) | 2016-04-22 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228003B2 (en) | 2016-04-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228002B2 (en) | 2016-04-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017186760A1 (en) | 2016-04-29 | 2017-11-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10985328B2 (en) | 2016-05-25 | 2021-04-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10840458B2 (en) | 2016-05-25 | 2020-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10468609B2 (en) | 2016-06-02 | 2019-11-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3978477A2 (de) | 2016-06-03 | 2022-04-06 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| WO2017207596A1 (en) | 2016-06-03 | 2017-12-07 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| DE102016110970A1 (de) | 2016-06-15 | 2017-12-21 | Technische Universität Dresden | Effiziente lichtemittierende Emittermoleküle für optoelektronische Anwendungen durch gezielte Verstärkung der Emission aus ladungsseparierten CT-Zuständen auf Basis dual fluoreszierender Benzol-(Poly)carboxylat-Akzeptoren |
| WO2017216299A1 (de) | 2016-06-15 | 2017-12-21 | Technische Universität Dresden | Emittermoleküle auf basis dual fluoreszierender benzol-(poly)carboxylat-akzeptoren |
| US11114624B2 (en) | 2016-06-20 | 2021-09-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3758084A1 (de) | 2016-06-20 | 2020-12-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3270435A2 (de) | 2016-06-20 | 2018-01-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11482683B2 (en) | 2016-06-20 | 2022-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11839139B2 (en) | 2016-06-20 | 2023-12-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11588121B2 (en) | 2016-06-20 | 2023-02-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10651403B2 (en) | 2016-06-20 | 2020-05-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11690284B2 (en) | 2016-06-20 | 2023-06-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3920254A1 (de) | 2016-06-20 | 2021-12-08 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11683981B2 (en) | 2016-06-20 | 2023-06-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10686140B2 (en) | 2016-06-20 | 2020-06-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10727423B2 (en) | 2016-06-20 | 2020-07-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3261147A1 (de) | 2016-06-20 | 2017-12-27 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3261146A2 (de) | 2016-06-20 | 2017-12-27 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4349935A2 (de) | 2016-06-20 | 2024-04-10 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10672997B2 (en) | 2016-06-20 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11424419B2 (en) | 2016-06-20 | 2022-08-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11903306B2 (en) | 2016-06-20 | 2024-02-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3843171A1 (de) | 2016-06-20 | 2021-06-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10862054B2 (en) | 2016-06-20 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017221999A1 (en) | 2016-06-22 | 2017-12-28 | Idemitsu Kosan Co., Ltd. | Specifically substituted benzofuro- and benzothienoquinolines for organic light emitting diodes |
| US10957866B2 (en) | 2016-06-30 | 2021-03-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9929360B2 (en) | 2016-07-08 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018007421A1 (en) | 2016-07-08 | 2018-01-11 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP3792235A1 (de) | 2016-07-08 | 2021-03-17 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| US10680184B2 (en) | 2016-07-11 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10566547B2 (en) | 2016-07-11 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10720587B2 (en) | 2016-07-19 | 2020-07-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10153443B2 (en) | 2016-07-19 | 2018-12-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10205105B2 (en) | 2016-08-15 | 2019-02-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10608186B2 (en) | 2016-09-14 | 2020-03-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3297051A1 (de) | 2016-09-14 | 2018-03-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11024807B2 (en) | 2016-09-14 | 2021-06-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018050583A1 (de) | 2016-09-14 | 2018-03-22 | Merck Patent Gmbh | Verbindungen mit carbazol-strukturen |
| WO2018050584A1 (de) | 2016-09-14 | 2018-03-22 | Merck Patent Gmbh | Verbindungen mit spirobifluoren-strukturen |
| US10505127B2 (en) | 2016-09-19 | 2019-12-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3323822A1 (de) | 2016-09-23 | 2018-05-23 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10680187B2 (en) | 2016-09-23 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018060218A1 (de) | 2016-09-30 | 2018-04-05 | Merck Patent Gmbh | Carbazole mit diazadibenzofuran- oder diazadibenzothiophen-strukturen |
| WO2018060307A1 (de) | 2016-09-30 | 2018-04-05 | Merck Patent Gmbh | Verbindungen mit diazadibenzofuran- oder diazadibenzothiophen-strukturen |
| US11081658B2 (en) | 2016-10-03 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11196010B2 (en) | 2016-10-03 | 2021-12-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3301088A1 (de) | 2016-10-03 | 2018-04-04 | Universal Display Corporation | Kondensierte pyridine als organische elektrolumineszente materialien und vorrichtungen |
| US11127906B2 (en) | 2016-10-03 | 2021-09-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11189804B2 (en) | 2016-10-03 | 2021-11-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11183642B2 (en) | 2016-10-03 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11711969B2 (en) | 2016-10-03 | 2023-07-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11011709B2 (en) | 2016-10-07 | 2021-05-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3305796A1 (de) | 2016-10-07 | 2018-04-11 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11711968B2 (en) | 2016-10-07 | 2023-07-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3858844A1 (de) | 2016-10-07 | 2021-08-04 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4255151A2 (de) | 2016-10-10 | 2023-10-04 | Merck Patent GmbH | Spiro[fluoren-9,9'-(thio)xanthen] verbindungen |
| EP4113643A1 (de) | 2016-10-10 | 2023-01-04 | Merck Patent GmbH | Elektronische vorrichtung |
| WO2018069167A1 (de) | 2016-10-10 | 2018-04-19 | Merck Patent Gmbh | Elektronische vorrichtung |
| US11239432B2 (en) | 2016-10-14 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10608185B2 (en) | 2016-10-17 | 2020-03-31 | Univeral Display Corporation | Organic electroluminescent materials and devices |
| DE102017008794A1 (de) | 2016-10-17 | 2018-04-19 | Merck Patent Gmbh | Materialien zur Verwendung in elektronischen Vorrichtungen |
| US10236458B2 (en) | 2016-10-24 | 2019-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018083053A1 (de) | 2016-11-02 | 2018-05-11 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018087020A1 (en) | 2016-11-08 | 2018-05-17 | Merck Patent Gmbh | Compounds for electronic devices |
| EP3321258A1 (de) | 2016-11-09 | 2018-05-16 | Universal Display Corporation | 4-phenylbenzo[g]quinazolin oder 4-(3,5-dimethylphenylbenzo[g]quinazoline iridiumkomplexe zur verwendung als nah-infrarot oder infrarot emittierende materialien in oleds |
| WO2018087022A1 (de) | 2016-11-09 | 2018-05-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| EP3789379A1 (de) | 2016-11-09 | 2021-03-10 | Universal Display Corporation | 4-phenylbenzo[g]quinazolin oder 4-(3,5-dimethylphenylbenzo[g]quinazoline iridiumkomplexe zur verwendung als nah-infrarot oder infrarot emittierende materialien in oleds |
| US10340464B2 (en) | 2016-11-10 | 2019-07-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680188B2 (en) | 2016-11-11 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11069864B2 (en) | 2016-11-11 | 2021-07-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3354654A2 (de) | 2016-11-11 | 2018-08-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4092036A1 (de) | 2016-11-11 | 2022-11-23 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4271163A2 (de) | 2016-11-14 | 2023-11-01 | Merck Patent GmbH | Verbindungen mit einer akzeptor- und einer donorgruppe |
| WO2018087346A1 (de) | 2016-11-14 | 2018-05-17 | Merck Patent Gmbh | Verbindungen mit einer akzeptor- und einer donorgruppe |
| US10897016B2 (en) | 2016-11-14 | 2021-01-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10662196B2 (en) | 2016-11-17 | 2020-05-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018091435A1 (en) | 2016-11-17 | 2018-05-24 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US10964893B2 (en) | 2016-11-17 | 2021-03-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10833276B2 (en) | 2016-11-21 | 2020-11-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10153445B2 (en) | 2016-11-21 | 2018-12-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018095839A1 (de) | 2016-11-22 | 2018-05-31 | Merck Patent Gmbh | Verbrückte triarylamine für elektronische vorrichtungen |
| WO2018095381A1 (zh) | 2016-11-23 | 2018-05-31 | 广州华睿光电材料有限公司 | 印刷油墨组合物及其制备方法和用途 |
| US11248138B2 (en) | 2016-11-23 | 2022-02-15 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Printing ink formulations, preparation methods and uses thereof |
| US11239428B2 (en) | 2016-11-23 | 2022-02-01 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Boron-containing organic compound and applications thereof, organic mixture, and organic electronic device |
| US11447496B2 (en) | 2016-11-23 | 2022-09-20 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Nitrogen-containing fused heterocyclic ring compound and application thereof |
| WO2018095392A1 (zh) | 2016-11-23 | 2018-05-31 | 广州华睿光电材料有限公司 | 有机混合物、组合物以及有机电子器件 |
| US10804470B2 (en) | 2016-11-23 | 2020-10-13 | Guangzhou Chinaray Optoelectronic Materials Ltd | Organic compound |
| WO2018095395A1 (zh) | 2016-11-23 | 2018-05-31 | 广州华睿光电材料有限公司 | 高聚物、包含其的混合物、组合物和有机电子器件以及用于聚合的单体 |
| US11453745B2 (en) | 2016-11-23 | 2022-09-27 | Guangzhou Chinaray Optoelectronic Materials Ltd. | High polymer, mixture containing same, composition, organic electronic component, and monomer for polymerization |
| US11634444B2 (en) | 2016-11-23 | 2023-04-25 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Metal organic complex, high polymer, composition, and organic electronic component |
| WO2018095888A1 (en) | 2016-11-25 | 2018-05-31 | Merck Patent Gmbh | Bisbenzofuran-fused 2,8-diaminoindeno[1,2-b]fluorene derivatives and related compounds as materials for organic electroluminescent devices (oled) |
| WO2018095940A1 (en) | 2016-11-25 | 2018-05-31 | Merck Patent Gmbh | Bisbenzofuran-fused indeno[1,2-b]fluorene derivatives and related compounds as materials for organic electroluminescent devices (oled) |
| WO2018099846A1 (de) | 2016-11-30 | 2018-06-07 | Merck Patent Gmbh | Verbindungen mit valerolaktam-strukturen |
| US11555048B2 (en) | 2016-12-01 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018104194A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018104195A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen zur verwendung in oleds |
| WO2018104193A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| EP3978491A1 (de) | 2016-12-05 | 2022-04-06 | Merck Patent GmbH | Stickstoffhaltige heterocyclen zur verwendung in oleds |
| WO2018103744A1 (zh) | 2016-12-08 | 2018-06-14 | 广州华睿光电材料有限公司 | 混合物、组合物及有机电子器件 |
| US10978642B2 (en) | 2016-12-08 | 2021-04-13 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Mixture, composition and organic electronic device |
| US11161933B2 (en) | 2016-12-13 | 2021-11-02 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Conjugated polymer and use thereof in organic electronic device |
| US11548905B2 (en) | 2016-12-15 | 2023-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10490753B2 (en) | 2016-12-15 | 2019-11-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11545636B2 (en) | 2016-12-15 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10811618B2 (en) | 2016-12-19 | 2020-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018114883A1 (de) | 2016-12-22 | 2018-06-28 | Merck Patent Gmbh | Mischungen umfassend mindestens zwei organisch funktionelle verbindungen |
| US11292875B2 (en) | 2016-12-22 | 2022-04-05 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Cross-linkable polymer based on Diels-Alder reaction and use thereof in organic electronic device |
| US11289654B2 (en) | 2016-12-22 | 2022-03-29 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Polymers containing furanyl crosslinkable groups and uses thereof |
| WO2018113785A1 (zh) | 2016-12-22 | 2018-06-28 | 广州华睿光电材料有限公司 | 含呋喃交联基团的聚合物及其应用 |
| WO2018114882A1 (de) | 2016-12-22 | 2018-06-28 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US11152579B2 (en) | 2016-12-28 | 2021-10-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018127465A1 (de) | 2017-01-04 | 2018-07-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| EP4212540A1 (de) | 2017-01-09 | 2023-07-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3689890A1 (de) | 2017-01-09 | 2020-08-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11201298B2 (en) | 2017-01-09 | 2021-12-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3345914A1 (de) | 2017-01-09 | 2018-07-11 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11780865B2 (en) | 2017-01-09 | 2023-10-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10804475B2 (en) | 2017-01-11 | 2020-10-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11545637B2 (en) | 2017-01-13 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10629820B2 (en) | 2017-01-18 | 2020-04-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10964904B2 (en) | 2017-01-20 | 2021-03-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11566034B2 (en) | 2017-01-20 | 2023-01-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11053268B2 (en) | 2017-01-20 | 2021-07-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018134392A1 (en) | 2017-01-23 | 2018-07-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11765968B2 (en) | 2017-01-23 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11765966B2 (en) | 2017-01-24 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11050028B2 (en) | 2017-01-24 | 2021-06-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018138039A1 (de) | 2017-01-25 | 2018-08-02 | Merck Patent Gmbh | Carbazolderivate |
| WO2018138306A1 (de) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018141706A1 (de) | 2017-02-02 | 2018-08-09 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018149769A1 (de) | 2017-02-14 | 2018-08-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10978647B2 (en) | 2017-02-15 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10822361B2 (en) | 2017-02-22 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10844084B2 (en) | 2017-02-22 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11697661B2 (en) | 2017-02-22 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11254697B2 (en) | 2017-02-22 | 2022-02-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11760770B2 (en) | 2017-02-22 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018158232A1 (en) | 2017-03-01 | 2018-09-07 | Merck Patent Gmbh | Organic electroluminescent device |
| WO2018157981A1 (de) | 2017-03-02 | 2018-09-07 | Merck Patent Gmbh | Materialien für organische elektronische vorrichtungen |
| US10882877B2 (en) | 2017-03-03 | 2021-01-05 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including the organometallic compound, and diagnostic compositions including the organometallic compound |
| US10745431B2 (en) | 2017-03-08 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10923667B2 (en) | 2017-03-08 | 2021-02-16 | Samsung Electronics Co., Ltd. | Organometallic compound, composition containing the organometallic compound, and organic light-emitting device including the organometallic compound |
| US10741780B2 (en) | 2017-03-10 | 2020-08-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018166932A1 (de) | 2017-03-13 | 2018-09-20 | Merck Patent Gmbh | Verbindungen mit arylamin-strukturen |
| WO2018166934A1 (de) | 2017-03-15 | 2018-09-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10672998B2 (en) | 2017-03-23 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10873037B2 (en) | 2017-03-28 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10910577B2 (en) | 2017-03-28 | 2021-02-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3985012A1 (de) | 2017-03-29 | 2022-04-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11192910B2 (en) | 2017-03-29 | 2021-12-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10844085B2 (en) | 2017-03-29 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11725021B2 (en) | 2017-03-29 | 2023-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11158820B2 (en) | 2017-03-29 | 2021-10-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11056658B2 (en) | 2017-03-29 | 2021-07-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3730506A1 (de) | 2017-03-29 | 2020-10-28 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11678563B2 (en) | 2017-03-29 | 2023-06-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3381927A1 (de) | 2017-03-29 | 2018-10-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10862046B2 (en) | 2017-03-30 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11139443B2 (en) | 2017-03-31 | 2021-10-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11276829B2 (en) | 2017-03-31 | 2022-03-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10777754B2 (en) | 2017-04-11 | 2020-09-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11038117B2 (en) | 2017-04-11 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018189134A1 (de) | 2017-04-13 | 2018-10-18 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| US11591356B2 (en) | 2017-04-21 | 2023-02-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11101434B2 (en) | 2017-04-21 | 2021-08-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10975113B2 (en) | 2017-04-21 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11566035B2 (en) | 2017-04-21 | 2023-01-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11084838B2 (en) | 2017-04-21 | 2021-08-10 | Universal Display Corporation | Organic electroluminescent materials and device |
| WO2018197447A1 (de) | 2017-04-25 | 2018-11-01 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| US11038137B2 (en) | 2017-04-28 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10910570B2 (en) | 2017-04-28 | 2021-02-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11117897B2 (en) | 2017-05-01 | 2021-09-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11702420B2 (en) | 2017-05-01 | 2023-07-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10941170B2 (en) | 2017-05-03 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11201299B2 (en) | 2017-05-04 | 2021-12-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10870668B2 (en) | 2017-05-05 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10862055B2 (en) | 2017-05-05 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11377459B2 (en) | 2017-05-05 | 2022-07-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10930864B2 (en) | 2017-05-10 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10944060B2 (en) | 2017-05-11 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4141010A1 (de) | 2017-05-11 | 2023-03-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3401318A1 (de) | 2017-05-11 | 2018-11-14 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2018206526A1 (en) | 2017-05-11 | 2018-11-15 | Merck Patent Gmbh | Organoboron complexes for organic electroluminescent devices |
| WO2018206537A1 (en) | 2017-05-11 | 2018-11-15 | Merck Patent Gmbh | Carbazole-based bodipys for organic electroluminescent devices |
| US10822362B2 (en) | 2017-05-11 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10790455B2 (en) | 2017-05-18 | 2020-09-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10934293B2 (en) | 2017-05-18 | 2021-03-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10944062B2 (en) | 2017-05-18 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10840459B2 (en) | 2017-05-18 | 2020-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11038115B2 (en) | 2017-05-18 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and device |
| WO2018215318A1 (de) | 2017-05-22 | 2018-11-29 | Merck Patent Gmbh | Hexazyklische heteroaromatische verbindungen für elektronische vorrichtungen |
| US10930862B2 (en) | 2017-06-01 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3418285A1 (de) | 2017-06-20 | 2018-12-26 | Idemitsu Kosan Co., Ltd. | Zusammensetzung mit einem substituierten ir-komplex und einem mit einem heteroatom verbrückten phenylchinazolin |
| WO2018234220A1 (de) | 2017-06-21 | 2018-12-27 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US11678565B2 (en) | 2017-06-23 | 2023-06-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11814403B2 (en) | 2017-06-23 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018234346A1 (en) | 2017-06-23 | 2018-12-27 | Merck Patent Gmbh | MATERIALS FOR ORGANIC ELECTROLUMINESCENT DEVICES |
| EP3418286A1 (de) | 2017-06-23 | 2018-12-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11495757B2 (en) | 2017-06-23 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10968226B2 (en) | 2017-06-23 | 2021-04-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11832510B2 (en) | 2017-06-23 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11552261B2 (en) | 2017-06-23 | 2023-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11802136B2 (en) | 2017-06-23 | 2023-10-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11758804B2 (en) | 2017-06-23 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11174259B2 (en) | 2017-06-23 | 2021-11-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11725022B2 (en) | 2017-06-23 | 2023-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11731975B2 (en) | 2017-06-23 | 2023-08-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11608321B2 (en) | 2017-06-23 | 2023-03-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11958825B2 (en) | 2017-06-23 | 2024-04-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019002198A1 (en) | 2017-06-26 | 2019-01-03 | Merck Patent Gmbh | HOMOGENEOUS MIXTURES |
| WO2019002190A1 (en) | 2017-06-28 | 2019-01-03 | Merck Patent Gmbh | MATERIALS FOR ELECTRONIC DEVICES |
| WO2019007866A1 (de) | 2017-07-05 | 2019-01-10 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2019007867A1 (de) | 2017-07-05 | 2019-01-10 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| EP4186898A1 (de) | 2017-07-05 | 2023-05-31 | Merck Patent GmbH | Zusammensetzung für organische elektronische verbindungen |
| US11469382B2 (en) | 2017-07-12 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11765970B2 (en) | 2017-07-26 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11917843B2 (en) | 2017-07-26 | 2024-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11322691B2 (en) | 2017-07-26 | 2022-05-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11239433B2 (en) | 2017-07-26 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228010B2 (en) | 2017-07-26 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4185086A1 (de) | 2017-07-26 | 2023-05-24 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2019020654A1 (en) | 2017-07-28 | 2019-01-31 | Merck Patent Gmbh | SPIROBIFLUORENE DERIVATIVES FOR USE IN ELECTRONIC DEVICES |
| US11744141B2 (en) | 2017-08-09 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3783006A1 (de) | 2017-08-10 | 2021-02-24 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3444258A2 (de) | 2017-08-10 | 2019-02-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11349083B2 (en) | 2017-08-10 | 2022-05-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11910699B2 (en) | 2017-08-10 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11508913B2 (en) | 2017-08-10 | 2022-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11744142B2 (en) | 2017-08-10 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11462697B2 (en) | 2017-08-22 | 2022-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11723269B2 (en) | 2017-08-22 | 2023-08-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11437591B2 (en) | 2017-08-24 | 2022-09-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11605791B2 (en) | 2017-09-01 | 2023-03-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11424420B2 (en) | 2017-09-07 | 2022-08-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11696492B2 (en) | 2017-09-07 | 2023-07-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11444249B2 (en) | 2017-09-07 | 2022-09-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019048443A1 (de) | 2017-09-08 | 2019-03-14 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US10964895B2 (en) | 2017-09-11 | 2021-03-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10608188B2 (en) | 2017-09-11 | 2020-03-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019052933A1 (de) | 2017-09-12 | 2019-03-21 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11778897B2 (en) | 2017-09-20 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3466954A1 (de) | 2017-10-04 | 2019-04-10 | Idemitsu Kosan Co., Ltd. | Mit einem heteroatom verbrückte kondensierte phenylchinazoline |
| WO2019068679A1 (en) | 2017-10-06 | 2019-04-11 | Merck Patent Gmbh | MATERIALS FOR ORGANIC ELECTROLUMINESCENT DEVICES |
| WO2019076789A1 (en) | 2017-10-17 | 2019-04-25 | Merck Patent Gmbh | MATERIALS FOR ORGANIC ELECTROLUMINESCENT DEVICES |
| WO2019081391A1 (de) | 2017-10-24 | 2019-05-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11183646B2 (en) | 2017-11-07 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11910702B2 (en) | 2017-11-07 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent devices |
| US11685756B2 (en) | 2017-11-07 | 2023-06-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11214587B2 (en) | 2017-11-07 | 2022-01-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019096717A2 (de) | 2017-11-14 | 2019-05-23 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| US11168103B2 (en) | 2017-11-17 | 2021-11-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11011710B2 (en) | 2017-11-23 | 2021-05-18 | Samsung Electronics Co., Ltd. | Organometallic compound and organic light-emitting device including the same |
| EP4242286A2 (de) | 2017-11-23 | 2023-09-13 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2019101719A1 (de) | 2017-11-23 | 2019-05-31 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2019101835A1 (en) | 2017-11-24 | 2019-05-31 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2019101833A1 (en) | 2017-11-24 | 2019-05-31 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP3878855A1 (de) | 2017-11-28 | 2021-09-15 | University of Southern California | Carbenverbindungen und organische elektrolumineszente vorrichtungen |
| EP3489243A1 (de) | 2017-11-28 | 2019-05-29 | University of Southern California | Carbenverbindungen und organische elektrolumineszente vorrichtungen |
| US11825735B2 (en) | 2017-11-28 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3492480A2 (de) | 2017-11-29 | 2019-06-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3492528A1 (de) | 2017-11-30 | 2019-06-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11937503B2 (en) | 2017-11-30 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11404651B2 (en) | 2017-12-14 | 2022-08-02 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Transition metal complex material and application thereof in electronic devices |
| US11594690B2 (en) | 2017-12-14 | 2023-02-28 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Organometallic complex, and polymer, mixture and formulation comprising same, and use thereof in electronic device |
| US10971687B2 (en) | 2017-12-14 | 2021-04-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11674080B2 (en) | 2017-12-14 | 2023-06-13 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Transition metal complex, polymer, mixture, formulation and use thereof |
| US11233204B2 (en) | 2017-12-14 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11233205B2 (en) | 2017-12-14 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019115577A1 (en) | 2017-12-15 | 2019-06-20 | Merck Patent Gmbh | Substituted aromatic amines for use in organic electroluminescent devices |
| WO2019121458A1 (de) | 2017-12-19 | 2019-06-27 | Merck Patent Gmbh | Heterocyclische verbindung zur verwendung in electronischen vorrichtungen |
| WO2019121483A1 (en) | 2017-12-20 | 2019-06-27 | Merck Patent Gmbh | Heteroaromatic compounds |
| US11680059B2 (en) | 2017-12-21 | 2023-06-20 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Organic mixture and application thereof in organic electronic devices |
| US11700765B2 (en) | 2018-01-10 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11081659B2 (en) | 2018-01-10 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11818946B2 (en) | 2018-01-11 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11515493B2 (en) | 2018-01-11 | 2022-11-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11271177B2 (en) | 2018-01-11 | 2022-03-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019145316A1 (de) | 2018-01-25 | 2019-08-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11367840B2 (en) | 2018-01-26 | 2022-06-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11542289B2 (en) | 2018-01-26 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4019526A1 (de) | 2018-01-26 | 2022-06-29 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11957050B2 (en) | 2018-02-09 | 2024-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11910708B2 (en) | 2018-02-09 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11239434B2 (en) | 2018-02-09 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342509B2 (en) | 2018-02-09 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11697662B2 (en) | 2018-02-09 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11180519B2 (en) | 2018-02-09 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019170572A1 (en) | 2018-03-06 | 2019-09-12 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2019170578A1 (en) | 2018-03-06 | 2019-09-12 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11279722B2 (en) | 2018-03-12 | 2022-03-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11142538B2 (en) | 2018-03-12 | 2021-10-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11165028B2 (en) | 2018-03-12 | 2021-11-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11700766B2 (en) | 2018-03-12 | 2023-07-11 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11746122B2 (en) | 2018-03-12 | 2023-09-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11557733B2 (en) | 2018-03-12 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11217757B2 (en) | 2018-03-12 | 2022-01-04 | Universal Display Corporation | Host materials for electroluminescent devices |
| WO2019175149A1 (en) | 2018-03-16 | 2019-09-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11390639B2 (en) | 2018-04-13 | 2022-07-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11882759B2 (en) | 2018-04-13 | 2024-01-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11616203B2 (en) | 2018-04-17 | 2023-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11515494B2 (en) | 2018-05-04 | 2022-11-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11753427B2 (en) | 2018-05-04 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342513B2 (en) | 2018-05-04 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11839142B2 (en) | 2018-05-04 | 2023-12-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11793073B2 (en) | 2018-05-06 | 2023-10-17 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11844267B2 (en) | 2018-05-25 | 2023-12-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11459349B2 (en) | 2018-05-25 | 2022-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11450822B2 (en) | 2018-05-25 | 2022-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019229011A1 (de) | 2018-05-30 | 2019-12-05 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| US11716900B2 (en) | 2018-05-30 | 2023-08-01 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11296283B2 (en) | 2018-06-04 | 2022-04-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11404653B2 (en) | 2018-06-04 | 2022-08-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11925103B2 (en) | 2018-06-05 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2019233904A1 (de) | 2018-06-07 | 2019-12-12 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| US11339182B2 (en) | 2018-06-07 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228004B2 (en) | 2018-06-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11261207B2 (en) | 2018-06-25 | 2022-03-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2020011686A1 (de) | 2018-07-09 | 2020-01-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11753425B2 (en) | 2018-07-11 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2020016264A1 (en) | 2018-07-20 | 2020-01-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020026133A1 (en) | 2018-07-30 | 2020-02-06 | Idemitsu Kosan Co., Ltd. | Polycyclic compound, organic electroluminescence device, and electronic device |
| EP3604477A1 (de) | 2018-07-30 | 2020-02-05 | Idemitsu Kosan Co., Ltd. | Polycyclische verbindung, organische elektrolumineszenzvorrichtung und elektronische vorrichtung |
| EP3608319A1 (de) | 2018-08-07 | 2020-02-12 | Idemitsu Kosan Co., Ltd. | Kondensierte azazyklen als organische lichtemittierende vorrichtungen und materialien zur verwendung darin |
| EP3613751A1 (de) | 2018-08-22 | 2020-02-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4206210A1 (de) | 2018-08-22 | 2023-07-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2020043640A1 (en) | 2018-08-28 | 2020-03-05 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020043657A1 (en) | 2018-08-28 | 2020-03-05 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020043646A1 (en) | 2018-08-28 | 2020-03-05 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11233203B2 (en) | 2018-09-06 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11939293B2 (en) | 2018-09-11 | 2024-03-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11485706B2 (en) | 2018-09-11 | 2022-11-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| DE202019005923U1 (de) | 2018-09-12 | 2023-06-27 | MERCK Patent Gesellschaft mit beschränkter Haftung | Elektrolumineszierende Vorrichtungen |
| WO2020053150A1 (en) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020053315A1 (de) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Elektrolumineszierende vorrichtungen |
| WO2020053314A1 (de) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Elektrolumineszierende vorrichtungen |
| DE202019005924U1 (de) | 2018-09-12 | 2023-05-10 | MERCK Patent Gesellschaft mit beschränkter Haftung | Elektrolumineszierende Vorrichtungen |
| US11718634B2 (en) | 2018-09-14 | 2023-08-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11903305B2 (en) | 2018-09-24 | 2024-02-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2020064662A2 (de) | 2018-09-27 | 2020-04-02 | Merck Patent Gmbh | Verfahren zur herstellung von sterisch gehinderten stickstoffhaltigen heteroaromatischen verbindungen |
| EP4190880A1 (de) | 2018-09-27 | 2023-06-07 | Merck Patent GmbH | Verbindungen, die in einer organischen elektronischen vorrichtung als aktive verbindungen einsetzbar sind |
| WO2020064666A1 (de) | 2018-09-27 | 2020-04-02 | Merck Patent Gmbh | Verbindungen, die in einer organischen elektronischen vorrichtung als aktive verbindungen einsetzbar sind |
| US11469383B2 (en) | 2018-10-08 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495752B2 (en) | 2018-10-08 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11476430B2 (en) | 2018-10-15 | 2022-10-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11515482B2 (en) | 2018-10-23 | 2022-11-29 | Universal Display Corporation | Deep HOMO (highest occupied molecular orbital) emitter device structures |
| WO2020089138A1 (en) | 2018-10-31 | 2020-05-07 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11469384B2 (en) | 2018-11-02 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11839141B2 (en) | 2018-11-02 | 2023-12-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2020094539A1 (de) | 2018-11-05 | 2020-05-14 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2020094542A1 (de) | 2018-11-06 | 2020-05-14 | Merck Patent Gmbh | 5,6-diphenyl-5,6-dihydro-dibenz[c,e][1,2]azaphosphorin- und 6-phenyl-6h-dibenzo[c,e][1,2]thiazin-5,5-dioxid-derivate und ähnliche verbindungen als organische elektrolumineszenzmaterialien für oleds |
| WO2020099349A1 (de) | 2018-11-14 | 2020-05-22 | Merck Patent Gmbh | Zur herstellung einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2020099307A1 (de) | 2018-11-15 | 2020-05-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11825736B2 (en) | 2018-11-19 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11963441B2 (en) | 2018-11-26 | 2024-04-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11672176B2 (en) | 2018-11-28 | 2023-06-06 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11515489B2 (en) | 2018-11-28 | 2022-11-29 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11716899B2 (en) | 2018-11-28 | 2023-08-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11706980B2 (en) | 2018-11-28 | 2023-07-18 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11672165B2 (en) | 2018-11-28 | 2023-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11690285B2 (en) | 2018-11-28 | 2023-06-27 | Universal Display Corporation | Electroluminescent devices |
| US11623936B2 (en) | 2018-12-11 | 2023-04-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11737349B2 (en) | 2018-12-12 | 2023-08-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11834459B2 (en) | 2018-12-12 | 2023-12-05 | Universal Display Corporation | Host materials for electroluminescent devices |
| WO2020127165A1 (de) | 2018-12-19 | 2020-06-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020148243A1 (en) | 2019-01-16 | 2020-07-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020148303A1 (de) | 2019-01-17 | 2020-07-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11780829B2 (en) | 2019-01-30 | 2023-10-10 | The University Of Southern California | Organic electroluminescent materials and devices |
| EP3690973A1 (de) | 2019-01-30 | 2020-08-05 | University Of Southern California | Organische elektrolumineszente materialien und vorrichtungen |
| US11812624B2 (en) | 2019-01-30 | 2023-11-07 | The University Of Southern California | Organic electroluminescent materials and devices |
| US11844266B2 (en) | 2019-01-31 | 2023-12-12 | Samsung Electronics Co., Ltd. | Organometallic compound and organic light-emitting device including the same |
| EP3689889A1 (de) | 2019-02-01 | 2020-08-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4301117A2 (de) | 2019-02-01 | 2024-01-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11325932B2 (en) | 2019-02-08 | 2022-05-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11370809B2 (en) | 2019-02-08 | 2022-06-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2020169241A1 (de) | 2019-02-18 | 2020-08-27 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| US11773320B2 (en) | 2019-02-21 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11871653B2 (en) | 2019-02-22 | 2024-01-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11758807B2 (en) | 2019-02-22 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11557738B2 (en) | 2019-02-22 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11512093B2 (en) | 2019-03-04 | 2022-11-29 | Universal Display Corporation | Compound used for organic light emitting device (OLED), consumer product and formulation |
| WO2020178230A1 (en) | 2019-03-04 | 2020-09-10 | Merck Patent Gmbh | Ligands for nano-sized materials |
| US11739081B2 (en) | 2019-03-11 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11637261B2 (en) | 2019-03-12 | 2023-04-25 | Universal Display Corporation | Nanopatch antenna outcoupling structure for use in OLEDs |
| US11569480B2 (en) | 2019-03-12 | 2023-01-31 | Universal Display Corporation | Plasmonic OLEDs and vertical dipole emitters |
| WO2020182779A1 (de) | 2019-03-12 | 2020-09-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11963389B2 (en) | 2019-03-12 | 2024-04-16 | Universal Display Corporation | Plasmonic OLEDs and vertical dipole emitters |
| WO2020187865A1 (de) | 2019-03-20 | 2020-09-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020193447A1 (de) | 2019-03-25 | 2020-10-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| EP3715353A1 (de) | 2019-03-26 | 2020-09-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11963438B2 (en) | 2019-03-26 | 2024-04-16 | The University Of Southern California | Organic electroluminescent materials and devices |
| EP4134371A2 (de) | 2019-03-26 | 2023-02-15 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2020208051A1 (en) | 2019-04-11 | 2020-10-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11639363B2 (en) | 2019-04-22 | 2023-05-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11613550B2 (en) | 2019-04-30 | 2023-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices comprising benzimidazole-containing metal complexes |
| US11495756B2 (en) | 2019-05-07 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11807654B2 (en) | 2019-05-10 | 2023-11-07 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including organometallic compound, and diagnostic composition including organometallic compound |
| US11827651B2 (en) | 2019-05-13 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11634445B2 (en) | 2019-05-21 | 2023-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3750897A1 (de) | 2019-06-10 | 2020-12-16 | Universal Display Corporation | Organische elektrolumineszente materialien und geräte |
| US11832509B2 (en) | 2019-06-13 | 2023-11-28 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including the same, and diagnostic composition including the organometallic compound |
| US11858949B2 (en) | 2019-06-13 | 2024-01-02 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including the same, and diagnostic composition including the organometallic compound |
| US11778899B2 (en) | 2019-06-13 | 2023-10-03 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including the same, and diagnostic composition including the organometallic compound |
| US11647667B2 (en) | 2019-06-14 | 2023-05-09 | Universal Display Corporation | Organic electroluminescent compounds and organic light emitting devices using the same |
| US11920070B2 (en) | 2019-07-12 | 2024-03-05 | The University Of Southern California | Luminescent janus-type, two-coordinated metal complexes |
| US11926638B2 (en) | 2019-07-22 | 2024-03-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11685754B2 (en) | 2019-07-22 | 2023-06-27 | Universal Display Corporation | Heteroleptic organic electroluminescent materials |
| WO2021013775A1 (de) | 2019-07-22 | 2021-01-28 | Merck Patent Gmbh | Verfahren zur herstellung ortho-metallierter metallverbindungen |
| EP3771717A1 (de) | 2019-07-30 | 2021-02-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4219515A1 (de) | 2019-07-30 | 2023-08-02 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11708355B2 (en) | 2019-08-01 | 2023-07-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11889749B2 (en) | 2019-08-09 | 2024-01-30 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including organometallic compound, and diagnostic composition including organometallic compound |
| US11374181B2 (en) | 2019-08-14 | 2022-06-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11930699B2 (en) | 2019-08-15 | 2024-03-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3778614A1 (de) | 2019-08-16 | 2021-02-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2021037401A1 (de) | 2019-08-26 | 2021-03-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11925105B2 (en) | 2019-08-26 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11937494B2 (en) | 2019-08-28 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11600787B2 (en) | 2019-08-30 | 2023-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021043703A1 (de) | 2019-09-02 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021043755A1 (de) | 2019-09-03 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11820783B2 (en) | 2019-09-06 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021052924A1 (en) | 2019-09-16 | 2021-03-25 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021052921A1 (de) | 2019-09-19 | 2021-03-25 | Merck Patent Gmbh | Mischung von zwei hostmaterialien und organische elektrolumineszierende vorrichtung damit |
| WO2021053046A1 (de) | 2019-09-20 | 2021-03-25 | Merck Patent Gmbh | Peri-kondensierte heterozyklische verbindungen als materialien für elektronische vorrichtungen |
| US11864458B2 (en) | 2019-10-08 | 2024-01-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11950493B2 (en) | 2019-10-15 | 2024-04-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11697653B2 (en) | 2019-10-21 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021078710A1 (en) | 2019-10-22 | 2021-04-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11919914B2 (en) | 2019-10-25 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021078831A1 (de) | 2019-10-25 | 2021-04-29 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| US11765965B2 (en) | 2019-10-30 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3816175A1 (de) | 2019-11-04 | 2021-05-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2021089450A1 (en) | 2019-11-04 | 2021-05-14 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021089447A1 (de) | 2019-11-04 | 2021-05-14 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021094269A1 (en) | 2019-11-12 | 2021-05-20 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11889708B2 (en) | 2019-11-14 | 2024-01-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021110741A1 (en) | 2019-12-04 | 2021-06-10 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021122535A1 (de) | 2019-12-17 | 2021-06-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021122538A1 (de) | 2019-12-18 | 2021-06-24 | Merck Patent Gmbh | Aromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021122740A1 (de) | 2019-12-19 | 2021-06-24 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| EP4151644A1 (de) | 2020-01-06 | 2023-03-22 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3845545A1 (de) | 2020-01-06 | 2021-07-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11778895B2 (en) | 2020-01-13 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4294157A2 (de) | 2020-01-28 | 2023-12-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3858945A1 (de) | 2020-01-28 | 2021-08-04 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11917900B2 (en) | 2020-01-28 | 2024-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021151922A1 (de) | 2020-01-29 | 2021-08-05 | Merck Patent Gmbh | Benzimidazol-derivate |
| US11932660B2 (en) | 2020-01-29 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2021170522A1 (de) | 2020-02-25 | 2021-09-02 | Merck Patent Gmbh | Verwendung von heterocyclischen verbindungen in einer organischen elektronischen vorrichtung |
| WO2021175706A1 (de) | 2020-03-02 | 2021-09-10 | Merck Patent Gmbh | Verwendung von sulfonverbindungen in einer organischen elektronischen vorrichtung |
| WO2021180614A1 (de) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021180625A1 (de) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021185712A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021185829A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021191058A1 (en) | 2020-03-23 | 2021-09-30 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021191117A1 (de) | 2020-03-24 | 2021-09-30 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2021191183A1 (de) | 2020-03-26 | 2021-09-30 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021198213A1 (de) | 2020-04-02 | 2021-10-07 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021204646A1 (de) | 2020-04-06 | 2021-10-14 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021239772A1 (de) | 2020-05-29 | 2021-12-02 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021254984A1 (de) | 2020-06-18 | 2021-12-23 | Merck Patent Gmbh | Indenoazanaphthaline |
| WO2021259824A1 (de) | 2020-06-23 | 2021-12-30 | Merck Patent Gmbh | Verfahren zur herstellung einer mischung |
| WO2022002771A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022002772A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| EP3937268A1 (de) | 2020-07-10 | 2022-01-12 | Universal Display Corporation | Plasmonische oleds und vertikale dipolstrahler |
| WO2022017997A1 (en) | 2020-07-22 | 2022-01-27 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021170886A2 (de) | 2020-08-06 | 2021-09-02 | Merck Patent Gmbh | Elektronische vorrichtung |
| WO2022029096A1 (de) | 2020-08-06 | 2022-02-10 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022034046A1 (de) | 2020-08-13 | 2022-02-17 | Merck Patent Gmbh | Metallkomplexe |
| WO2022038065A1 (de) | 2020-08-18 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022038066A1 (de) | 2020-08-19 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022069422A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Verbindungen zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen |
| WO2022069421A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen einsetzbare verbindungen |
| WO2022079067A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Verbindungen mit heteroatomen für organische elektrolumineszenzvorrichtungen |
| WO2022079068A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022101171A1 (de) | 2020-11-10 | 2022-05-19 | Merck Patent Gmbh | Schwefelhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| EP4016659A1 (de) | 2020-11-16 | 2022-06-22 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4329463A2 (de) | 2020-11-24 | 2024-02-28 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4001286A1 (de) | 2020-11-24 | 2022-05-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4001287A1 (de) | 2020-11-24 | 2022-05-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2022117473A1 (de) | 2020-12-02 | 2022-06-09 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022122682A2 (de) | 2020-12-10 | 2022-06-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022129116A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Indolo[3.2.1-jk]carbazole-6-carbonitril-derivate als blau fluoreszierende emitter zur verwendung in oleds |
| WO2022129113A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| WO2022129114A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022148717A1 (de) | 2021-01-05 | 2022-07-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022157343A1 (de) | 2021-01-25 | 2022-07-28 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| EP4039692A1 (de) | 2021-02-03 | 2022-08-10 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4059915A2 (de) | 2021-02-26 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4060758A2 (de) | 2021-02-26 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2022184601A1 (de) | 2021-03-02 | 2022-09-09 | Merck Patent Gmbh | Verbindungen für organische elektrolumineszenzvorrichtungen |
| EP4053137A1 (de) | 2021-03-05 | 2022-09-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4056578A1 (de) | 2021-03-12 | 2022-09-14 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4059941A1 (de) | 2021-03-15 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2022194799A1 (de) | 2021-03-18 | 2022-09-22 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| EP4074723A1 (de) | 2021-04-05 | 2022-10-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4075531A1 (de) | 2021-04-13 | 2022-10-19 | Universal Display Corporation | Plasmonische oleds und vertikale dipolstrahler |
| EP4075530A1 (de) | 2021-04-14 | 2022-10-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4086266A1 (de) | 2021-04-23 | 2022-11-09 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4079743A1 (de) | 2021-04-23 | 2022-10-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2022229126A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229298A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229234A1 (de) | 2021-04-30 | 2022-11-03 | Merck Patent Gmbh | Stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022243403A1 (de) | 2021-05-21 | 2022-11-24 | Merck Patent Gmbh | Verfahren zur kontinuierlichen aufreinigung von mindestens einem funktionalen material und vorrichtung zur kontinuierlichen aufreinigung von mindestens einem funktionalen material |
| EP4112701A2 (de) | 2021-06-08 | 2023-01-04 | University of Southern California | Molekulare ausrichtung homoleptischer iridiumphosphore |
| WO2022200638A1 (de) | 2021-07-06 | 2022-09-29 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023036976A1 (en) | 2021-09-13 | 2023-03-16 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2023041454A1 (de) | 2021-09-14 | 2023-03-23 | Merck Patent Gmbh | Borhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| EP4151699A1 (de) | 2021-09-17 | 2023-03-22 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2023052314A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052272A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052275A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052313A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023072799A1 (de) | 2021-10-27 | 2023-05-04 | Merck Patent Gmbh | Bor- und stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023094412A1 (de) | 2021-11-25 | 2023-06-01 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023099543A1 (en) | 2021-11-30 | 2023-06-08 | Merck Patent Gmbh | Compounds having fluorene structures |
| WO2023110742A1 (de) | 2021-12-13 | 2023-06-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| EP4212539A1 (de) | 2021-12-16 | 2023-07-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2023117837A1 (de) | 2021-12-21 | 2023-06-29 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2023152063A1 (de) | 2022-02-09 | 2023-08-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023152346A1 (de) | 2022-02-14 | 2023-08-17 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP4231804A2 (de) | 2022-02-16 | 2023-08-23 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2023161168A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Aromatische heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2023161167A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| EP4242285A1 (de) | 2022-03-09 | 2023-09-13 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4265626A2 (de) | 2022-04-18 | 2023-10-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2023213837A1 (de) | 2022-05-06 | 2023-11-09 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023222559A1 (de) | 2022-05-18 | 2023-11-23 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| EP4282863A1 (de) | 2022-05-24 | 2023-11-29 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4293001A1 (de) | 2022-06-08 | 2023-12-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2023247663A1 (de) | 2022-06-24 | 2023-12-28 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2023247662A1 (de) | 2022-06-24 | 2023-12-28 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| EP4299693A1 (de) | 2022-06-28 | 2024-01-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2024013004A1 (de) | 2022-07-11 | 2024-01-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024033282A1 (en) | 2022-08-09 | 2024-02-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP4326030A1 (de) | 2022-08-17 | 2024-02-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2024061942A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2024061948A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
Also Published As
| Publication number | Publication date |
|---|---|
| CN100573961C (zh) | 2009-12-23 |
| EP3299437B1 (de) | 2020-09-23 |
| CN101654466A (zh) | 2010-02-24 |
| US20110049500A1 (en) | 2011-03-03 |
| US9024308B2 (en) | 2015-05-05 |
| US11539005B2 (en) | 2022-12-27 |
| US7846763B2 (en) | 2010-12-07 |
| DE10338550A1 (de) | 2005-03-31 |
| US20060258043A1 (en) | 2006-11-16 |
| US10573828B2 (en) | 2020-02-25 |
| JP2007533774A (ja) | 2007-11-22 |
| WO2005019373A3 (de) | 2005-05-19 |
| US8916853B2 (en) | 2014-12-23 |
| US20170365802A1 (en) | 2017-12-21 |
| US20230108701A1 (en) | 2023-04-06 |
| JP4351702B2 (ja) | 2009-10-28 |
| EP3805338A1 (de) | 2021-04-14 |
| US20110049499A1 (en) | 2011-03-03 |
| US20200266366A1 (en) | 2020-08-20 |
| US8377740B2 (en) | 2013-02-19 |
| US20150073152A1 (en) | 2015-03-12 |
| US20110049501A1 (en) | 2011-03-03 |
| EP1658349A2 (de) | 2006-05-24 |
| CN101654466B (zh) | 2013-11-27 |
| EP3299437A1 (de) | 2018-03-28 |
| CN1871322A (zh) | 2006-11-29 |
| US9748498B2 (en) | 2017-08-29 |
| KR20070050859A (ko) | 2007-05-16 |
| EP1658349B1 (de) | 2017-09-20 |
| KR101186706B1 (ko) | 2012-09-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1658349B1 (de) | VERWENDUNG VON ÜBERGANGSMETALLKOMPLEXEN MIT CARBENLIGANDEN ALS EMITTER FÜR ORGANISCHE LICHT-EMITTIERENDE DIODEN (OLEDs) UND OLEDs | |
| EP2007779B1 (de) | Heteroleptische übergangsmetall-carben-komplexe und deren verwendung in organischen leuchtdioden (oleds) | |
| EP2205615B1 (de) | Übergangsmetallkomplexe mit verbrückten carbenliganden und deren verwendung in oleds | |
| DE102004057072A1 (de) | Verwendung von Übergangsmetall-Carbenkomplexen in organischen Licht-emittierenden Dioden (OLEDs) | |
| EP2007781B1 (de) | Übergangsmetallkomplexe, enthaltend einen nicht-carben- und ein oder zwei carbenliganden und deren verwendung in oleds | |
| EP2203461B1 (de) | Übergangsmetallkomplexe mit verbrückten carbenliganden und deren verwendung in oleds | |
| EP2044169B1 (de) | Verwendung von pt- und pd-bis- und tetracarbenkomplexen mit verbrückten carbenliganden in oleds | |
| EP1394171A1 (de) | Mehrkernige Metallkomplexe als Phosphoreszenzemitter in elektrolumineszierenden Schichtanordnungen | |
| DE102011084639A1 (de) | Organisches elektronisches bauelement mit dotierstoff, verwendung eines dotierstoffs und verfahren zur herstellung des dotierstoffs | |
| DE60314452T2 (de) | Elektrolumineszente verbindungen und vorrichtungen | |
| DE10330761A1 (de) | Mischungen von organischen zur Emission befähigten Halbleitern und Matrixmaterialien, deren Verwendung und Elektronikbauteile enthaltend dieses |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 200480030649.2 Country of ref document: CN |
|
| AK | Designated states |
Kind code of ref document: A2 Designated state(s): AE AG AL AM AT AU AZ BA BB BG BR BW BY BZ CA CH CN CO CR CU CZ DE DK DM DZ EC EE EG ES FI GB GD GE GH GM HR HU ID IL IN IS JP KE KG KP KR KZ LC LK LR LS LT LU LV MA MD MG MK MN MW MX MZ NA NI NO NZ OM PG PH PL PT RO RU SC SD SE SG SK SL SY TJ TM TN TR TT TZ UA UG US UZ VC VN YU ZA ZM ZW |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A2 Designated state(s): BW GH GM KE LS MW MZ NA SD SL SZ TZ UG ZM ZW AM AZ BY KG KZ MD RU TJ TM AT BE BG CH CY CZ DE DK EE ES FI FR GB GR HU IE IT LU MC NL PL PT RO SE SI SK TR BF BJ CF CG CI CM GA GN GQ GW ML MR NE SN TD TG |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 2006258043 Country of ref document: US Ref document number: 10568344 Country of ref document: US |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 1020067003352 Country of ref document: KR Ref document number: 2006523602 Country of ref document: JP |
|
| REEP | Request for entry into the european phase |
Ref document number: 2004764255 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2004764255 Country of ref document: EP |
|
| DPEN | Request for preliminary examination filed prior to expiration of 19th month from priority date (pct application filed from 20040101) | ||
| WWP | Wipo information: published in national office |
Ref document number: 2004764255 Country of ref document: EP |
|
| WWP | Wipo information: published in national office |
Ref document number: 10568344 Country of ref document: US |